
امروز دوشنبه ۳۱ اردیبهشت ۱۴۰۳
دسته بندی سایت
برچسب های مهم
پیوند ها
آمار بازدید سایت
ترکیب دو واکسن کوید19 مختلف حفاظت مشابه با واکسنهای mRNA را فراهم میکند - از جمله حفاظت در برابر نوع دلتا .
"Ewen Callaway"
یکی از کارکنان بخش بهداشت و درمان در نوناترابوری تایلند , یک شیشه واکسن فایزر - BioNTch کوید19 را بررسی میکند . مطالعه بعد از مطالعه نشان داد که افرادی که دو واکسن کوید19 متفاوت دریافت میکنند , پاسخهای ایمنی قوی تولید میکنند و اثرات جانبی بدتر از اثرات جانبی ناشی از رژیمهای استاندارد نیست .
اما اکنون , برای اولین بار , محققان نشان دادهاند که چنین رژیمهای " ترکیبی و تطبیقی " در جلوگیری از کوید19 بسیار موثر هستند - تقریبا منطبق یا حتی فراتر از عملکرد واکسنهای mRNA .
سطوح بالای آنتیبادی و دیگر پاسخهای ایمنی قوی ناشی از رژیمهای ترکیبی و تطبیقی پیشنهاد میکند که آنها حفاظت خوبی در برابر بیماری دارند. با این حال، مارتینا استر، متخصص سیستم ایمنی، در دانشگاه سارلند در هامبورگ آلمان میگوید: " من خوشحال بودم که میبینم این روش به همان اندازه که انتظار میرود موثر است." " این خبر واقعا خوبی است و قطعا بر عملکرد بالینی تاثیر خواهد گذاشت."
متیو اسنیپ , یک مامور واکسیناسیون در دانشگاه آکسفورد بریتانیا میگوید : " این دادههای موثر در حال ظهور , استفاده از این واکسنهای کوید19 تایید شده را در برنامههای استاندارد یا ترکیبی پشتیبانی میکنند . "
مطالعات از یک آزمایش طبیعی در ماه مارس آغاز شد زمانی که تعدادی از کشورها استفاده از واکسن تهیهشده توسط دانشگاه آکسفورد و شرکت داروسازی آسترازنکا در کمبریج را به طور جزئی یا کامل متوقف کردند.
این بدین معنی بود که برخی از افرادی که قبلا یک دوز از این واکسن را دریافت کرده بودند، پس از آن واکسن متفاوتی به عنوان تزریق خود داشتند.
تیم استر و چند نفر دیگر نشان دادند که این ترکیبات ترکیبی و تطبیقی ایمن بوده و منجر به یک پاسخ ایمنی قوی میشوند.
اکنون، سه تیم اولین اندازهگیریهای اثربخشی رژیمهای ترکیبی و تطبیقی را ارائه کردهاند.
این مطالعات به جمعیتهای مختلف در زمانهای مختلف - از جمله در طول ظهور نوع دلتا فوق عفونی - نگاهی انداختند اما همه آنها توافق دارند که واکسیناسیون ترکیبی و تطبیقی، یا هترولوگ، بسیار محافظ است.
یکی از آنها در سوئد رخ داد، جایی که مقامات بهداشتی استفاده از واکسن آکسفورد - آسترازنکا را به شدت کاهش دادند، که متکی بر ویروس سرماخوردگی شامپانزه تضعیفشده است. در نتیجه , بیش از 100000 نفر در سوئد یک دوز از آسترازنکا دریافت کردند , و به دنبال آن یک تزریق مبتنی بر mRNA - یا واکسن از مودرنا در کمبریج , ماساچوست , و یا واکسن توسعهیافته توسط شرکت داروسازی فایزر , واقع در نیویورک سیتی , و آزمایشگاه زیست فنآوری در ماینتس آلمان .
عدم تطابق سودمند
متخصص بیماریهای همهگیر , پیتر نوردستروم , در دانشگاه اومی سوئد و همکاران وی , دادههای موجود در دفاتر ثبت ملی سلامت کشور را تحلیل کردند که شامل واکسیناسیون و تست کوید19 و اطلاعات درمانی برای همه ساکنان است . آنها دریافتند که در مقایسه با افراد واکسینه نشده، کسانی که برنامه واکسیناسیون ترکیبی داشتند ۶۸ % کمتر احتمال ابتلا به عفونت علامتدار را داشتند، در حالی که ۴۳۰،۰۰۰ نفر که دو دوز از آسترازنکا را دریافت کرده بودند ۵۰ % کمتر احتمال ابتلا به این عفونت را داشتند. نوردستروم میگوید که این ها و ارقام دیگر روشن میسازند که رژیمهای هترولوگ موثرتر از دو دوز از آسترازنکا هستند.
این نتیجهگیری، تحلیل مشابهی را در دانمارک نشان میدهد که دارای ثبت ملی بهداشت و واکسیناسیون مشابه با ثبت سوئد است. متخصص بیماریهای همهگیر " می آژنوز گرم " در موسسه " استینز سروم " در کپنهاگ , و نویسندگان مشترک دریافتند که یک دوز از داروی آسترازنکا و به دنبال آن یک دوز از داروی Pfizer - BioNTch در جلوگیری از عفونت SARS - CoV - 2 موثر بود - یک اثر مشابه با دو دوز از فایزر . مطالعه آنها هنوز مورد بازبینی دقیق قرار نگرفته است.
نیازی به وفاداری به برند نیست
یک مطالعه نشان داد که رژیمهای ترکیبی و تطبیقی میتوانند موثرتر از دو دوز واکسن mRNA باشند. دانشمند ایمنی، تیری والزر، در اینسرم و دانشگاه لیون در فرانسه، و همکارانش دادههای ۲۵۱۲ کارمند مراقبتهای بهداشتی را تحلیل کردند که ترکیبی از واکسنهای آسترازنکا و فایزر و بیش از ۱۰،۰۰۰ نفر که دو دوز دوم را دریافت کردند را دریافت کردند. این تیم نشان داد که میزان عفونت SARS - CoV - 2 در گروه ترکیبی و match نصف گروهی بود که دو دوز از فایزر را دریافت کردند .
نوردستروم میگوید , واکسنهای ترکیبی کوید19 ممکن است تست اثربخشی را پشت سر گذاشته باشند , اما سوالات باقی میمانند , مانند اینکه چگونه واکسنهای ترکیبی و تطبیقی در طول زمان دوام خواهند آورد , و اینکه آیا و چه زمانی نیاز به تقویت با دوزهای اضافی دارند . در دادههای منتشر نشده، تیم او کشف کردهاست که دوام حفاظت اعطا شده توسط واکسیناسیون ترکیبی با واکسن mRNA قابلمقایسه است. اما این دادهها همچنین نشان میدهند که افراد در معرض خطر بالاتر از دوز سوم سود میبرند.
استر میگوید: دانستن اینکه واکسنهای ترکیبی و تطبیق بسیار موثر هستند، پیامدهای جهانی خواهد داشت. شواهدی وجود دارد که افراد دارای نقص ایمنی یک پاسخ ایمنی قوی نسبت به رژیمهای ترکیبی دارند، بنابراین این احتمال وجود دارد که ترکیب دوز بتواند از دریافت کنندگان پیوند عضو و دیگران با سیستم ایمنی ضعیف بهتر از رژیمهای استاندارد محافظت کند. این دادهها همچنین میتوانند از برنامههای مختلط ایمنسازی در کشورهای کمدرآمد حمایت کنند که ممکن است در آنها کمبود واکسنهای خاص وجود داشته باشد. او میگوید: " این دادهها واقعا برای سیاستها مهم هستند."
برچسب های مهم
.
۹ سپتامبر ۲۰۲۱ ۱۰.۲۸ بعد از ظهر
وان کوپر
استاد میکروبیولوژی و ژنتیک مولکولی، دانشگاه پیتسبرگ
ظهور گونههای کرونا ویروس تاثیر عظیم زیستشناسی تکاملی بر زندگی روزمره را برجسته کردهاست. اما اینکه چگونه جهشها، شانس تصادفی و انتخاب طبیعی واریانت ها را تولید میکنند یک فرآیند پیچیده است، و سردرگمی زیادی در مورد چگونگی و چرایی ظهور واریانت های جدید وجود داشتهاست.
تا همین اواخر، مشهورترین مثال از تکامل سریع، داستان پروانه پفکرده بود. در اواسط دهه ۱۸۰۰، کارخانههای منچستر انگلستان شروع به پوشش دادن زیستگاه بید در دوده کردند و رنگ سفید معمولی بید آنها را برای شکارچیان آشکار کرد. اما بعضی از بیدها جهشی داشتند که آنها را تاریکتر میکرد. از آنجا که آنها در دنیای جدیدشان استتار بهتری داشتند، میتوانستند از دست شکارچیان فرار کنند و بیشتر از همتایان سفیدشان تولید مثل کنند.
ما زیستشناس تکاملی و متخصص بیماریهای عفونی در دانشگاه پیتسبرگ هستیم که با همکار میکنند تا تکامل پاتوژن ها را ردیابی و کنترل کنند. در طول یک سال و نیم گذشته، ما به دقت دنبال کردیم که چگونه ویروس کرونا جهشهای مختلفی را در سراسر جهان به دست آوردهاست.
طبیعی است که تعجب کنیم که آیا واکسنهای کوید19 بسیار موثر منجر به ظهور واریانت های میشوند که از پرواز پروانه مانند واکسن فرار میکنند یا خیر . اما با توجه به اینکه تنها کمتر از ۴۰ % از مردم جهان دوز واکسن را تنها ۲ % در کشورهای کمدرآمد دریافت کردهاند - و تقریبا یک میلیون عفونت جدید که هر روز در سطح جهانی رخ میدهد، ظهور انواع جدید و مسری مانند دلتا، توسط انتقال کنترلنشده هدایت میشود، نه واکسن.
چگونه ویروس تغییر میکند
برای هر موجود زنده، از جمله یک ویروس، کپی کردن کد ژنتیکی آن جوهر تولید مثل است - اما این فرآیند اغلب ناقص است. کروناویروس ها از RNA برای اطلاعات ژنتیکی خود استفاده میکنند و کپی کردن RNA بیشتر مستعد خطا است تا استفاده از DNA. محققان نشان دادهاند که وقتی ویروس کرونا تکثیر میشود، حدود ۳ % از کپیهای ویروس جدید یک خطای جدید تصادفی دارند، در غیر این صورت به عنوان جهش شناخته میشوند.
هر عفونت میلیونها ویروس را در بدن فرد تولید میکند که منجر به بسیاری از کروناویروس های جهشیافته میشود. با این حال، تعداد ویروسهای جهشیافته با تعداد بسیار بیشتری از ویروسها که مشابه سویه آغاز کننده عفونت هستند، کوتاه میشود.
تقریبا تمام جهشهایی که رخ میدهند، اشکال بی ضرری هستند که نحوه عملکرد ویروس را تغییر نمیدهند - و در واقع دیگر جهشهایی که رخ میدهند، به ویروس آسیب میزنند. بخش کوچکی از تغییرات ممکن است ویروس را عفونی کند، اما این جهشیافتهها نیز باید خوششانس باشند. برای اینکه واریانت جدیدی ایجاد شود، باید با موفقیت به سراغ یک فرد جدید برود و کپیهای زیادی را تکرار کند.
انتقال یک تنگنای مهم است
بیشتر ویروسها در یک فرد مبتلا از نظر ژنتیکی مشابه با سویه هستند که عفونت را آغاز کردهاست. بسیار محتمل است که یکی از این کپیها - و نه یک جهش نادر - به شخص دیگری منتقل شود. تحقیقات نشان دادهاست که تقریبا هیچ ویروس جهشیافته از میزبان اصلی خود به فرد دیگری منتقل نمیشود.
و حتی اگر یک موتان جدید باعث عفونت شود، ویروسهای موتان معمولا با ویروسهای غیر موتان در میزبان جدید بیشتر میشوند و معمولا به شخص بعدی منتقل نمیشوند.
شانس کوچک انتقال یک موتانت "تنگنای جمعیت" نامیده میشود. این واقعیت که تنها تعداد کمی از ویروسهایی هستند که عفونت بعدی را آغاز میکنند، یک عامل تصادفی مهم است که احتمال بروز انواع جدید را محدود میکند. تولد هر واریانت جدید یک رویداد تصادفی شامل یک خطای کپی کردن و یک رویداد انتقال غیر محتمل است. از میان میلیون ها کپی کرونا ویروس در یک فرد مبتلا، احتمال اینکه یک موتان مناسب در میان افراد کمی باشد که به فرد دیگری گسترش یابد و به یک موتان جدید گسترش یابد، بسیار بعید است.
واریانت های جدید چگونه پدیدار میشوند؟
متاسفانه، گسترش کنترلنشده یک ویروس حتی میتواند بر تنگناها غلبه کند. در حالی که بیشتر جهشها هیچ تاثیری بر این ویروس ندارند، برخی میتوانند و میزان شیوع ویروس کرونا را افزایش دادهاند. اگر یک نژاد با گسترش سریع قادر به ایجاد تعداد زیادی از موارد کوید19 در جایی باشد , شروع به رقابت با سویههای مسری کمتر و تولید یک گونه جدید خواهد کرد - درست مانند گونه دلتا .
بسیاری از محققان در حال مطالعه این موضوع هستند که کدام جهشها منجر به نسخههای قابل انتقال بیشتری از کرونا ویروس میشوند. معلوم شد که واریانت های تمایل به داشتن بسیاری از جهشهای مشابه دارند که مقدار ویروس تولید شده توسط فرد مبتلا را افزایش میدهد. با بیش از یک میلیون عفونت جدید که هر روز اتفاق میافتد و میلیاردها نفر هنوز واکسینه نشده اند، میزبانهای حساس به ندرت در کمبود غذا قرار دارند. بنابراین، انتخاب طبیعی به نفع جهشهایی خواهد بود که میتوانند از همه این افراد واکسینه نشده بهرهبرداری کنند و کرونا ویروس را قابل انتقال کنند.
تحت این شرایط، بهترین راه برای محدود کردن تکامل کرونا ویروس، کاهش تعداد عفونتها است.
واکسن واریانت های جدید را متوقف میکند
واریانت دلتا در سراسر جهان گسترشیافته است و متغیرهای بعدی در حال حاضر در حال افزایش هستند. اگر هدف محدود کردن عفونت است، واکسنها پاسخ این سوال هستند.
با اینکه افراد واکسینه شده هنوز هم میتوانند به نوع دلتا آلوده شوند، اما نسبت به افراد واکسینه نشده، عفونتهای کوتاهتر و ملایمتر را تجربه میکنند. این امر تا حد زیادی شانس هر گونه ویروس جهشیافته را کاهش میدهد - چه آنهایی که ویروس را قابل انتقال میکنند و چه آنهایی که به آن اجازه میدهند از مصونیت خود در برابر واکسنها بگذرد - از پریدن از یک فرد به فرد دیگر.
در نهایت، هنگامی که تقریبا همه نسبت به ویروس کرونا از طریق واکسیناسیون مصونیت دارند، ویروسهایی که این مصونیت را از بین میبرند، میتوانند نسبت به دیگر سویهها برتری رقابتی به دست آورند. از نظر تئوری ممکن است که در این وضعیت، انتخاب طبیعی منجر به انواع مختلفی شود که میتوانند در افراد واکسینه شده بیماری جدی ایجاد کنند. با این حال، این جهشیافتهها هنوز باید از تنگنای جمعیت فرار کنند.
در حال حاضر، بعید به نظر میرسد که ایمنی ناشی از واکسن، بازیگر اصلی در ظهور واریانت باشد، زیرا عفونتهای جدید زیادی در حال وقوع هستند. این فقط یک بازی اعداد است. مزیت نسبی ویروس از فرار از واکسن، با فرصتهای گسترده برای آلوده کردن افراد واکسینه نشده، کم جلوه میکند.
جهان در حال حاضر شاهد رابطه بین تعداد عفونتها و افزایش جهشیافتهها بودهاست. ویروس کرونا تا ماهها بدون تغییر باقی ماند تا اینکه این بیماری همهگیر از کنترل خارج شد. با تعداد نسبتا کمی عفونت، کد ژنتیکی فرصتهای محدودی برای جهش داشت. اما هنگامی که خوشههای عفونت منفجر شدند، ویروس میلیون ها بار تکرار می شود و برخی از جهشها، جهشیافتههای مناسب تری تولید کردند.
بهترین راه برای جلوگیری از انتشار گونههای جدید، جلوگیری از انتشار آنها است و پاسخ به آن واکسیناسیون است.
خلاصه
پیشزمینه پیشرفت مداوم در کنترل مالاریای پلاسمودیوم فالسیپاروم نیاز به یک واکسن موثر و قابل گسترش را برجسته میسازد. RTS، S / AS۰۱، موثرترین نامزد واکسن مالاریا تا به امروز، ۵۶ درصد کارآیی را در طی ۱۲ ماه در کودکان آفریقایی نشان داد. بنابراین ما یک واکسن کاندید جدید برای ایمنی و کارایی را مورد ارزیابی قرار دادیم.
روشها در این آزمایش دو سویه کور، تصادفی، کنترلشده، فاز ۲ b، واکسن مبتنی بر پروتیین دورزوآیت با دوز کم R۲۱، با دو دوز مختلف از ماتریکس M کمکی (MM)، به کودکان ۵ تا ۱۷ ماهه در نانورو، بورکینافاسو - یک محیط انتقال بسیار فصلی مالاریا - داده شد. سه واکسیناسیون در فواصل ۴ هفتهای قبل از فصل مالاریا، با دوز چهارم ۱ سال بعد انجام شد. همه واکسنها به صورت عضلانی به ران تزریق شدند. گروه ۱، ۵ میکروگرم R۲۱ به علاوه ۲۵ میکروگرم MM، گروه ۲، ۵ میکروگرم R۲۱ به علاوه ۵۰ میکروگرم MM و گروه ۳، گروه کنترل، واکسیناسیون هاری را دریافت کردند. کودکان به طور تصادفی (۱: ۱: ۱)به گروههای ۱ تا ۳ اختصاص داده شدند. یک لیست تخصیص تصادفی با استفاده از روش تصادفی بلوکی با اندازه بلوک متغیر تولید شد که برای تخصیص شرکت کنندگان مورد استفاده قرار گرفت. شرکت کنندگان، خانوادههایشان، و تیم مطالعه محلی همگی ماسکزده بودند تا به تخصیص گروه بپردازند. تنها داروسازانی که واکسن را آماده میکردند، برای تخصیص این گروه مخفی نشده بودند. ایمنی واکسن، immunogenicity و کارایی واکسن بیش از یک سال ارزیابی شد. هدف اولیه، کارایی حفاظتی R۲۱ به علاوه MM (R۲۱ / MM)را از ۱۴ روز پس از سومین واکسیناسیون تا ۶ ماه ارزیابی کرد. تجزیه و تحلیل اولیه کارایی واکسن براساس یک جمعیت تغییر یافته قصد برای درمان بود، که شامل تمام شرکت کنندگانی میشد که سه واکسن دریافت کرده بودند، که اجازه میداد شرکت کنندگانی که واکسن اشتباهی را در هر نقطه زمانی دریافت میکردند، وارد مطالعه شوند. یافتهها از ۷ می تا ۱۳ ژوئن ۲۰۱۹، ۴۹۸ کودک ۵ تا ۱۷ ماهه غربالگری شدند و ۴۸ کودک از مطالعه حذف شدند. تعداد ۴۵۰ کودک وارد مطالعه شدند و حداقل یک نوبت واکسن دریافت کردند. ۱۵۰ کودک در گروه اول، ۱۵۰ کودک در گروه دوم و ۱۵۰ کودک در گروه سوم قرار گرفتند. بر روی Aug ۷، ۲۰۱۹ اجرا شد. R۲۱ / MM یک پروفایل ایمنی مطلوب داشت و به خوبی تحمل میشد. اکثر عوارض جانبی خفیف بودند و شایعترین عارضه تب بود. هیچ یک از هفت عارضه جدی به واکسن نسبت داده نشدند. در تحلیل اثربخشی اولیه ۶ ماهه، ۴۳ نفر (۲۹ %)از ۱۴۶ شرکتکننده در گروه ۱، ۳۸ نفر (۲۶ %)از ۱۴۶ شرکتکننده در گروه ۲، و ۱۰۵ نفر (۷۱ %)از ۱۴۷ شرکتکننده در گروه ۳ دچار مالاریا بالینی شدند. کارآیی واکسن در گروه ۱ ۷۴ % (۹۵ % CI ۶۳ - ۸۲)و در گروه ۲ ۷۷ % (۶۷ - ۸۴)در ۶ ماه بود. در یک سال، اثربخشی واکسن در ۷۷ درصد (۸۴ - ۶۷)در گروه ۱ بالا باقی ماند. آنتیبادی Asn - Ala - Asn - Pro (NANP)۲۸ روز پس از سومین واکسیناسیون، که با دوز کمکی بالاتر تقریبا دو برابر شد. پس از انجام اولین سری واکسیناسیون پس از گذشت یک سال از دریافت چهارمین دوز واکسن، تیتر آن رو به کاهش گذاشت اما به سطحی مشابه با بالاترین تیتر رسید.
تفسیر R۲۱ / MM در کودکان آفریقایی ایمن و immunogenic به نظر میرسد و کارایی سطح بالایی را نشان میدهد.
وقوع کوید19 در گروههای اولویتدار دریافتکننده واکسن کرونا ویروس ChAdOx1 nCoV - 19 ( نوترکیب ) : تجزیه و تحلیل مقدماتی از شمال هند
چکیده
سابقه و هدف : در شرایط کنترلشده تصادفی , اثربخشی واکسن نزدیک به 70 % در برابر کوید19 علامتدار توسط واکسن NCoV - 19 ChAdOx1 نشانداده شدهاست که یک واکسن نوترکیب آدنوویروس شامپانزه است که پروتئین اسپایک SARS - CoV - 2 را بیان میکند . با این حال، مطالعات تایید پس از آن برای تایید اعتبار پایانهها در دنیای واقعی ضروری است.
روشها : یک مطالعه مشاهدهای آیندهنگر در بیمارستان سوم شمال هند از 5 فوریه 2021 با هدف اولیه تعیین ایمنی واکسنهای کوید19 و هدف ثانویه ارزیابی میزان وقوع کوید19 در گروه واکسینه شده انجام میشود . گروه پرخطر متشکل از کارکنان مراقبتهای بهداشتی، دیگر کارکنان خط مقدم (پلیس، کارکنان بهداشتی و غیره)و شهروندان مسن که در ابتدا گروههای متمرکز برای توزیع واکسن در هند بودند، در این مطالعه وارد شدند. این مطالعه شامل تمام دریافت کنندگان واکسن بود که رضایت دادند و در زمان دریافت اولین یا دومین دوز واکسن کوویشر فیلد ثبتنام کردند و به صورت تلفنی پیگیری شدند.
نتایج: در میان ۱۶۵۰ دریافتکننده واکسن، ۱۵۰۰ شرکتکننده (زن / مرد: ۴۷۲ / ۱۰۲۸؛ میانگین سنی ۳۸.۸ سال)حداقل ۲ ماه پیگیری را پس از دوز دوم به پایان رساندند. بیماریهای همراه شایع در شرکت کنندگان مطالعه فشار خون بالا (۱۷۰، ۱۱.۳ %)، دیابت (۱۴۲، ۹.۵ %)، و کمکاری تیروئید (۵۴، ۳.۶ %)بودند. از کسانی که یک دوز واکسن دریافت کردند (n = ۶۵)، عفونت آزمایشگاهی SARS - CoV - ۲ در ۲۷ نفر (۴۱.۵ %)مشاهده شد و ۳ نفر مظنون بودند. از نظر شدت، عفونت در ۲۱ مورد از ۳۰ مورد (۷۰ %)خفیف، در ۵ مورد (۱۶.۷ %)متوسط و در ۲ مورد (۶.۷ %)شدید بود. از کسانی که هر دو دوز واکسن را دریافت کردند (n = ۱۴۳۵)، ۳۸۸ مورد مشکوک به عفونت SARS - CoV - ۲ تشخیص داده شدند. از این ۳۸۸ مورد، RT - PCR مثبت در ۲۷۱ نفر (۱۸.۹ %)دیده شد، ۸۲ نفر (۵.۷ %)به عنوان "مظنون" و ۳۵ نفر (۲.۴ %)به عنوان مظنونین منفی RT - PCR نامگذاری شدند. از نظر دقت، اکثر عفونتهای SCoV - ۲ "ملایم" (۳۳۱ / ۳۸۸، ۸۵.۳ %)و پس از آن "متوسط" (۳۳ / ۳۸۸، ۸.۵ %)و "شدید" (۶ / ۳۸۸، ۱.۵ %)بودند. ۴۰۴ نفر از ۱۵۰۰ پزشک شرکتکننده در این مطالعه شامل اساتید مشاور / مدرس، پزشکان مقیم و پزشکان عمومی بودند. از بین ۳۷۷ پزشکی که هر دو دوز واکسن را دریافت کردند، ۱۶۰ نفر مبتلا به عفونت SARS - CoV - ۲ تشخیص داده شدند. از این تعداد، ۱۳۱ (۳۴.۷ %)، ۱۷ (۴.۵ %)و ۱۲ (۳.۲ %)به ترتیب موارد مشکوک آزمایشگاهی، "مظنونین" و منفی RT - PCR بودند. عفونت بدون علامت، خفیف، متوسط و شدید به ترتیب در ۹ (۵.۶ %)، ۱۳۰ (۸۱.۳ %)، ۱۶ (۱۰ %)و ۵ (۳.۱ %)بود. در ۱۴۸ پزشکی که هر دو دوز را دریافت کرده بودند (۳۹.۲ %)، یا در ۱۱۹ پزشک (۳۱.۶ %)، تنها در صورتی که موارد تایید شده آزمایشگاهی در نظر گرفته میشد، عفونت در روز بیش ۱۴ پس از دریافت دوز دوم دیده میشد. چهار مورد مرگ در این مطالعه در طی دوره مطالعه، دو مورد در گروه واکسینه شده جزئی و دو مورد در گروه واکسینه شده کامل رخ دادهاست. دو نفر از این شرکت کنندگان، هر دو در گروه واکسینه شده جزئی، عفونت SARS - CoV - ۲ را در طول پیگیری خود ایجاد کرده بودند.
نتیجهگیری : شیوع نسبتا بالای عفونت SARS - CoV - 2 و کوید19 در گروههای واکسینه شده در مطالعه ما را می توان تا حدی با وجود گونههایی مانند دلتا توضیح داد که ممکن است از واکسن تولید شده محافظت ایمنی جان سالم به در برده باشند . علیرغم شیوع بالای کوید19 , مشاهده شد که شدت کوید19 کم است . از آنجا که مطالعه در حال انجام در درجه اول بر روی حوادث ناگوار پس از ایمنسازی (AEFI ها)متمرکز بود و تنها افراد واکسینه شده را ثبتنام میکرد، نتایج ثانویه فاقد گروه کنترل غیر واکسینه بودند. با این حال، نتیجه این تجزیه و تحلیل اولیه نیاز به تحقیقات قوی در مورد عملکرد واکسنها در برابر انواع، زمانبندی بهینه واکسیناسیون، نیاز به واکسینه کنندهها و همچنین زمانبندی بهینه مطالعات اثربخشی برای هدایت سیاست واکسیناسیون آینده دارد.
مقدمه
برای مقابله با بحران جاری کوید19 , برخی از کشورها به واکسنهای کوید19 اجازه استفاده اضطراری دادهاند . اینها شامل واکسنهای mRNA، واکسنهای مبتنی بر وکتور ویروس آدنو و واکسنهای غیر فعال SARS - CoV - ۲ هستند. در شرایط کنترلشده تصادفی , کارایی نزدیک به 70 % در مقابل کوید19 علامتدار برای واکسن NCoV - 19 ChAdOx1 نشانداده شدهاست که از کدگذاری آدنوویروس شامپانزه نوترکیب برای پروتئین سنبله SARS - CoV - 2 استفاده میکند . با این حال، مطالعات تایید پس از آن برای تایید اعتبار پایانهها در دنیای واقعی ضروری است. یک مطالعه مشاهدهای آیندهنگر از 5 فوریه 2021 در بیمارستانی در شمال هند در حال انجام است که هدف اولیه آن تعیین ایمنی واکسنهای کوید19 و هدف ثانویه آن ارزیابی میزان وقوع کوید19 در گروه واکسینه شده میباشد . گروه پرخطر متشکل از کارکنان مراقبتهای بهداشتی، دیگر کارکنان خط مقدم (پلیس، کارکنان بهداشتی و غیره)و شهروندان مسن که در ابتدا گروههای متمرکز برای توزیع واکسن در هند بودند، در این مطالعه وارد شدند. طبق سیاستهای دولت، COVisIELD، براساس پلتفرم ChAdOx۱ واکسن تعیین شدهبرای مرکز مطالعه در طول دوره ثبتنام مطالعه بود. این نویسندگان اخیرا یک برنامه ایمنی مطلوب COVISHIELD در زمانی که تا ۷ روز پس از دوز دوم ارزیابی شد، نشان دادند. در اینجا ما یافتههای اولیه را با توجه به معیار نتیجه ثانویه عفونت کوید19 یا SARS - CoV - 2 پس از واکسیناسیون گزارش میکنیم . دادهها براساس حداقل ۲ ماه پیگیری از زمان دوز دوم واکسن در شرکت کنندگان ثبتنامشده است که میتوانند با موفقیت از راه دور برای جزئیات تماس بگیرند.
متد
این مطالعه شامل تمام دریافت کنندگان واکسن بود که رضایت دادند و در زمان دریافت اولین یا دومین دوز واکسن COVISHIELD ثبتنام کردند. دریافت کنندگان عمدتا شامل پرسنل پزشکی و پیراپزشکی بودند چرا که آنها ذینفعان اولیه توزیع واکسن بودند. در مراحل بعدی ثبتنام، افراد مسن غیر بهداشتی که برای واکسیناسیون به مرکز مطالعه مراجعه کرده بودند نیز ثبتنام کردند. اطلاعات دموگرافیک پایه هر شرکتکننده در یک فرم گزارش موردی از پیش طراحیشده جمعآوری شد.
ثبتنام تا رسیدن به اندازه نمونه هدف (n = ۱۶۵۰)ادامه یافت.
به عنوان بخشی از مطالعه مشاهده آیندهنگر در حال انجام، هر شرکتکننده به صورت تلفنی در فواصل خاص پس از دوز دوم، برای مدتزمان کلی یک سال (مدتزمان مطالعه)تحت نظارت قرار میگیرد.
افرادی که تنها یک دوز دریافت کردهاند نیز به همین شیوه پیگیری میشوند.
برای هدف دوم , جزئیات مربوط به توسعه علائم مشابه کوید19 , مثبت بودن RT - PCR , یا مثبت بودن تست آنتیژن سریع برای SARS - CoV - 2 در هر زمان پس از واکسیناسیون جمعآوری شد .
علائم کوید19 در صورت لزوم , نیاز به بستری شدن , جزئیات مورد نیاز اکسیژن نیز جمعآوری شدند .
نتیجه
در میان ۱۶۵۰ دریافتکننده واکسن، ۱۵۰۰ شرکتکننده در این مطالعه (زن / مرد: ۴۷۲ / ۱۰۲۸)حداقل ۲ ماه پیگیری پس از دوز دوم را به پایان رساندند. ویژگیهای اساسی شرکت کنندگان در این تجزیه و تحلیل اولیه در جدول ۱ ارائه شدهاست. از میان این ۱۵۰۰ شرکتکننده، ۱۴۳۵ نفر هر دو دوز واکسن را دریافت کردند و ۶۵ نفر تنها یک دوز واکسن را دریافت کردند.
وقوع و شدت کوید19 پس از یک دوز واکسن :
از کسانی که یک دوز واکسن دریافت کردند (n = ۶۵)، عفونت آزمایشگاهی SARS - CoV - ۲ در ۲۷ نفر مشاهده شد (۴۱.۵ %). دو نفر (۳.۱ %)به عنوان "مظنون" و یک نفر (۱.۵ %)به عنوان مظنون منفی RT - PCR نامگذاری شدند. از نظر شدت، عفونت در ۲۱ مورد از ۳۰ مورد (۷۰ %)خفیف، در ۵ مورد (۱۶.۷ %)متوسط و در ۲ مورد (۶.۷ %)شدید بود. یکی از شرکت کنندگان (۳.۳ %)بدون علامت بود. سه نفر برای نیاز به اکسیژن نیاز به بستری شدن در بیمارستان (۱۰ % موارد)داشتند. دو مرگ در این گروه مشاهده شد , یکی در یک مرد مسن مبتلا به بیماری عروق کرونر از پیش موجود که به خاطر حادثه قلبی نامشخص پس از بهبودی از COVID19 مرد و دیگری در یک مرد مسن مبتلا به دیابت همراه و نارسایی احتقانی قلب که در اثر عوارض نامشخص پس از کوید19 فوت کرد . جزئیات هر دو رویداد براساس تاریخ ارائهشده توسط اعضای خانواده بود. جدول ۱
وقوع و شدت کوید19 پس از هر دو دوز واکسن :
از کسانی که هر دو دوز واکسن را دریافت کردند (n = ۱۴۳۵)، ۳۸۸ مورد مشکوک به عفونت SARS - CoV - ۲ تشخیص داده شدند. از این ۳۸۸ مورد، RT - PCR مثبت در ۲۷۱ نفر (۱۸.۹ %)دیده شد، ۸۲ نفر (۵.۷ %)به عنوان "مظنون" و ۳۵ نفر (۲.۴ %)به عنوان مظنونین منفی RT - PCR نامگذاری شدند. از نظر دقت، اکثر عفونتهای SARS - CoV - ۲ "ملایم" (۳۳۱ / ۳۸۸، ۸۵.۳ %)، و پس از آن "متوسط" (۳۳ / ۳۸۸، ۸.۵ %)و "شدید" (۶ / ۳۸۸، ۱.۵ %)بودند. عفونت در ۱۸ / ۳۸۸ (۷ / ۴ %)بدون علامت بود. عفونت در کمتر و برابر 14روز پس از دریافت دوز دوم در ۳۱ روز و پس از ۱۴ روز از دریافت دوز دوم در ۳۵۷ روز رخ داد. در صورتی که فقط موارد تایید شده آزمایشگاهی در نظر گرفته شوند، میزان آلودگی به این ویروس نزدیک به ۲۵ % (۳۵۷ / ۱۴۳۵)و ۱۷ % (۲۴۶ / ۱۴۳۵)تعیین گردید. نوزده نفر به بستری شدن نیاز داشتند (۱.۳ %)که شش نفر به دلیل مشکلات تنفسی و یا اکسیژن مورد نیاز بستری شدند (۰.۴ %). دو مرگ گزارش شدهاست. یکی از آنها یک مرد میانسال مبتلا به دیابت همراه بود که سلولیت اندام تحتانی را ایجاد کرد که منجر به سپسیس و آنسفالوپاتی شد و به دلیل نارسایی چند عضوی مرد. او دو بار برای عفونت SARS - CoV - ۲ ارزیابی شد اما منفی ارزیابی شد. مرگ دیگر یک کارمند مراقبتهای بهداشتی همراه با دیابت و فشار خون بود که از یک رویداد قلبی نامشخص مرد. جزئیات کوید19 برای این شرکتکننده را نمی توان از اعضای خانواده به دست آورد . جزئیات هر دو رویداد براساس تاریخ ارائهشده توسط اعضای خانواده بود. جدول ۱
وقوع کوید19 در پزشکان :
۴۰۴ نفر از ۱۵۰۰ پزشک شرکتکننده در این مطالعه شامل اساتید مشاور / مدرس، پزشکان مقیم و پزشکان عمومی بودند. از این تعداد، ۲۷ نفر یک دوز واکسن را دریافت کرده بودند و ۳۷۷ نفر در زمان آزمایش هر دو دوز واکسن را دریافت کرده بودند. در میان ۲۷ بیماری که تک دوز دریافت کرده بودند، عفونت RT - PCR در ۱۸ نفر (۶۶.۷ %)رخ داد و یکی از شرکت کنندگان به عنوان "مظنون" RT - PCR منفی نامگذاری شد. عفونت در یک مورد (۵.۳ %)"بدون علامت" و در ۱۹ / ۱۴ (۷۳.۷ %)"خفیف"، ۱۹ / ۳ (۱۵.۸ %)"متوسط" و ۱۹ / ۱ (۵.۳ %)"شدید" بود.
از بین ۳۷۷ پزشکی که هر دو دوز واکسن را دریافت کردند، ۱۶۰ نفر مبتلا به عفونت SARS - CoV - ۲ تشخیص داده شدند. از این تعداد، ۱۳۱ (۳۴.۷ %)، ۱۷ (۴.۵ %)و ۱۲ (۳.۲ %)به ترتیب موارد مشکوک آزمایشگاهی، "مظنونین" و منفی RT - PCR بودند. عفونت بدون علامت، خفیف، متوسط و شدید به ترتیب در ۹ (۵.۶ %)، ۱۳۰ (۸۱.۳ %)، ۱۶ (۱۰ %)و ۵ (۳.۱ %)بود. عفونت در روز ۱۴ پس از دریافت دوز دوم در ۱۴۸ پزشک (۳۹.۲ %)و یا ۱۱۹ پزشک (۳۱.۶ %)مشاهده شد. جدول ۱
بحث
مشخص شد که واکسن ChAdOx1 میزان کوید19 علامتدار را تا حدود 70 % در آزمایشهای کنترلشده تصادفی کاهش میدهد و حفاظت مشابه در برابر کوید19 علامتدار نیز در برخی از مطالعات دنیای واقعی مشاهده شدهاست .
درصد افرادی که COVID۱۹ را در محیطهای کنترلشده و دنیای واقعی پس از واکسیناسیون با واکسن ChAdOx۱ توسعه میدهند پایین بوده و از ۰.۶ تا ۱.۲ درصد متغیر است.
با این حال , ممکن است تفاوتهایی در اثربخشی واکسن و میزان موفقیت عفونت بسته به زمانی که نظارت با توجه به زمانبندی امواج کوید19 انجام میشود , وجود داشته باشد .
درصد افرادی که COVID۱۹ را در محیطهای کنترلشده و دنیای واقعی پس از واکسیناسیون با واکسن ChAdOx۱ توسعه میدهند پایین بوده و از ۰.۶ تا ۱.۲ درصد متغیر است.
با این حال , ممکن است تفاوتهایی در اثربخشی واکسن و میزان موفقیت عفونت بسته به زمانی که نظارت با توجه به زمانبندی امواج کوید19 انجام میشود , وجود داشته باشد .
در یک دوره نسبتا ساکن پس از پایین شیب یک موج، ممکن است موارد کمی وجود داشته باشد در حالی که تعداد موارد رسوخ یافته ممکن است در طول یک موج در حال پیشرفت بیشتر باشد.
ویکتور پی جی و همکاران , نزدیک به 10 درصد از وقوع کوید19 را در کارکنان مراقبتهای بهداشتی واکسینه شده از یک بیمارستان مراقبتی ثالث در جنوب هند گزارش کردند .
نرخ بستری شدن و نیاز به اکسیژن در گروه واکسینه شده به ترتیب ۰.۹ % و ۰.۰۶ % بود.
در مطالعه ما، ۴.۶ % از افرادی که یک دوز دریافت کردند و ۰.۴ % که هر دو دوز را دریافت کردند، برای نیازهای اکسیژن در بیمارستان بستری شدند.
برخی از شرکت کنندگانی که دچار هیپوکسمی شدند، درمان مبتنی بر منزل از جمله مکمل اکسیژن را ترجیح میدادند.
یک مطالعه هندی دیگر از یک بیمارستان سوم در شمال هند میزان کمی ( 2.6 % ) از وقوع کوید19 را پس از دو دوز واکسن COVisIELD گزارش کردهاست .
حتی پس از حذف موارد منفی و تست نشده RT - PCR، میزان عفونت SARS - CoV - ۲ در شرکت کنندگان به طور کامل واکسینه شده در مطالعه ما بسیار بالاتر (نزدیک به ۱۹ %)و در میان پزشکان به طور کامل واکسینه شده نزدیک به ۳۴ % بود.
این به طور نامتناسبی شیوع بالای عفونت SARS - CoV - 2 و کوید19 در گروههای پرخطر واکسینه شده در مطالعه ما را می توان تا حدی با وجود گونههایی مانند دلتا توضیح داد که ممکن است از واکسن تولید شده محافظت ایمنی جان سالم به در برده باشند . شیوع واریانت دلتا از SARSCoV - ۲ پس از اولین دوز واکسن مبتنی بر ChAdox۱ (VAXZEV)در یک خانه سالمندان در لندن گزارش شد. اخیرا کاهش حفاظت در برابر واریانت دلتا در مقایسه با واریانت آلفا برای واکسن NCoV - ۱۹ ChAdOx۱ نشانداده شدهاست. [ سایر توضیحات بالقوه برای اختلاف در میزان وقوع عفونت SARS - CoV - ۲ بین مطالعات مختلف هندی میتواند مربوط به طرحهای مطالعه و تغییرات منطقهای باشد. مطالعه انجامشده توسط رانا و همکاران به حداقل دوره پیگیری ۲ هفته پس از دوز دوم و همچنین میانه زمان رسیدن به موفقیت پس از دوز دوم (۲۹.۵ روز)اشاره میکند اما به کل مدتزمان پیگیری اشاره نمیکند. احتمال عفونتهایی که در سایر کارکنان مراقبتهای بهداشتی با ایمنی رو به کاهش با گذشت زمان رخ میدهند، از این رو نمی توان آنها را رد کرد. مطالعه هند جنوبی که میزان نسبتا بالاتری از عفونت را گزارش کرد همزمان با مطالعه ما و اوج موج دوم در هند بود. با این حال، تغییرات منطقهای بین ایالتهای مختلف ممکن است تفاوت در نرخهای موفقیت را توضیح دهد. علاوه بر این، ممکن است تفاوتی در انواع غالب SARS - CoV - ۲ بین دو بیمارستان وجود داشته باشد. ما به پیگیری تمام شرکت کنندگان موجود ادامه میدهیم و بر این باوریم که نتایج آینده نمایش دقیق تری از وقوع کوید19 را فراهم میکند .
علیرغم میزان بالای بروز عفونتهای SARS - CoV - 2 در افراد واکسینه شده , مشاهده شد که شدت کوید19 پایین است . ۴۱ % افرادی که تنها یک دوز واکسن را دریافت کردند و ۱۹ % آنهایی که هر دو دوز را دریافت کردند عفونت ناشی از SARS - CoV - ۲ را ایجاد کردند. وقوع کوید19 " شدید " 7 / 7 برابر کمتر ( 4 / 0 % ) در شرکت کنندگان واکسینه شده کامل در مقایسه با گروه واکسینه شده جزئی ( 1 / 3 % ) بود . این میزان ممکن است رابطه پاسخ دوز واکسن در کاهش عفونت و همچنین شدت بیماری را تحتتاثیر قرار دهد. از چهار مرگ مشاهدهشده , یکی احتمالا مربوط به کوید19 بود و در یک بیمار مسن که تا حدی واکسینه شده بود رخ داد . هیچ تلفاتی به دلیل کوید19 در افراد واکسینه شده کامل مشاهده نشد .
از آنجا که مطالعه در حال انجام در درجه اول بر روی حوادث ناگوار پس از ایمنسازی (AEFI ها)متمرکز بود و تنها افراد واکسینه شده را ثبتنام میکرد، نتایج ثانویه فاقد کنترل گروه واکسینه نشده بودند. از این رو، نویسندگان نمیتوانند در مورد موثر بودن واکسن علیه عفونت، بستری شدن و مرگ اظهار نظر کنند. یک مطالعه جداگانه برای تجزیه و تحلیل نتایج در کارکنان بهداشتی واکسینه نشده و واکسینه نشده و کارکنان کمکی بیمارستان آغاز شدهاست.
پایان
موج دوم پاندمی کوید19 در ماههای آوریل و مه به بخشهای بزرگی از هند رسید . یافتههای مطالعه حاضر نشان میدهد که حفاظت دنیای واقعی توسط واکسن ChAdOx۱ علیه COVID - ۱۹ نشانهای ممکن است به اندازه آنچه که در شرایط کارآزمایی بالینی یا حتی در شرایط دنیای واقعی وقتی که موج فروکش کردهاست، مشاهده شدهاست، زیاد نباشد. تفاوتها ممکن است بسته به انواع غالب نیز وجود داشته باشند. اگر چه میزان عفونت در افراد واکسینه شده بیش از 20 برابر بیشتر از میزان مشاهدهشده در محیطهای کنترلشده تصادفی بود , کوید19 شدید تنها در 0.4 % افراد واکسینه شده کامل رخ داد . تجزیه و تحلیل دقیق علت مرگ در چهار مورد مرگ به دلیل ماهیت مشاهدهای مطالعه امکان پذیر نیست. نتیجه این تجزیه و تحلیل اولیه نیاز به تحقیقات قوی در مورد عملکرد واکسنها در برابر انواع، زمانبندی بهینه واکسیناسیون، نیاز به واکسینه کنندهها و همچنین زمانبندی بهینه مطالعات اثربخشی برای هدایت سیاست واکسیناسیون آینده دارد.
برچسب های مهم
چکیده
اهداف : حصول اطمینان از درک بالای واکسن کوید19 در میان ارائه دهندگان مراقبت از کودکان در کاهش پیامدهای سلامت عمومی انتقال کودک به پرسنل و پرسنل به کودک SARS - CoV - 2 حیاتی است ; با این حال , میزان واکسیناسیون در میان این گروه نامشخص است .
روشها: برای مشخص کردن درک واکسن در میان ارائه دهندگان مراقبت از کودکان، ما یک بررسی مقطعی از نیروی کار مراقبت از کودکان انجام دادیم. عرضهکنندگان از طریق پایگاههای داده ملی مختلف و دفاتر ثبت دولتی شناسایی شدند. یک لینک به نظرسنجی از طریق ایمیل بین ۲۶ می و ۲۳ ژوئن ۲۰۲۱ فرستاده شد. از ۴۴،۷۷۱ پاسخدهنده بالقوه، ۲۱،۶۶۳ نفر (۴۸.۴ درصد)پاسخ دادند.
نتایج : درک کلی واکسن کوید19 در میان ارائه دهندگان مراقبت از کودکان ایالاتمتحده ( 78.1 % , ) بالاتر از جمعیت بزرگسال ایالاتمتحده ( 65 % ) بود . نرخ واکسیناسیون از ۵۳.۵ % تا ۸۹.۴ % بین ایالتها متغیر بود. درک واکسن به طور قابلتوجهی براساس سن پاسخ دهندگان (۷۰.۰ % برای سنین ۲۵ - ۳۴، ۹۱.۵ % برای سنین ۷۵ - ۸۴)، نژاد (۷۰.۰ % برای آمریکاییهای سیاهپوست یا آفریقایی، ۹۲.۵ % برای آسیایی - آمریکاییها)، درآمد سالانه خانواده و تنظیم مراقبت از کودکان (۷۲.۹ % برای خانه - محور، ۷۹.۷ % برای مرکز - محور)متفاوت بود.
نتیجهگیری : دریافت واکسن کوید19 در میان ارائه دهندگان مراقبت از کودکان ایالاتمتحده بیشتر از جمعیت عمومی بزرگسالان ایالاتمتحده بود . کسانی که جوانتر، با درآمد پایینتر بودند، سیاه یا آفریقایی آمریکایی، در ایالتهای کوهستانی غرب یا جنوب ساکن بودند، و / یا در برنامههای مراقبت از کودکان در خانه کار میکردند، کمترین میزان واکسیناسیون را گزارش میکردند؛ رهبران بهداشت عمومی و نمایندگان مجلس باید این زیر گروهها را برای قرار دادن در دستور کار سیاست گذاری جهت دستیابی به بیشترین بهره در جذب واکسن در میان ارائه دهندگان، اولویتبندی نمایند.
مقدمه
ترویج بیماری کرونا ویروس - 2019 ( کوید19 ) دریافت واکسن در میان ارائه دهندگان مراقبت از کودکان یک گام حیاتی در بازگرداندن ایالاتمتحده به عملکرد پیش از پاندمی است . ارائه دهندگان خدمات مراقبت از کودکان، که به تازگی به عنوان "نیروی کار پشت سر هم" معرفی شدهاند، خدمات ضروری را برای والدینی فراهم میکنند که به دنبال ورود دوباره به بازار کار ایالاتمتحده هستند. شواهد این امر را می توان در بررسی ملی انجامشده توسط وزارت آموزش و پرورش یافت که تخمین زده بود تقریبا ۹۰ درصد از والدین در خانوادههای با درآمد دوگانه، قبل از شیوع بیماری همهگیر، به برخی از انواع مراقبت از کودکان متکی بودند. علاوه بر این، پس از این بیماری همهگیر، عدم دسترسی به خدمات مراقبت از کودکان و تعطیلی مدارس از جمله دلایل اصلی جلوگیری از بازگشت والدین به نیروی کار بودهاست. علاوه بر انگیزه اقتصادی، با توجه به پیامدهای بالقوه انتقال دو طرفه SARS - CoV - ۲ بین کارکنان و کودکان، یک ضرورت سلامت عمومی برای محافظت از ارائه دهندگان مراقبت از کودکان از طریق واکسیناسیون وجود دارد. انتقال کارکنان به کودکان ممکن است منجر به کوید19 در میان کودکان شود که بسیاری از آنها یا بدون علامت هستند و یا نسبت به بزرگسالان دارای علائم پوسی هستند و ممکن است ناخواسته این عفونت را به تماسهای خانگی منتقل کنند . تماسهای خانوادگی ممکن است شامل والدین و پدربزرگها و مادربزرگها باشد، که بسیاری از آنها مسن هستند و / یا شرایط پزشکی اساسی دارند، که آنها را در معرض خطر بالاتری برای بیماریهای مرتبط با COVID۱۹ و مرگ و میر قرار میدهد. در حالی که ریسک پایین است , ممکن است انتقال کودک به کارمند SARSCoV - 2 منجر به کوید19 در میان ارائه دهندگان مراقبت از کودکان شود , که تعداد زیادی از آنها اعضای گروههای اقلیت نژادی و قومی هستند که در معرض خطر بالاتری برای عوارض مرتبط با کوید19 قرار دارند . بنابراین، تضمین جذب بالای واکسن در میان ارائه دهندگان مراقبت از کودکان، فراتر از مساله فوری سلامت شخصی رفته و به عنوان مکانیسمی برای بهبود اقتصادی، سلامت عمومی، و عدالت در سلامت به کار میرود.
علیرغم اهمیت کسب اطمینان از جذب بالای واکسن در میان ارائه دهندگان مراقبت از کودکان، اطلاعات کمی در مورد وضعیت واکسیناسیون فعلی این گروه وجود دارد. برای توصیف بهتر وضعیت فعلی جذب واکسن در میان ارائه دهندگان مراقبت از کودکان، ما یک بررسی مقطعی در مقیاس بزرگ از نیروی کار مراقبت از کودکان ایالاتمتحده انجام دادیم.
متد
مدیریت نظرسنجی
نتیجه
در مجموع ۲۱،۶۶۳ نفر از ۴۴،۷۷۱ نفری که این نظرسنجی به آنها فرستاده شد، این نظرسنجی را به پایان رساندند که نرخ پاسخ ۴۸.۴ % بود. از این تعداد، ۲۰،۰۱۳ (۴۴.۷ درصد از کسانی که نظرسنجی را ارسال کردیم)پاسخ دهندگان معیارهای واجد شرایط ورود را داشتند. دریافت کلی واکسن در میان تمام پاسخ دهندگان واجد شرایط ۷۸.۲ % بود (۷۷.۷ % بدون وزن)، و دریافت واکسن در میان کسانی که هنوز به عنوان ارائه دهندگان مراقبت از کودکان کار میکنند در زمان تکمیل نظرسنجی (۹۲ % پاسخ دهندگان)۷۸.۴ % در مقابل ۷۵.۸ % برای کسانی بود که در حال حاضر در مراقبت از کودکان کار نمیکنند (۲ = ۲.۸۶؛ p = ۰.۰۹). بیشتر پاسخ دهندگان گزارش دادند که یا فایزر - BioNTch ( 50.5 % ) و یا مودرنا 42.1 % ) دریافت کردهاند و نسبت کمتری گزارش دادند که در آن جانسون ( 6.9 % ) و یا واکسن دیگر ( 0.6 % ) را دریافت کردهاند . رایجترین ماه برای دریافت دوز اول ماه مارس ۲۰۲۱ (۳۳.۱ %)بود که نسبت آن پس از مارس ۲۰۲۱ به شدت کاهش یافت.
دریافت واکسن با استفاده از آمار جمعیتی
همانطور که در جدول ۱ نشانداده شدهاست، دریافت واکسن در میان پاسخ دهندگان مسنتر بیشتر بود: میزان واکسیناسیون کسانی که بین ۲۵ تا ۳۴ سال سن داشتند ۷۰.۰ % بود در حالی که میزان واکسیناسیون کسانی که بین ۷۵ تا ۸۴ سال سن داشتند ۹۱.۵ % بود (۲ = ۳۱.۵۹؛ p.
دریافت واکسن در میان ارائه دهندگان آمریکایی سیاهپوست یا آفریقایی به میزان ۰ / ۷۰ % کمتر و در میان آسیایی آمریکاییها به میزان ۵ / ۹۲ % بیشتر بود.
سطح درآمد خانوار با افزایش جذب واکسن همراه بود به طوری که افراد با درآمد سالانه ۳۵۰۰۰ دلار، ۷۰.۷ درصد و افراد با درآمد سالانه ۷۵،۰۰۰ دلار، ۸۵ درصد واکسن دریافت میکردند.
سابقه کوید19 با جذب کمتر واکسن در 70.5 % در مقابل 79.6 % در افرادی که سابقه کوید19 نداشتند , همراه بود .
دریافت واکسن با تنظیم مراقبت از کودکان
دریافت واکسن در میان ارائه دهندگان مراقبت از کودکان در مرکز نسبت به ارائه دهندگان مراقبت از کودکان در منزل با نرخ واکسیناسیون به ترتیب ۷۹.۷ % و ۷۲.۹ % بیشتر بود (۲ = ۵۰.۹۲؛ p < ۰.۰۱). قابلذکر است که ارائه دهندگان اقلیت نژادی، نسبت بالاتری از تنظیمات مراقبت از کودکان در خانه را نسبت به تنظیمات مراقبت از کودکان در مرکز تشکیل میدهند. در میان انواع مختلف برنامههای مراقبت از کودکان مبتنی بر مرکز، دریافت واکسن به شرح زیر بود: برای مراکز سود - ۷۸.۵ %، مراکز سازمانهای غیر انتفاعی - ۸۴.۱ %، مراکز مدرسه - ۸۱.۱ %، مراکز شروع سرپرست یا شروع زود هنگام (مراکز مراقبت از کودکان با بودجه فدرال)- ۷۲.۹ %، مراقبت از کودکان با هزینه کم (کودکان هر روز تغییر میکنند)- ۶۳.۴ %، برنامههای مراقبت از کودکان با هزینه کم - ۷۹.۶ % و سایر مراکز - ۸۲.۵ %.
دلایل عدم واکسیناسیون
در میان کسانی که واکسینه نشده بودند، تنها ۵ % "کاملا مطمئن" بودند که در آینده واکسینه خواهند شد، ۶.۹ % "بسیار محتمل"، ۲۸.۲ % "تا حدی محتمل" و ۵۹.۲ % "غیر محتمل" بودند (۰.۴ % پاسخ ندادند). در میان کسانی که گزارش دادند در آینده تنها "تا حدودی محتمل" یا "غیر محتمل" واکسینه خواهند شد، شایعترین دلایل عدم واکسیناسیون عبارتند از نگرانی در مورد ایمنی واکسن (۷۹.۹ %)، نگرانی در مورد سرعت توسعه واکسن (۶۶.۸ %)و عدم اعتماد به فرآیند توسعه واکسن (۳۲.۰ %). شایعترین موانع ساختاری واکسیناسیون عبارتند از ناتوانی در مرخصی از کار (۵.۴ %)، مشغله بیش از حد برای واکسیناسیون (۳.۵ %)، و مشکل در برنامهریزی تاریخ قرار دادن واکسن (۲.۷ %). لیست کاملی از دلایل گزارش شدهبرای عدم واکسیناسیون در میان پاسخ دهندگان را می توان در شکل ۲ یافت.
بحث
دریافت کلی واکسن در میان ارائه دهندگان مراقبت از کودکان ایالاتمتحده (۷۸.۲ % (۹۵ % CI: ۷۷.۳ تا ۷۸.۹))به طور قابلتوجهی بیشتر از جمعیت عمومی بزرگسالان ایالاتمتحده (۶۵ %)در زمان بررسی بود. قابلذکر است که میزان واکسیناسیون در میان ارائه دهندگان مراقبت از کودکان که به طور فعال در صنعت مراقبت از کودکان کار میکنند (۹۲ % پاسخ دهندگان)در زمان بررسی حتی بالاتر بود (۷۸.۴ %). از کسانی که هنوز واکسن کوید19 را دریافت نکرده اند , 11.9 % دیگر گفتند که آنها " کاملا مطمئن " ( 5 % ) یا " بسیار محتمل " ( 6.9 % ) برای واکسینه شدن در آینده هستند , که نشان میدهد دریافت نهایی واکسن در میان ارائه دهندگان مراقبت از کودکان ممکن است حدود 90 % باشد . نتایج ما مشابه نتایجی است که در گزارش رسانهای ۶ آوریل ۲۰۲۱ که توسط مرکز کنترل و پیشگیری از بیماریها براساس دادههای منتشر نشده منتشر شد، بیان شد. علاوه بر این، مطالعه ما تفکیک دقیقی از دریافت واکسن در میان ارائه دهندگان مراقبت از کودکان براساس ویژگیهای جمعیت شناختی، موقعیت و محیط مراقبت از کودکان فراهم میکند.
افزایش دریافت واکسن در میان ارائه دهندگان مراقبت از کودکان نسبت به جمعیت عمومی ممکن است با افزایش برجستگی بیماری در میان این گروه مربوط به کوید19 توضیح داده شود . به عنوان مثال، بخش های congregate (به عنوان مثال، مدارس، برنامههای مراقبت از کودکان، خانههای سالمندان، زندانها)بدون اقدامات مناسب کاهش عفونت، ناقل های شناختهشده برای انتقال جامعه هستند. همچنین، کودکان خردسال واجد شرایط مداخلات دارویی مانند واکسیناسیون در زمان جمعآوری اطلاعات نبودند و ممکن است قادر به پیروی موثر از مداخلات رفتاری غیر دارویی نباشند. این امر به ویژه به ارائه دهندگان مراقبت از کودکان مربوط است که بر خلاف معلمان K - ۱۲، از کودکان زیر پنج سال مراقبت میکنند. ارائه دهندگان مراقبت از کودکان نیز ممکن است احساس کنند که این وظیفه آنها است که از کودکان واکسینه نشده در حال حاضر مراقبت کنند. علاوه بر این، در حالی که در حال حاضر هیچ کشوری نیاز به واکسینه کردن ارائه دهندگان مراقبت از کودکان ندارد، برخی موسسات مراقبت از کودکان ممکن است به واکسیناسیون به عنوان شرایط استخدام نیاز داشته باشند.
در حالی که دریافت کلی واکسن در میان ارائه دهندگان مراقبت از کودکان ایالاتمتحده به طور قابلتوجهی بیشتر از جمعیت عمومی بزرگسالان ایالاتمتحده بود، الگوی تفاوتهای نسبی در میزان واکسیناسیون از نظر جمعیت شناختی، وضعیت ارائه مراقبت و دلایل عدم واکسیناسیون مشابه بود. آنهایی که جوانتر بودند، درآمد کمتری داشتند و / یا سیاه یا آفریقایی - آمریکایی کمترین میزان واکسیناسیون را گزارش کردند. در مقابل، افراد مسن، درآمد بالاتر و آسیایی - آمریکایی بیشترین میزان واکسیناسیون را گزارش کردند (یک مورد استثنا، ارایه دهندگان مراقبت از کودکان بین سنین ۱۸ تا ۲۴ سال بودند که دریافت واکسن بالاتری را نسبت به گروه سنی ۲۵ تا ۳۴ سال گزارش کردند، شاید به این دلیل که برخی موسسات آموزش عالی آن را به عنوان شرط ورود به دانشگاه الزامی میدانستند). دریافت واکسن در کوهستان غرب و جنوب و بیشترین آن در نیوانگلند و اقیانوس آرام غرب مشاهده شد. رایجترین دلایل عدم واکسیناسیون به جای مسائل ساختاری مربوط به عدم دسترسی به واکسن، مربوط به تردید در استفاده از واکسن بود. از جمله این دلایل می توان به نگرانی در مورد ایمنی واکسن، عدم اعتماد به فرآیند تولید واکسن و یا عدم اعتماد به دولت اشاره کرد.
در نهایت , جذب واکسن کوید19 در میان بخش های مختلف مراقبت از کودکان متفاوت بود . ارائه دهندگان مراقبت از کودکان در مرکز نسبت به ارائه دهندگان مراقبت از کودکان در منزل، میزان واکسیناسیون بالاتری را گزارش کردند (به ترتیب ۷ / ۷۹ % و ۹ / ۷۲ %). یکی از دلایل این امر ممکن است این باشد که ارائه دهندگان کودک در منزل نسبت به ارائه دهندگان مراقبت از کودکان در مرکز، نسبت به سیاه پوستان یا آفریقایی - آمریکایی، بومیان آمریکا و / یا اسپانیولیها (هر چند که مورد اخیر قابلتوجه نبود)، انحراف بیشتری دارند. مشخص شدهاست که گروههای اقلیت نسبت به سفید پوستان غیر اسپانیایی دریافت واکسن کمتری دارند. [ XVIII ] ملاحظه دیگری که میتواند این تفاوت را توجیه کند، ممکن است افزایش برجستگی بیماری در میان ارائه دهندگان مراقبت از کودکان مبتنی بر مرکز در خانه باشد که ناشی از تغییر در اندازه گروه و پتانسیل این است که برخی از کارفرمایان مراقبت از کودکان ممکن است نیاز به واکسیناسیون ارائه دهندگان مراقبت به عنوان شرایطی برای بازگشت به کار داشته باشند. هم اندازه گروه و هم نسبت کودک به کارمند در میان تنظیمات مراقبت از کودکان به شدت تنظیم شدهاند، و تنظیمات مراقبت از کودکان در خانه دارای محدودیت کمتری در اندازه گروه نسبت به بخش های مراقبت از کودکان در مرکز هستند.
نتیجه گیری
مشخص شد که دریافت واکسن کوید19 در میان ارائه دهندگان مراقبت از کودکان ایالاتمتحده بیشتر از جمعیت عمومی بزرگسالان ایالاتمتحده است . کمترین میزان واکسیناسیون در میان ارائه دهندگان مراقبت از کودکان گزارش شد که جوانتر، با درآمد پایینتر، سیاه یا آفریقایی - آمریکایی بودند، در ایالتهای کوهستانی غرب یا جنوب زندگی میکردند، و / یا در مراکز مراقبت از کودکان خانگی کار میکردند. رهبران بهداشت عمومی و قانونگذاران باید این زیرگروهها را برای دسترسی و قرار دادن در دستور کار سیاست اولویتبندی کنند تا به بزرگترین دستاوردهای ممکن در جذب واکسن در میان ارائه دهندگان مراقبت از کودکان دست یابند. تلاشها برای ارتقای جذب واکسن کوید19 در میان ارائه دهندگان مراقبت از کودکان با در نظر گرفتن ظهور متغیر دلتا قابل انتقال اهمیت بیشتری پیدا کرد , که در جولای 2021 به لکه غالب SARS - CoV - 2 در ایالاتمتحده تبدیل شد .
کودکان زیر 12 سال فاقد شرایط لازم برای واکسیناسیون کوید19 باقی میمانند و به این ترتیب , عامل محدود کننده در تضمین عرضه مناسب خدمات مراقبت از کودکان مشروط به حفاظت از سلامت شخصی ارائه دهندگان مراقبت از کودکان خواهد بود .
COVID-19 Vaccine Uptake among U.S. Child Care Providers
برچسب های مهم

مقدمه
تحت سومین وضعیت اضطراری در ژاپن، رستورانها و بارها در توکیو از نوشیدن الکل منع شدند. اگر چه شواهد غیر مستقیم نشان میدهد که عفونت در رستورانها و بارها ممکن است شایع باشد [ ۱ ]، شواهد مستقیم، به خصوص برای ژاپن، ضعیف باقی میماند. بنابراین، سیاستهای ممنوعیت الکل نیاز به شواهد قوی تری برای نشان دادن اثربخشی آنها دارد.
تحت این شرایط، برخی از محققان گزارش دادند که شیوع عفونت در میان افرادی که برای خوردن شام و نوشیدن الکل با بیش از دو شرکتکننده با هم ملاقات کرده بودند، بیش از دو برابر افرادی بود که این کار را با بیش از دو شرکتکننده یا حتی یکبار در طول دو هفته گذشته انجام نداده بودند [ ۲ ]. با این حال، از آنجا که این یافتهها شامل هیچ اثر جداگانهای از مصرف الکل نبود، فراوانی و تعداد شرکت کنندگان در گروه شام خوردن، نوشیدن الکل را به عنوان خطر بالا نشان ندادند.
بنابراین، آنها به دلیل بروز صفر، مصرف الکل و شام در گروه را تجزیه و تحلیل نکردند. با این حال، با توجه به مقیاس و فراوانی یکسان غذا خوردن، آنها دریافتند که شیوع عفونت در افرادی که با بیش از دو شرکتکننده شام خورده بودند، در حالی که الکل را بیش از دو برابر افرادی که بدون الکل شام میخوردند، مصرف میکردند. برای مقایسه در حال حاضر , تعداد شرکت کنندگان و فراوانی آنها یکسان بود , اما برخی تفاوتها ممکن است به نوشیدن الکل نسبت داده شود : 7 نفر کوید19 مثبت با نوشیدن الکل , 12 نفر با نوشیدن الکل منفی و 8 نفر بدون نوشیدن الکل منفی بودند . کسی پیدا نشد که بدون مشروب خوردن، مثبت باشد.
از آنجا که میزان بروز در افراد بدون مصرف الکل صفر بود، هیچ مطالعه مورد - شاهدی انجام نشد. با این وجود، این یافته شامل اطلاعاتی در مورد خطرات آشامیدنی است. بنابراین، ما رویکرد دیگری را برای ارزیابی این اطلاعات به کار بردیم.
متد
برای مطالعه قبلی [ 2 ] , تحقیقی در طول 30 مارس تا 8 ژوئن برای بیماران مبتلا به تب انجام شد که برای عفونت کوید19 در دو بیمارستان در توکیو تست PCR شده بودند . از ۴۰۷ بیماری که وارد مطالعه شدهبودند، تنها ۲۷ نفر در طول دو هفته گذشته با بیش از دو نفر شام خورده بودند.
ما یک روش بوت استرپینگ غیر پارامتری با تکرار کامل را براساس یک توزیع تجربی [ ۳، ۴، ۵ ] برای توزیع { xi (i = ۱، ۲، ۳، ۴)} بررسی کردیم که نشاندهنده تعداد افرادی است که تست مثبت یا منفی برای عفونت و با یا بدون نوشیدن الکل داشتهاند. علاوه بر بوت استرپینگ معمول، ما از روشی با ملاحظه ویژه برای حالت xi = ۰ استفاده کردیم. برای توزیع و بدست آوردن { xi + ۱ } b - ۱ (i = ۱، ۲، ۳، ۴){ xi + ۱ } b - ۱ (i = ۱، ۲، ۳، ۴)، که در آن بالانویس b یک سری خود راهاندازی شده را نشان میدهد، خود راهاندازی کردیم.
براساس توزیع خودراهاندازی شده j ام { xib (i = ۱، ۲، ۳، ۴)} j، می توان نسبت ریسک R، j * را به دست آورد، که نشاندهنده ریسک نسبی ناشی از نوشیدن است. ما این روند را یک میلیون بار تکرار کردیم، در نتیجه یک میلیون R، j * به دست آوردیم. ما این متغیرها را مرتب کردیم. انتظار میرود مدتزمان از Ri، ۵۰۰ * تا Ri، ۹۹۵۰۰ * ۹۹ % CI از R * باشد.
علاوه بر این تحلیلها، ما کنترل وضعیت شیوع پسزمینه را نیز انجام دادیم. اگر یک گروه به دوره شیوع بالا محدود میشد، خطر عفونت احتمالا بیشتر از گروه دیگر بود، بدون توجه به نوشیدن. بنابراین، اگر دوره زمانی که یک گروه مشاهدهشده متعادل نبود، وضعیت پسزمینه باید تنظیم شود.
برای این دوره مطالعه، حالت سوم اضطراری از ۲۵ آوریل تا ۲۰ ژوئن ۲۰۲۱ اعلام شد. برای این اقدام متقابل، نوشیدن الکل در رستورانها و بارها ممنوع شد. از ۲۱ ژوئن، نوشیدن الکل در رستورانها یا بارها به تنهایی یا با یک فرد دیگر مجاز بود، اما برگزاری جلسات با بیش از دو شرکتکننده همچنان ممنوع بود. بنابراین، فرض بر این است که یک گروه غذاخوری یا نوشیدنی شامل بیش از دو شرکتکننده که بیش از دو بار در طول دو هفته گذشته جلسه داشتهاند، قبل از حالت اضطراری سوم ملاقات کردهاند. در مقابل، گروه غیر آشامیدنی میتواند در هر زمانی در طول دوره ملاقات کند. بنابراین، شرایط پسزمینه شیوع ممکن است متفاوت باشد. ما نتایج را طوری تنظیم کردیم که شیوع عفونت در گروه نوشیدن به وسیله تفاوت در شیوع بین قبل از وضعیت اضطراری و کل دوره مطالعه تقسیم شد. ما ۱ % را به عنوان سطح اهمیت انتخاب کردیم.
نتیجه
R، j * مرتب شده در شکل ۱ نشانداده شدهاست. شیوع مصرف الکل صفر بود. نسبت خطر در این مورد بینهایت بود. با این حال، R، ۱ * به وضوح کمتر از یک بود، که نشان میدهد احتمال اینکه گروهی که با نوشیدن غذا میخورند نسبت به گروهی که بدون نوشیدن غذا میخورند، ریسک کمتری دارند. در واقع، احتمال آن ۲.۲۵ % برآورد شدهاست. از آنجا که این احتمال بیش از نیمی از سطح معنیداری ۰.۵ % است، فرضیه صفر، که شیوع عفونت دو نوع ملاقات متفاوت نبود، نمیتواند رد شود.
بحث
اگرچه ما به این نتیجه رسیدیم که فرضیه صفر را نمی توان رد کرد، اگر همانند بسیاری از مطالعات همه گیرشناسی، ۵ % را به عنوان سطح معناداری در نظر بگیریم، آنگاه میتوانیم فرضیه صفر را رد کنیم زیرا نسبت ریسک بزرگتر از ۵ / ۲ % است. به عبارت دیگر، نتیجه این مطالعه ممکن است به شدت تحتتاثیر سطح اهمیت اتخاذ شده قرار گیرد. حداقل میتوان گفت که خطرات زیاد ناشی از نوشیدن ممکن است با شواهد قوی قابل تحمل نباشند. سطح اهمیت مورد استفاده برای نتیجهگیری به طور کامل توسط سطح قابلقبول خطای محققان تعیین میشود. بنابراین، نتایج باید با دقت بیشتری ارزیابی شوند.
مطالعه حاضر محدودیتهایی دارد. اول، سن، جنسیت و عوامل دیگری که ممکن است بر رفتار تاثیر بگذارند را نمی توان کنترل کرد زیرا ما هیچ اطلاعاتی غیر از آنچه که برای تجزیه و تحلیل منتشر شده و مورد استفاده قرار گرفتهاست، نداریم، اگرچه مطالعه قبلی [ ۲ ] شامل کنترل آنها بود. رفتارهای نوشیدن ممکن است با توجه به سن و جنسیت تحتتاثیر قرار گیرند. این گرایشها ممکن است با بروز عفونت کوید19 مرتبط باشند . اگر چنین باشد، مشروب خوردن ممکن است خطر عفونت نداشته باشد.
دوم، دادههای اصلی مورد استفاده برای مطالعه قبلی [ ۲ ] ممکن است شامل اطلاعاتی برای آزمایش خطر شام خوردن گروهی با بیش از دو شرکتکننده در دو هفته گذشته در مقایسه با عدم شام خوردن گروهی باشد. از طرف دیگر، ممکن است خطر شام خوردن گروهی با بیش از دو شرکتکننده در دو هفته گذشته در مقایسه با شام خوردن گروهی با یک شرکتکننده در دو هفته گذشته را آزمایش کند. این تحلیلها ممکن است به ارزیابی خطرات ناشی از فراوانی و تعداد شرکت کنندگان به غیر از آنهایی که توسط نوشیدن مطرح شدهاند کمک کند. ما هیچ داده اصلی نداریم. سوم، سویه واریانت N۵۰۱Y در طول دوره مطالعه، به ویژه در طول نیمه آخر دوره شایع بود. شیوع آن ممکن است بر نتایج افزایش خطرات غیر آشامیدنی تاثیر بگذارد.
پایان
نتایج این مطالعه نشان داد که هیچ مدرک روشنی برای روشن کردن خطرات نوشیدن وجود ندارد. با این حال، انتظار میرود که تحلیلهای بیشتر شامل جمعآوری دادهها ضروری باشند. سیاستهای مورد نیاز برای محدود کردن آزادیهایی مانند محدودیت علیه خروج یا ممنوعیت نوشیدن باید براساس شواهد قوی برای کاهش موثر عفونت باشد. علاوه بر این، خطرات ناشی از فراوانی و تعداد شرکت کنندگان در طول شام گروهی و نوشیدن الکل باید مورد ارزیابی قرار گیرد.
مطالعه حاضر براساس نظرات نویسندگان است: این مطالعه هیچ موضع یا سیاستی از نهادهای وابسته حرفهای آنها را منعکس نمیکند.

برچسب های مهم
چکیده : گزینههای درمانی برای کوید19 , بیماری ناشی از عفونت ویروس تنفسی حاد و شدید کورنوویروس 2 ( SARS - CoV - 2 ) , در حال حاضر به شدت محدود هستند . بنابراین , داروهای ضد ویروسی که به طور موثر تکثیر SARS - CoV - 2 را کاهش میدهند یا علائم کوید19 را کاهش میدهند , به شدت مورد نیاز هستند . در حال حاضر گلوکوکورتیکوئیدهای استنشاقی در زمینه درمان کوید19 مورد بحث قرار میگیرند , که تا حدودی براساس مطالعه قبلی است که کاهش زمان ریکاوری را در موارد کوید19 ملایم پس از تجویز استنشاقی گلوکوکورتیکوئیدها گزارش کردهاست . با توجه به گزارشهای مختلف که فعالیت بالقوه ضد ویروسی گلوکوکورتیکوئیدها در برابر ویروسهای تنفسی را توصیف میکنند، ما هدف تجزیه و تحلیل فعالیت بالقوه ضد ویروسی budesonide برابر SARS - CoV - ۲ و انواع در گردش نگرانی (VOC)B.۱.۱.۷ (آلفا)و B.۱.(بتا) را انجام دادیم ما مهار وابسته به دوز SARS - CoV - ۲ را نشان میدهیم که بین تمام انواع ویروسی تست شده قابلمقایسه بود در حالی که زیست پذیری سلول تحتتاثیر قرار نگرفته باقی میماند. نتایج ما دلگرمکننده هستند زیرا میتوانند حالت چند وجهی عمل budesonide برابر SARS - CoV - 2 و کوید19 را نشان دهند که میتواند به بهبود عملکرد بالینی کمک کند .
کلمات کلیدی: SARS - CoV - ۲؛ ضد ویروس؛
budesonide.
انواع نگران کننده؛
کورتیکواستروئید (انواع هورمونها که توسط غدد فوق کلیوی ترشح میشود)
۱. مقدمه
سندروم شدید تنفسی حاد کورنوویروس 2 ( SARS - CoV - 2 ) در دسامبر 2019 در چین ظهور کرد [ 1 ] و با سرعتی فوقالعاده به گسترش جهانی خود ادامه داد که نیاز به یک تلاش علمی و دارویی بیسابقه برای توسعه گزینههای درمانی جدید و ارزیابی مجدد درمانهای موجود برای مبارزه با بیماری مرتبط با آن کوید19دارد , . از 21 آوریل 2020 , موسسه ملی بهداشت ( NIH ) درمان با باملانی وی ماب bamlanivimab به علاوه اته سه ویماب etesevimab[ 2 ] یا کاسی ری وی ماب casirivimab به علاوه ایمده وی ماب imdevimab را توصیه میکند و داروی ضد ویروسی تایید شده FDA یعنی رمدسیویر را به ترتیب برای بیماران سرپایی با علائم خفیف تا متوسط کوید19 و برای بیمارانی که به اکسیژن مکمل نیاز دارند , تایید میکند . با این حال، به دلیل عدم قطعیت در مورد مزایای بالینی در بیماران شدید که به اکسیژن با جریان بالا، تهویه مکانیکی غیر تهاجمی یا تهاجمی نیاز دارند، remdesivir به طور معمول برای درمان در این بیماران توصیه نمیشود [ ۴، ۵ ]. ظاهرا، توسعه داروهای موثر برای درمان، به ویژه برای افرادی که از علائم شدید عفونت SARSCoV - ۲ رنج میبرند، روز به روز فوریت بیشتری پیدا میکند. علاوه بر این، ظهور جهانی انواع جدید نگران کننده (VOC)، از جمله نوع B.۱.۱.۷ (آلفا)و نوع B.۱.۳۵۱ (بتا)[ ۶، ۷ ] با افزایش سینتیک انتقال و / یا تشخیص ایمنی تغییر یافته بیشتر نیاز به استراتژیهای ضد ویروسی سریع و موثر دارد که میتواند تلاشهای واکسیناسیون فعلی را به منظور کنترل پاندمی فعلی تکمیل کند.
مطالعه اخیر راماکریشنان و همکارانش کاهش زمان بهبودی را در موارد خفیف کوید19 , که در یک آزمایش فاز 2 تصادفی , پس از استنشاق دوز کلی روزانه 1600 گرم budesonide [ 8 ] تجزیه و تحلیل شد , گزارش کردند . جالب توجه است که این مطالعه از این مشاهده الهامگرفته است که شیوع بیماریهای تنفسی مزمن در میان بیماران مبتلا به کوید19 در مقایسه با جمعیت عمومی کمتر به نظر میرسد [ 9 ] . بودزوناید، یک گلوکوکورتیکوئید غیر هالوژنه، یک داروی ضد التهاب گسترده است و معمولا از طریق استنشاق برای درمان بیماریهای تنفسی، مانند bronchiale آسم بزرگسالان و کودکان [ ۱۰، ۱۱ ]، و بیماری انسدادی مزمن متوسط تا شدید ریه (COPD)[ ۱۲ ] به کار میرود. علاوه بر اثرات ضد التهابی، budesonide شدهاست که بومیسونید یک فعالیت ضد ویروسی در شرایط آزمایشگاهی علیه عفونت رینو ویروس انسانی با فعالسازی اتوخواری از طریق غنیسازی گونههای فعال اکسیژن اعمال میکند [ ۱۳ ] و اخیرا برای کاهش اثر سایتوپاتیک سندروم تنفسی خاورمیانه (Mers)- سلولهای عفونی شده با CoV نشانداده شدهاست [ ۱۴ ]. علاوه بر اثرات ضد التهابی، نشانداده شدهاست که بودزوناید یک فعالیت ضد ویروسی در شرایط آزمایشگاهی علیه عفونت رینو ویروس انسانی با فعالسازی اتوفاژی از طریق غنیسازی گونههای فعال اکسیژن اعمال میکند [ ۱۳ ] و اخیرا برای کاهش اثر سایتوپاتیک سلول های عفونی شده با سندروم تنفسی خاورمیانه (MERS) نشانداده شدهاست [ ۱۴ ]. در همین راستا، یک مطالعه قبلی اثر بازدارندگی budesonide را در ترکیب با گلیکوپیرونیوم و فورموترول در برابر ویروس کرونا ویروس فصلی انسان (HCoV)- ۲۲۹ E گزارش کرد [ ۱۵ ].
با این حال، تاثیر مستقیم بر SARS - CoV - ۲ هنوز تا جایی که ما میدانیم مورد مطالعه قرار نگرفته است. از این رو، ما یک اثر ضد ویروسی بالقوه ترکیب خالص بودزوناید و مخلوط سوسپانسیون بودزوناید در برابر سویه SARS - CoV - ۲ WT B ۱.۷۰ و VOCs در حال گردش B.۱.۱.۷ (آلفا)و B.1.351 (بتا) را بررسی کردیم. روش رقیقسازی محدود برای تعیین تیتر ویروسی پس از درمان به کار گرفته شد در حالی که حیات سلولی با انتشار LDH نظارت شد. نتایج ما نشان میدهد که درمان با بودزوناید ، تیترهای SARS - CoV - ۲ و VOCs را به طور قابلتوجهی کاهش میدهد در حالی که قابلیت زیست پذیری سلول تحتتاثیر قرار نگرفته باقی میماند.
برچسب های مهم
CDC
به روز رسانی شده ۱۵ ژوئن ۲۰۲۱
واکسنهای کوید19 با استفاده از دانشی که برای چندین دهه وجود داشتهاست , توسعه یافتند .
واکسنهای کوید19 آزمایشی نیستند . آنها تمام مراحل مورد نیاز آزمایشها بالینی را طی کردند. آزمایش و نظارت گسترده نشان دادهاست که این واکسنها ایمن و موثر هستند.
واکسنهای کوید19 بیشترین نظارت ایمنی را در تاریخ ایالاتمتحده دریافت کرده و به کار خود ادامه میدهند . واکسنهای کوید19 موثر هستند
- واکسنها COVID ۱۹موثر هستند. آنها میتوانند شما را از انتشار ویروس کوید19 جلوگیری کنند . واکسن کوید19 به شما کمک میکند که حتی اگر کوید19 را هم دریافت کنید , به طور جدی بیمار نشوید .
هم چنین واکسینه کردن خود ممکن است از افراد اطراف شما , به ویژه افرادی که در معرض خطر بیماریهای شدید از کوید19 هستند , محافظت کند .
زمانی که به طور کامل واکسینه شدید، میتوانید کار بیشتری را شروع کنید
پس از اینکه واکسن کوید19 را به طور کامل دریافت کردید , میتوانید بسیاری از فعالیتهایی که قبل از این بیماری همهگیر انجام دادهاید را ازسر بگیرید . شما میتوانید فعالیتها را بدون پوشیدن ماسک و یا با فاصله ۶ فوت ادامه دهید، به جز مواردی که توسط قوانین فدرال، ایالتی، محلی، قبیلهای یا منطقهای، قوانین، قوانین، و مقررات، از جمله کسبوکار محلی و راهن مردم تا دو هفته پس از دومین دوز واکسن Pfizer - BioNTch یا واکسن مودرنا کوید19 , یا دو هفته پس از یک دوز واکسن جانسون جانسون , COVID19 , به طور کامل واکسینه نمیشوند . شما باید به استفاده از تمام ابزارهای موجود برای حفاظت از خود و دیگران ادامه دهید تا زمانی که به طور کامل واکسینه شوید.
در مورد واکسن کوید19 برای افراد با شرایط پزشکی اساسی و یا سیستم ایمنی ضعیف بیشتر یاد بگیرید .
واکسیناسیون کوید19 راهی امنتر برای کمک به ایجاد حفاظت است
صرفنظر از اینکه آیا قبلا کوید19 را داشتهاید یا خیر , واکسینه شوید . مطالعات نشان دادهاند که واکسیناسیون باعث افزایش حفاظت در افرادی میشود که از کوید19 بهبود یافتهاند .
در مورد ملاحظات بالینی برای افرادی که برای کوید19 با آنتیبادیهای مونوکلونال یا پلاسمای دوران نقاهت درمان شدهبودند یا سابقه سندروم التهابی چند سیستمی در بزرگسالان یا کودکان بیشتر بدانید .
کوید19 هنوز هم تهدیدی برای افرادی است که واکسینه نشده اند . برخی از افرادی که کوید19 دریافت میکنند ممکن است به شدت بیمار شوند , که میتواند منجر به بستری شدن شود , و برخی از افراد چندین هفته یا حتی بیشتر بعد از ابتلا به این بیماری , مشکلات سلامتی مداوم دارند . حتی افرادی که در زمان ابتلا علائم بیماری نداشته اند نیز میتوانند این مشکلات سلامتی مداوم را داشته باشند.
ایمنی پس از واکسیناسیون کوید19
هنوز چیزهای زیادی درباره واکسنهای کوید19 یاد میگیریم و CDC به طور مداوم در حال بررسی شواهد و به روز رسانی راهنمایی است . ما نمیدانیم چه مدت حفاظت برای کسانی که واکسینه شدهاند طول میکشد. آنچه ما میدانیم این است که کوید19 باعث بیماری و مرگ بسیار جدی برای بسیاری از مردم شدهاست .
اگر شما COVID۱۹ را گرفتید، در معرض خطر دادن آن به عزیزان خود که ممکن است بسیار بیمار شوند نیز قرار خواهید گرفت. گرفتن واکسن کوید19 انتخاب بی خطرتری است . در حال حاضر، اطلاعات محدودی در مورد اثربخشی واکسن در افرادی که دچار نقص ایمنی هستند، از جمله کسانی که از داروهای سرکوبکننده سیستم ایمنی استفاده میکنند، وجود دارد. هیچ کدام از واکسنهای کوید19 نمیتواند شما را از کوید19 بیمار کند .
هیچ کدام از واکسنهای کوید19 حاوی ویروس زنده کوید19 نیستند بنابراین واکسن کوید19 نمیتواند شما را مبتلا به کوید19 کند . فواید واکسن کوید19 چیست ؟
اگرچه کارشناسان هنوز در مورد واکسنهای کوید19 چیزهای زیادی یاد میگیرند , اما برخی فواید واضح برای واکسینه شدن وجود دارد .
اگر قبلا واکسن را دریافت کردهاید، کار عالی است! این حقایق را با دیگران که ممکن است مردد باشند به اشتراک بگذارید. اگر مطمئن نیستید که آیا واکسن برای شما مناسب است، این چهار فایده را که واکسن میتواند برای شما و عزیزان شما فراهم کند، در نظر بگیرید.
این واکسن خطر عفونت شما را کاهش میدهد.
هنگامی که شما اولین واکسن خود را دریافت کردید، بدن شما شروع به تولید آنتیبادی بر علیه ویروس کورونا میکند. این پادتنها به سیستم ایمنی شما در مبارزه با ویروس کمک میکنند اگر شما در معرض این ویروس قرار بگیرید، پس شانس ابتلا به این بیماری را کاهش میدهد. سه واکسن مجاز برای استفاده در ایالاتمتحده وجود دارد و همه آنها بیش از ۷۰ % در جلوگیری از عفونت موثر هستند. درست است که شما هنوز هم میتوانید پس از واکسینه شدن، آلوده شوید، اما یکبار دیگر جمعیت واکسینه میشود، این احتمال به خاطر چیزی به نام ایمنی گله، بیشتر کاهش مییابد. بنابراین، واکسینه شدن نه تنها شانس آلوده شدن شما را کاهش میدهد، بلکه به حفاظت از جامعه نیز کمک میکند و احتمال انتقال ویروس را کاهش میدهد.
این واکسن میتواند به نوزاد و یا نوزاد متولد نشده شما کمک کند.
یک مطالعه جدید نشان داد که مادران باردار که واکسن کوید19 را دریافت میکنند , آنتیبادی بر علیه ویروس ایجاد میکنند و آنها را از طریق جفت به نوزاد متولد نشده خود منتقل میکنند . مادران نیز نشان دادند که از طریق شیر مادر، آنتیبادی را به نوزادان خود منتقل میکنند. این نشان میدهد که آن نوزادان نسبت به ویروس مصونیت دارند که به ویژه مهم است چون کودکان کوچک نمیتوانند واکسن بگیرند. این واکسن از بیماری شدید محافظت میکند.
در طول مطالعات , سه واکسن مجاز در پیشگیری از بیماریهای شدید کوید19 موثر بودهاند . بنابراین حتی اگر واکسینه شوید و مبتلا شوید، احتمال اینکه به شدت بیمار شوید بسیار کم است. آزمایشها بالینی برای واکسنهای فایزر - بیونتک و مودرنا داد که آنها 100 % در پیشگیری از بیماریهای شدید موثر بودند . واکسن جانسون و جانسون ۸۵ % اثربخشی را در برابر بیماری شدید نشان داد.
این واکسنها همچنین در مقابله با انواع جدیدی که ما شروع به دیدن گردش خون میکنیم، مانند نوع دلتا، موثر هستند. این واکسنها همچنین در مقابله با واریانت های جدیدی که در گردش هستند، مانند نوع دلتا، موثر هستند. همانند سویه اصلی، هر سه واکسن از شما در برابر بیماریهای شدید محافظت میکنند و احتمال بستری شدن در بیمارستان را کاهش میدهند.
مطالعات نشان دادهاست که افراد واکسینه شده که آلوده میشوند در مقایسه با افرادی که واکسینه نمیشوند , موارد خفیف تا متوسط کوید19 دارند . بنابراین خطر بستری شدن و مرگ به دلیل کوید19 زمانی که به طور کامل واکسینه شدید تقریبا از بین میرود .
واکسن به ما کمک کرد تا ماسک رو کنار بزاریم
این واکسن آخرین گام در تلاش ما برای بازگشت به زندگی طبیعیتر است. اقدامات بهداشت عمومی مانند پوشیدن ماسک، فاصله فیزیکی و شستن دستها برای کاهش شیوع ویروس انجام شد و ثابت شد که این اقدامات موثر هستند. مرکز کنترل بیماریها در حال حاضر توصیه میکند که هر کسی که واکسینه نشده است به پوشیدن ماسک ادامه دهد. اگر واکسینه شوید و احساس راحتی بیشتری در پوشیدن یک ماسک داشته باشید، این به صلاحدید شما بستگی دارد.
شواهد حاکی از آن است که افراد واکسینه شده که ممکن است به ویروس کرونا آلوده شوند، ذرات ویروس کمتری در بینی و دهان خود دارند و احتمال اینکه این ویروس به دیگران سرایت کند، کمتر است. این یافته مهم است چون واکسینه شدن نه تنها از شما محافظت میکند بلکه گسترش ویروس به دوستان و عزیزان را نیز محدود میکند.
همانطور که افراد بیشتری به دریافت واکسن ادامه میدهند، ما ممکن است به ایمنی جمعی دست پیدا کنیم، که به این معنی است که گسترش ویروس بعید میشود. مهم است که همه ما این واکسن را دریافت کنیم تا به ما در رسیدن به این هدف بهداشت عمومی کمک کند.
این واکسن به شما کمک خواهد کرد که با دوستان و خانواده خود ارتباط برقرار کنید.
زمانی که واکسن را دریافت کردید و منتظر زمان توصیه شدهبرای بدن خود برای ایجاد ایمنی بودید، میتوانید شخصا با افراد دیگری که بدون ماسک واکسینه شدهاند، ملاقات کنید. همچنین , اگر در اطراف کسی بودهاید که تست کوید19 را مثبت ارزیابی کردهاست , اگر به طور کامل واکسینه شدهاید و علائم بیماری را تجربه نکرده اید , نیازی به قرنطینه ندارید .
پس از یک سال عدم اطمینان، این واکسن وارد شدهاست و مزایای روشنی دارد که باید به همه نشان دهد که باید به شدت به گرفتن واکسن فکر کنند. با انتخاب برای واکسینه شدن، شما نه تنها میتوانید از خودتان و خانواده بلکه از جامعه خود نیز محافظت کنید.
اهمیت واکسیناسیون جهانی کوید19
از زمانی که سازمان بهداشت جهانی شیوع کوید19 را در مارس 2020 یک بیماری همهگیر اعلام کرد , این ویروس جان بیش از 2.5 میلیون نفر را در سطح جهان گرفت و بیش از 113 میلیون مورد آن در آزمایشهای آزمایشگاهی تایید شد ( مارس 2021 ) .
پاندمی تقریبا تمام جنبههای زندگی را تحتتاثیر قرار دادهاست، و باعث شدهاست که اقتصادهای جهانی از کار بیفتند، شیوه کار و تعامل ما با عزیزانمان را تغییر دهند، و سیستمهای مراقبت بهداشتی را تا حدی گسترش دهند. دولتها در سراسر جهان مجبور شدهاند تا محدودیتهای شدیدی را بر فعالیتهای انسانی اعمال کنند تا از گسترش ویروس جلوگیری کنند.
واکسیناسیون کوید19 در حال حاضر راهی برای خروج از این مرحله از پاندمی است . بدون آنها، بسیاری از دانشمندان بر این باورند که ایمنی طبیعی گله برای بازگرداندن جامعه به وضعیت عادی خود کافی نبوده و منجر به مرگ و میر شدیدی شدهاست. این چیزی است که توسط بسیاری از سازمانهای بهداشتی از جمله سازمان بهداشت جهانی انعکاس یافتهاست. در یک سناریو بدون دسترسی به واکسن، اقدامات رفتاری شدید ممکن است برای آینده قابلپیشبینی باقی مانده باشد.
خوشبختانه، در آغاز سال ۲۰۲۱ واکسنهای متعددی با مجوز اضطراری دریافت کردند و شروع به کار در کشورهای سراسر جهان کردند. تا مارس ۲۰۲۱، تنها حدود ۳۰۰ میلیون دوز واکسن در سراسر جهان تجویز شده بود. این ارقام امید به بازگشت به حالت عادی را میدهند. با این حال , واکسیناسیون جهانی کوید19 با چالشهای متعددی روبرو است که ممکن است بر موفقیت آن تاثیر بگذارد .
تاثیر واکسیناسیون کوید19
در حال حاضر , در مجموع هفت واکسن کوید19 موجود در سه سطح مورد تایید قرار گرفته و در سراسر جهان در حال پخش شدن هستند . با این حال، برخی کارایی این واکسنها را زیر سوال میبرند، به ویژه با توجه به ظهور سویههای جدید ویروس. واکسن باید در کاهش چشمگیر گسترش ویروس موثر باشد تا آنها موفق شوند.
تحقیقات نشان دادهاست که واکسنهای مودرنا و مبتنی بر mRNA فایزر 94 - 95 % موثر هستند , و این ارقام حتی در مطالعاتی که افراد در معرض خطر بالا و افراد مسن را مورد مطالعه قرار میدهند نیز درست است .
این یک تصور غلط رایج است که این به این معنی است که ۹۵ % کسانی که واکسن را دریافت میکنند از بیماری محافظت میشوند و ۵ % بدون محافظ میمانند. اگر این امر صحت داشته باشد، در جمعیت ۱۰۰ هزار نفری که واکسینه شدهاند، این امر منجر به ابتلای ۵۰۰۰ نفر به ویروس و گسترش بیماری در طول سه ماه خواهد شد. اثربخشی 95 % در واقع به این معنی است که افراد دارای واکسن در مقایسه با گروه کنترل , 95 % کمتر در معرض خطر کوید19 قرار دارند . بدون واکسن، ما انتظار داریم که تقریبا ۱ % مردم به این بیماری مبتلا شوند و با واکسن، این میزان به ۰.۰۵ % کاهش مییابد. با چنین نرخ پایینی، واکسنها به جامعه اجازه خواهند داد تا به حالت "عادی" بازگردد و محدودیتها برای همیشه کاهش یابند.
از زمانی که سازمان بهداشت جهانی شیوع کوید19 را در مارس 2020 یک بیماری همهگیر اعلام کرد , این ویروس جان بیش از 2.5 میلیون نفر را در سطح جهان گرفت و بیش از 113 میلیون مورد آن در آزمایشهای آزمایشگاهی تایید شد ( مارس 2021 ) .
پاندمی تقریبا تمام جنبههای زندگی را تحتتاثیر قرار دادهاست، و باعث شدهاست که اقتصادهای جهانی از کار بیفتند، شیوه کار و تعامل ما با عزیزانمان را تغییر دهند، و سیستمهای مراقبت بهداشتی را تا حدی گسترش دهند. دولتها در سراسر جهان مجبور شدهاند تا محدودیتهای شدیدی را بر فعالیتهای انسانی اعمال کنند تا از گسترش ویروس جلوگیری کنند.
واکسیناسیون کوید19 در حال حاضر راهی برای خروج از این مرحله از پاندمی است . بدون آنها، بسیاری از دانشمندان بر این باورند که ایمنی طبیعی گله برای بازگرداندن جامعه به وضعیت عادی خود کافی نبوده و منجر به مرگ و میر شدیدی شدهاست. این چیزی است که توسط بسیاری از سازمانهای بهداشتی از جمله سازمان بهداشت جهانی انعکاس یافتهاست. در یک سناریو بدون دسترسی به واکسن، اقدامات رفتاری شدید ممکن است برای آینده قابلپیشبینی باقی مانده باشد.
۱.۱ آنتیبیوتیک
آنتیبیوتیکها سنگ بنای داروهای مدرن هستند و به طور گسترده در سراسر جهان توسعهیافته و در حال توسعه در انسان و برای اهداف دامپزشکی و کشاورزی مورد استفاده قرار میگیرند. آنها داروهایی هستند که رشد و تکثیر یک باکتری را از بین میبرند و برای درمان عفونتهای باکتریایی در بدن به کار میروند. آنها متمایز از آنتیسپتیکها (که برای استریل کردن بافت زنده و کاهش خطر عفونت به جای درمان عفونت به کار میروند)و ضدعفونیکنندهها (ضد میکروبی غیر انتخابی که طیف وسیعی از میکروارگانیسمها را میکشد، نه فقط باکتریها، و در سطوح غیر زنده به کار میروند)هستند. هم چنین آنها سم نیستند چون سموم به عنوان یک ماده سمی که توسط یک میکروارگانیسم، گیاه و یا حیوان تولید میشود و موجب بیماری در بدن میشود، تعریف میشوند. آنتیبیوتیکها باعث آسیب مستقیم به سلولهای انسانی نمیشوند. آنتیبیوتیکها میتوانند به صورت وریدی (از طریق سرنگ یا کاتتر)، عضلانی (از طریق سرنگ)، خوراکی (از طریق قرص، کپسول یا مایع)و یا موضعی (مانند کرم، لوسیون، اسپری یا قطره)تجویز شوند. Intravenous موثرترین مسیر است زیرا سطح خونی درمانی فوری آنتیبیوتیک را ایجاد میکند، اما روشهای دهانی اغلب ترجیح داده میشوند چون کمتر تهاجمی هستند، نیازی به بستری در بیمارستان ندارند، و اغلب به سطوح خونی فوق بازدارنده دست مییابند ۲.
آنتیبیوتیکها امروزه میتوانند در یک آزمایشگاه مورد استفاده قرار گیرند اما اغلب بر پایه ترکیباتی هستند که به طور طبیعی توسط میکروارگانیسمها برای آسیب رساندن یا کشتن باکتریها در محیط خود تولید میشوند. در واقع همه میکروارگانیسمها ترکیبات آنتیبیوتیک تولید نمیکنند، تنها حدود ۲۰ گونه وجود دارند که آنتیبیوتیک تولید میکنند که در حال حاضر تولید انبوه دارند و در پزشکی مورد استفاده قرار میگیرند ۳. به طور معمول این میکرو ارگانیسمهای ساکن خاک هستند، اگرچه جستجو برای آنتیبیوتیکهای جدید در حال حاضر شروع به تغییر به میکروب دریایی کردهاست. هر دوی این محیطها تنوع و تراکم بالای میکروارگانیسمها را نشان میدهند. تولید آنتیبیوتیک را می توان به عنوان مکانیسمی در کنار باکتریها و یا دفاع از آنها در نظر گرفت که امکان بقای تولید کننده آنتیبیوتیک را فراهم میآورد. ترکیبات آنتی بیوتیک همچنین میتوانند به عنوان مولکولهای سیگنالینگ بین سلولهای باکتریایی عمل کنند و رفتار باکتریایی مانند تشکیل بیوفیلم را تنظیم کنند. ۶. بنابراین، آنها نقش مهمی در طبیعت دارند که انسانها برای منفعت ما و استفاده از آنتیبیوتیکهای یکپارچه در پزشکی انسان و حیوان انتخاب کردهاند. تعیین کمیت دقیق تاثیر کلی آنتیبیوتیکها بر پویایی عفونت و تمایز بین اثرات عوامل دیگر مانند معرفی واکسن یا بهبود بهداشت دشوار است. با این وجود، استفاده از آنتیبیوتیک با کاهش مرگ و میر ناشی از بیماریهای مسری در سال و افزایش میانگین امید به زندگی در ارتباط است.
۱.۲ تاریخچه آنتیبیوتیکها
تنها به تازگی و در یک جدول زمانی نسبتا کوتاه است که آنتیبیوتیکها در جامعه ما تثبیت شدهاند تا عفونتهای باکتریایی را درمان کنند (شکل ۱ - ۱). درست ۱۱۰ سال پیش، پل ارلیخ (زیست شیمی دان آلمانی، ۱۸۵۴ - ۱۹۱۵)اصطلاح "گلوله جادویی" را زمانی ابداع کرد که در مورد یک ماده شیمیایی که میتواند به طور انتخابی عوامل بیماری زا را در بدن بدون آسیب رساندن به بیمار هدف قرار دهد و بکشد، نظریهپردازی کرد. اولین آنتیبیوتیک جادویی "واقعی" علیه باکتریهایی که به طور بالینی علیه عفونتهای باکتریایی استفاده میشدند، در واقع سالها قبل از استفاده از این اصطلاح مورد استفاده قرار میگرفت. پیوسیانین یک عصاره تهیهشده از باکتری گرم منفی سودوموناس آئروژینوزا توسط اممریچ و لو در سال ۱۸۹۹ بود. این ماده بر علیه تعدادی از باکتریهای بیماری زا فعال بود اما از آنجا که اثر بخشی آن متناقض بود و برای انسانها تا حدی سمی بود، رها شد . ارلیخ، که اکنون پدر بنیانگذار شیمیدرمانی و در مقیاس بزرگ است، با استفاده از صفحات سیستماتیک دارویی، گلوله جادویی خود ("ترکیب ۶۰۶")را علیه باکتری سیفیلیس، ترپونما پالیدوم ایجاد کرد. ترکیب ۶۰۶، یا سالوارسان، پس از کشف آن در سال ۱۹۰۹، رایجترین داروی تجویز شده بود. پرونتوسیل یک آنتیبیوتیک اولیه دیگر بود، ترکیبی که به عنوان بخشی از screen توسط شیمیدانان بایر جوزف کلیر و فریتز میتزش سنتز شد و نشان داده شد که خواص ضد باکتریایی در برابر تعدادی از بیماریها توسط گرهارد دوماگ دارد.. جز فعال سولفانامید قبلا در صنعت رنگ مورد استفاده قرار گرفته بود و پیش از این اختراع نشده بود و امکان تولید مشتقات سولفونامید توسط شرکتهای مختلف را فراهم میکرد. سولفونامیدها قدیمیترین گروه از آنتیبیوتیکها هستند و نسخههای جدید هنوز هم تولید میشوند و امروزه مورد استفاده قرار میگیرند.
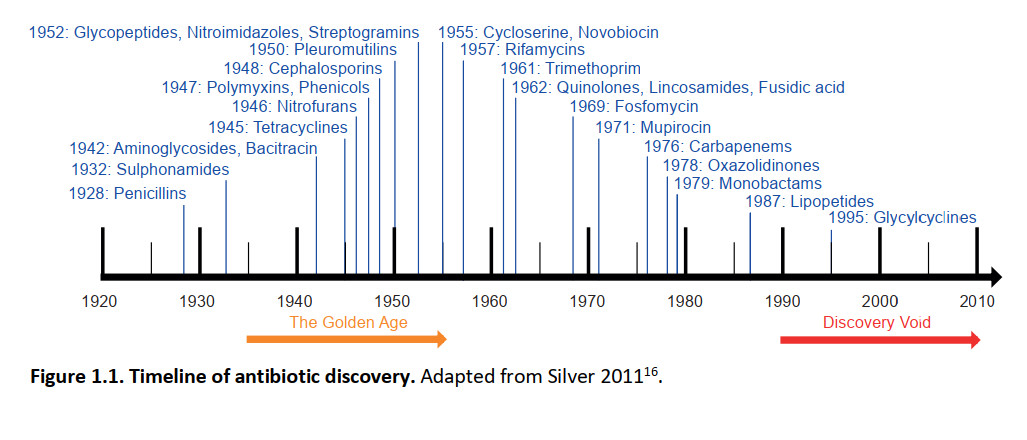
شکل ۱ - ۱: خط زمانی کشف آنتیبیوتیک.
احتمالا معروفترین آنتیبیوتیک، و یکی از قدیمیترین آنتیبیوتیکهای تولید انبوه، پنیسیلین است که در سال ۱۹۲۸ در داستان معروف الکساندر فلمینگ (باکتریشناس اسکاتلندی، ۱۸۸۱ - ۱۹۵۵)و یک پنجره باز کشف شد.
احتمالا شناختهشدهترین آنتیبیوتیک و یکی از قدیمیترین آنتیبیوتیکهای تولید شده به صورت انبوه، آنتیبیوتیک است.
پنیسیلین، در سال ۱۹۲۸ در داستان معروف الکساندر فلمینگ (باکتریشناس اسکاتلندی، ۱۸۸۱ - ۱۹۵۵)و یک پنجره باز کشف شد. یک قارچ مرموز از میان یک پنجره باز و پلیت های آلوده عبور کرده بود که برای مطالعه استافیلوکوکوس مورد استفاده قرار میگرفت، که به عنوان عامل عفونت در انسان شناخته میشد، و این قارچ موفق به توقف رشد این باکتری شده بود.
خواص ضد میکروبی کپکها از قبل شناخته شدهبودند، اما فلمینگ به طور قابلتوجهی در تلاشهای خود برای تصفیه ترکیب دقیق مسئول این اثر، وقف شد. پنیسیلین سرانجام در سال ۱۹۴۵ با غلبه بر سالوارسان در ۱۵ سالگی به تولید انبوه رسید. آنتیبیوتیکهای پنیسیلین تا به امروز هنوز بیشترین داروی تجویز شده در سطح جهان هستند. تولید انبوه پنیسیلین با کشف استرپتومایسین در سال ۱۹۴۳ همزمان شد، یک آنتیبیوتیک جدا شده از باکتری خاک، استرپتومایسس گریزئوس که میتوانست میکوباکتریوم سل، علت سل را درمان کند. این وقایع آغاز "عصر طلایی آنتیبیوتیکها" را نشان داد (شکل ۱.۱): هجده نوع آنتیبیوتیک جدید بین سالهای ۱۹۴۴ تا ۱۹۷۰ کشف شد. پس از آن نرخ کشف با تنها چهار کلاس جدید در دهه ۱۹۷۰ و یک کلاس در دهه ۱۹۸۰ شروع به کاهش کرد. از آن زمان تا کنون هیچ نوع آنتیبیوتیک جدیدی کشف نشده است.
تنها "کشفهای مجدد" رخ دادهاند که شامل اصلاحات آنتی بیوتیکهای از قبل شناختهشده هستند (جدول ۱.۱). کاهش در کشف طبقات جدیدی از آنتیبیوتیکها به دلیل ظهور و گسترش مقاومت آنتیبیوتیکی مشکلساز است، که در آن عفونتهای باکتریایی دیگر نمیتوانند با همان داروهایی که زمانی موثر بودند درمان شوند. از آنجایی که آنتیبیوتیکها از دنیای امروز جداییناپذیر هستند، نگرانیهایی در مورد دوره پس از آنتیبیوتیک وجود دارد. با توجه به این موضوع، تحقیقات فوقالعادهای در سراسر جهان برای کشف آنتیبیوتیکهای جدید، توسعه جایگزینهایی برای آنتیبیوتیکها، و درک تکامل و گسترش مقاومت آنتیبیوتیکی در حال انجام است.
جدول ۱.۱ منابع آنتیبیوتیکها.
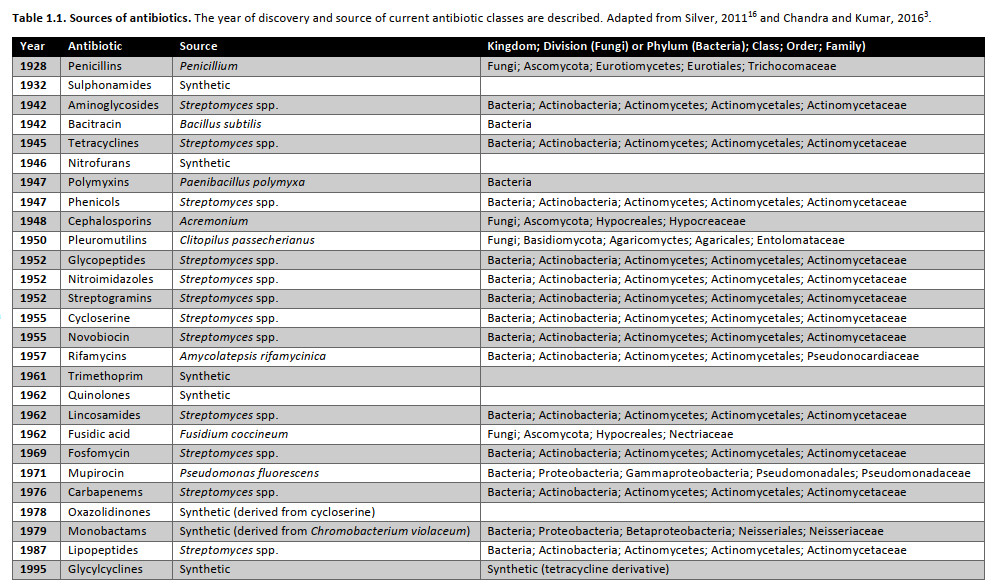
سال کشف و منبع کلاسهای فعلی آنتیبیوتیک توضیح داده میشود.
۱.۳ آنتیبیوتیکهای مربوط به کلینیک
امروزه، ۱۷ گروه از آنتیبیوتیکها برای سازمان بهداشت جهانی ضروری هستند (جدول ۱.۲). سه دسته از آنتیبیوتیکهای ضروری وجود دارد: دسترسی (اولین یا دومین خط گزینههای دفاعی برای عفونتهای شایع)؛ مراقب باشید (پتانسیل مقاومت بالاتر اما هنوز هم به عنوان تیمار خط اول یا دوم توصیه میشود)؛ و رزرو (گزینه "آخرین راهحل" برای عفونتهای جدی مقاوم به آنتیبیوتیک). هر آنتیبیوتیک مکانیسم عمل متفاوتی دارد (شکل ۱.۲)، مکانیسم مقاومت و میتواند انواع مختلف پاتوژن های باکتریایی را هدف قرار دهد (جدول ۱.۲). این ممکن است شامل باکتریهای گرم منفی و گرم مثبت باشد که توسط تکنیک رنگآمیزی گرم که توسط هانس کریستین گرم در سال ۱۸۸۴ ایجاد شد تعیین شدهاست. علاوه بر این، باکتریها میتوانند به شدت هوازی یا بیهوازی باشند، به این معنی که نبود یا حضور اکسیژن به ترتیب سمی است، یا جایی بین آنها. آنتیبیوتیکها مانند آمینوگلیکوزیدها بر اجزای مسیر تنفس هوازی تکیه میکنند و چنین تصور میشود که طیف فعالیت آنها تنها شامل باکتریهای هوازی است نه بیهوازی. آنتیبیوتیکهای ضروری در زیر با جزئیات بیشتر مورد بحث قرار میگیرند، از جمله طیف گزارششده آنها از فعالیت.
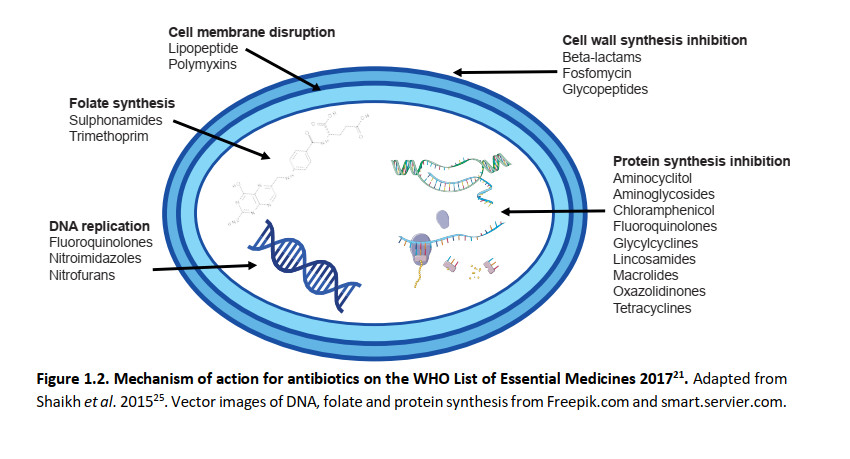
شکل ۱.۲ مکانیسم عمل آنتیبیوتیکها در فهرست داروهای ضروری سال ۲۰۱۷ سازمان بهداشت جهانی
جدول ۱.۲ آنتیبیوتیکهای موجود در نسخه بیستم فهرست داروهای ضروری سازمان بهداشت جهانی (۲۰۱۷). این آنتیبیوتیکها توسط WH O برای درمان عفونتهای باکتریایی ضروری هستند. سه دسته وجود دارد: دسترسی (گزینههای خط اول یا دوم برای عفونتهای مشترک)؛ مراقب باشید (پتانسیل مقاومت بالاتر اما هنوز هم به عنوان تیمار خط اول یا دوم توصیه میشود)؛ و رزرو (گزینه "آخرین راهحل" برای عفونتهای جدی مقاوم به آنتیبیوتیک). به گفته سازمان بهداشت جهانی، آنتیبیوتیکهای دسترسی، داروهای خط اول یا دوم برای بیماریهای عفونی مشترک هستند و باید به صورت گسترده در دسترس، مقرونبهصرفه، به طور مناسب فرموله شده و کنترل کیفی باشند. آنتیبیوتیکهای خط اول معمولا طیف باریکی هستند: آنها تنها طیف محدودی از باکتریها را هدف قرار میدهند، مانند باکتری بیماری زای مورد نظر و احتمالا برخی از اعضای نزدیک. آنها همچنین باید دارای پتانسیل مقاومت پایین و نسبت سود به ریسک مثبت باشند یعنی خطر آسیب به بیمار در مقایسه با درمان بالقوه عفونت آنها پایین است. آنتیبیوتیکهای طیف گسترده، که طیف وسیع تری از باکتریها را هدف قرار میدهند، به طور کلی به عنوان گزینههای خط دوم استفاده میشوند، مانند داروهایی با پتانسیل مقاومت بالاتر یا نسبت سود به ریسک کمتر (به عنوان مثال آنها ممکن است عوارض جانبی مشترک یا جدی تری داشته باشند).
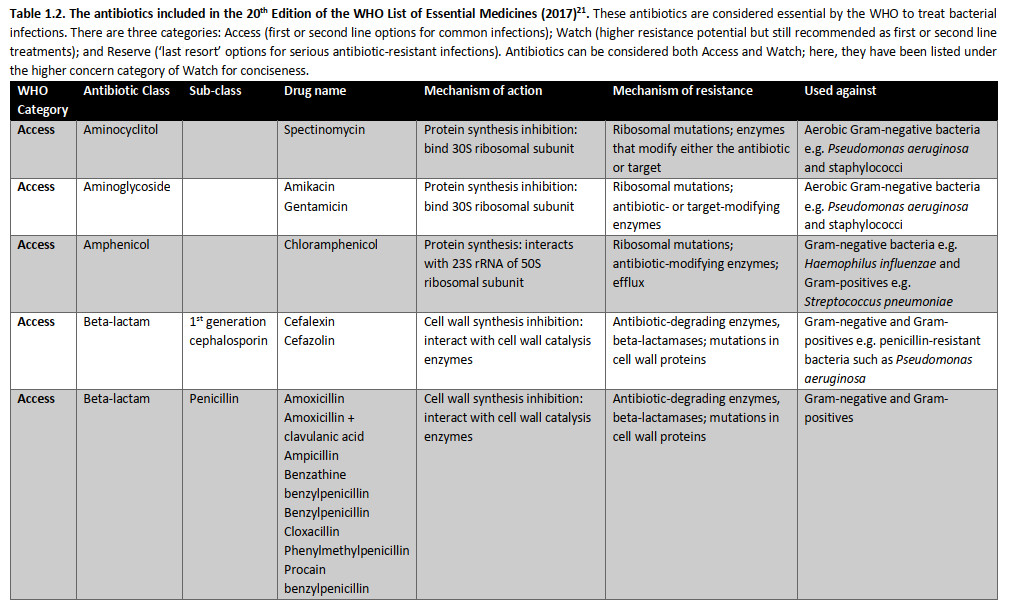
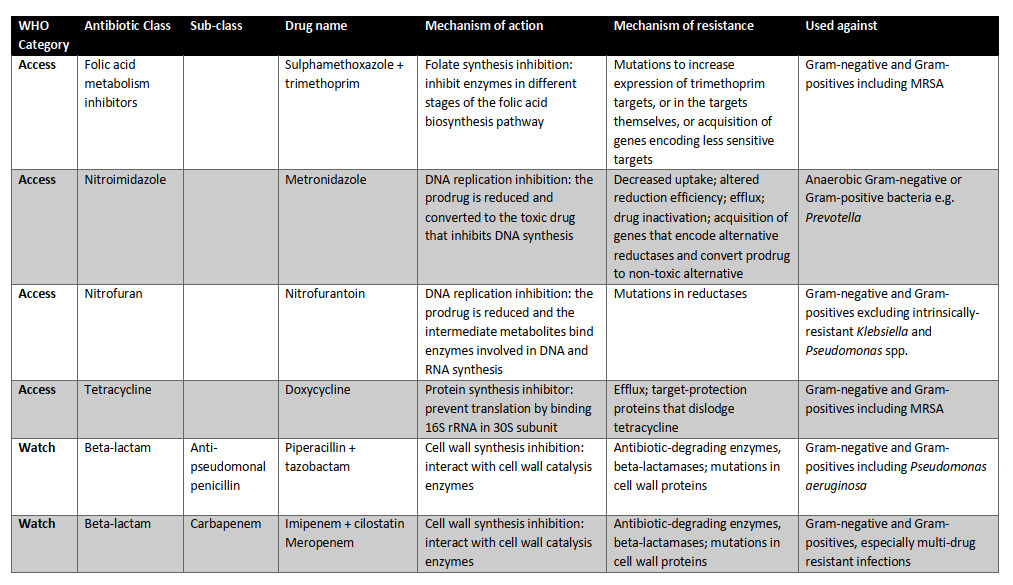
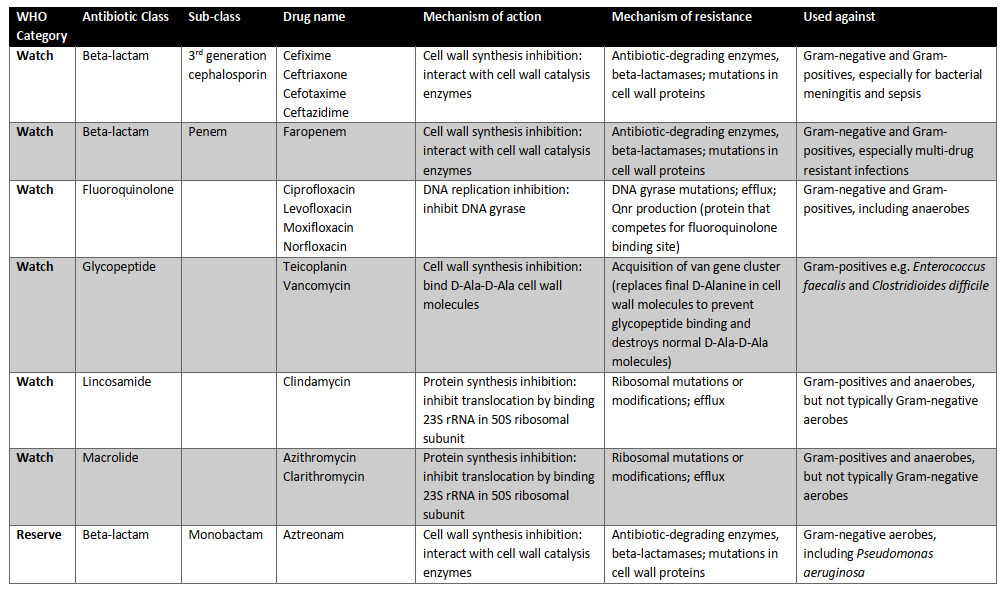
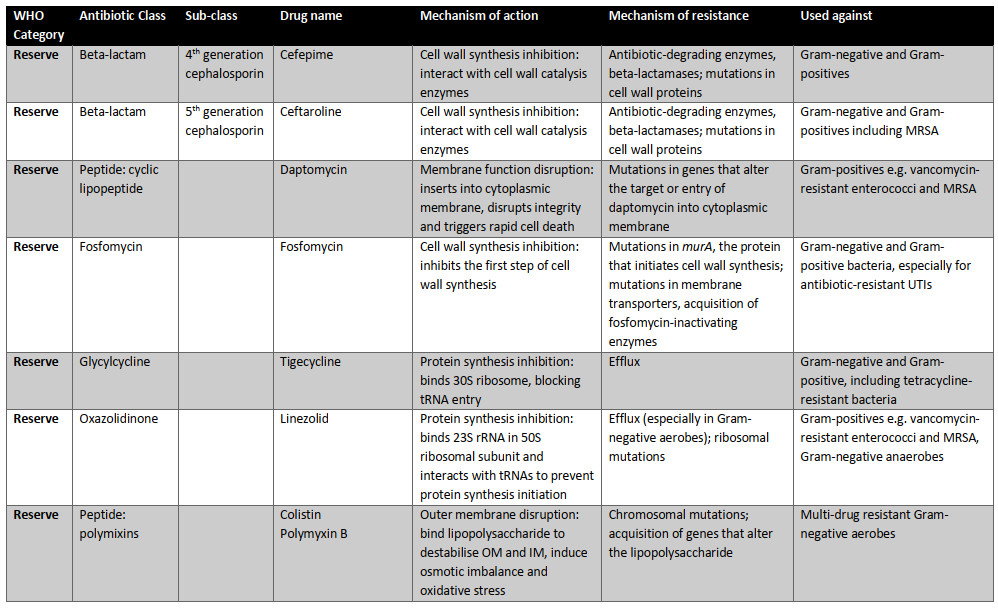
آنتیبیوتیکهای آمینو سیتوکلیتول، مانند اسپکتینومایسین، زیر واحد ۳۰ S ریبوزوم باکتریایی را متصل میکنند و سنتز پروتئین را مختل میکنند.
آمینوگلیکوزیدها مانند آمیکاسین و جنتامایسین از طریق مکانیسم مشابه عمل میکنند. برای انجام این کار، آنها باید از طریق غشا سیتوپلاسمی خود وارد سلول شوند، فرایندی که به ترانسپوت باکتریایی فعال وابسته به انرژی نیاز دارد.
این امر به نوبه خود نیازمند اکسیژن و نیروی محرکه پروتون فعال است.
بنابراین این داروها فقط برای باکتریهایی که قادر به تنفس هوازی هستند موثر هستند و آمینوگلیکوزیدها در مقابل باکتریهای بیهوازی که برای زنده ماندن بدون اکسیژن سازگار شدهاند و اجزای مورد نیاز معمول برای انتقال این داروها به داخل سلولهای خود را ندارند، غیرفعال محسوب میشوند. بنابراین، این داروها طیف گستردهای در نظر گرفته میشوند اما تنها برای طیف وسیعی از باکتریهای هوازی هستند.
اگرچه این آنتیبیوتیکها برای انسان سمی شناخته میشوند و میتوانند باعث کاهش شنوایی شوند، اما به عنوان خط اول درمان عفونتهای تنفسی در بیماران فیبروز کیستیک در نظر گرفته میشوند.
آنها همچنین برای درمان عفونتهای مقاوم به چند دارو (MDR)، اغلب به عنوان بخشی از درمان ترکیبی با بتالاکتام ها مورد استفاده قرار میگیرند، زیرا این دسته از آنتیبیوتیکها وقتی با هم استفاده شوند، اثر سینرژیک دارند. مقاومت آمینوگلیکوزیدی توسط جهشهای ریبوزومی، آنزیمهایی که آنتیبیوتیک یا آنزیمهایی که هدف را تغییر میدهند، میانجی گری میشود.
کلرآمفنیکل، یک amphenicol، یک آنتیبیوتیک طیف وسیع در نظر گرفته میشود و با rRNA ۲۳ S زیر واحد ریبوزومی ۵۰ S میانکنش میدهد و از سنتز پروتئین جلوگیری میکند. این روش خط اول برای عفونتهای چشمی مانند ورم ملتحمه است که میتواند توسط باکتریهایی از جمله هموفیلوس آنفلوانزا، استرپتوکوک پنومونیه و موراکسلا کاتارالیس ایجاد شود. مقاومت به کلرامفنیکل توسط جهشهای ریبوزومی یا آنزیمهای تغییر دهنده کلرامفنیکل میانجی گری میشود. همچنین میتواند به دلیل مقاومت با واسطه برونریزی باشد. جهش در اجزای سیستمهای برونریزی میتواند تمایل به مولکولهای خاصی از جمله آنتیبیوتیکها را افزایش دهد که منجر به افزایش مقاومت میشود.
بتالاکتام ها گروه متنوعی از آنتیبیوتیکها با چندین زیر گروه هستند.
این شامل پنیسیلینها، سفالوسپورین ها، کارباپنم ها و مونوباکتام ها است. آنتیبیوتیکهای بتا لاکتام ساختار شیمیایی مشابه دی - آلانیل - D - Alanine (D - Ala - D - Ala)دارند که یک "بلوک سازنده" دیوارهای سلول باکتریایی است. این بدان معنی است که بتالاکتام ها میتوانند با آنزیمهایی که سنتز دیواره سلولی را کاتالیز میکنند، از سنتز مناسب دیواره سلولی جلوگیری کنند و منجر به ناپایداری اسمزی و مرگ سلول باکتریایی شوند.
زیر ردههای مختلف بتالاکتام ها با اصلاح ساختار استاندارد بتالاکتام که آن گروه خاص را تعریف میکند، طبقهبندی میشوند.
پنیسیلینها و سفالوسپورین های نسل اول در لیست دسترسی آنتیبیوتیکها قرار دارند.
هر دوی این زیر طبقات از بتالاکتام ها معمولا طیف باریکی در نظر گرفته میشوند. اما طیف آن از دارویی به دارویی دیگر متفاوت است. برای مثال آموکسیسیلین در مقایسه با پنیسیلین اصلی طیف وسیع و یا طیف وسیع تری دارد.
Penicillins، به ویژه آموکسیسیلین، اولین داروی خط اول درمان عفونتهای باکتریایی شایع مانند عفونتهای دندانی، گوش، تنفسی و گلو هستند، از این رو جایگاه آنها به عنوان پر مصرف ترین داروها در دنیا است.
ژنهایی که آنزیمهای بتالاکتاماز را کد میکنند، که آنتیبیوتیکهای بتالاکتام را تجزیه میکنند، برخی از رایجترین ژنهای مقاومت آنتیبیوتیکی (ARG ها)بیش از ۱۰۰۰ ژن بتالاکتاماز مختلف هستند. بتالاکتام ها میتوانند در کنار یک مهار کننده بتالاکتاماز، مانند آموکسیسیلین با کلاولانیک، برای جلوگیری از عملکرد مناسب یک آنزیم بتالاکتاماز داده شوند. این ترکیب بازده آموکسیسیلین را افزایش میدهد. سفالوسپورین های نسل اول، مانند سفالکسین و سفازولین، اغلب به عنوان گزینههای خط دوم به عنوان جایگزین پنیسیلین در موارد مقاومت یا آلرژی استفاده میشوند. مقاومت بتا - لاکتامی همچنین میتواند با جهش یا تغییر در هدف آنتیبیوتیک (پروتئینهای متصل شونده به پنیسیلین (PBPs)در دیواره سلول)یا در پورینها میانجی گری شود، که به آنتیبیوتیکهای بتا - لاکتامی اجازه ورود به سلول را میدهد.
متابولیسم اسید فولیک مانع از ترکیب سولفامتوکسازول و تری متوپریم در برابر بسیاری از عفونتهای باکتریایی مختلف میشود. باکتریها باید از نو ترکیب شوند تا بتوانند به عنوان عوامل مشترک برای مسیرهای مختلف بیوسنتزی عمل کنند. بدون این عوامل رشد آنها مهار میشود. سولفونامیدها، مانند سولفامتوکسازول و تری متوپریم، یک آنتیبیوتیک دی آمینوپیریمیدین، آنزیمهای درگیر در مراحل مختلف مسیر سنتز اسید فولیک را مهار میکنند و در نتیجه این ترکیب به عنوان سینرژیستی در نظر گرفته میشود. این یک درمان خط اول شایع برای عفونتها از جمله عفونتهای مجاری ادراری (UTIs)، اسهال مسافرتی، عفونتهای پوستی استافیلوکوکوس اورئوس مقاوم به متی سیلین (MRSA)، عفونتهای دستگاه تنفسی و وبا است. مقاومت در برابر تری متوپریم توسط جهشهایی میانجی گری میشود که بیان اهداف تری متوپریم را افزایش میدهد به طوری که تعداد آنتیبیوتیکها بیشتر شده و اثر آن محدود میشود. جهشهایی که خود اهداف را تغییر میدهند یا به دست آوردن ژنهایی که اهداف با حساسیت کمتر را رمزگذاری میکنند نیز منجر به مقاومت به تریمتوپریم میشوند. مقاومت سولفونامید رایج است و عمدتا به دلیل ژنهای حامل پلاسمید است که آنزیمهای جایگزین را کدگذاری میکنند که حساسیت کمتری به آنتی بیوتیکها دارند. این یک روش انتقال افقی ژن (HGT)است: حرکت ژنها بین سلولهای باکتریایی که عبور عمودی را نادیده میگیرند.
نیتروایمیدازول، مترونیدازول، سنتز DNA را مهار میکند و باعث آسیب DNA در سلولهای باکتریایی بیهوازی میشود. باکتریهای هوازی سرسخت فاقد پروتیین حامل الکترون با پتانسیل احیای منفی کافی برای فعال کردن فرم پرودارو پس از ورود به سلول هستند در نتیجه مترونیدازول دارای طیف مخالف با آمینوگلیکوزیدها است. این اولین گزینه برای عفونتهای ناشی از باکتریهای بیهوازی مانند آبسههای دندانی (به عنوان مثال توسط پرووتلا یا استرپتو کوکوس) و یا واژینوز باکتریایی ناشی از گارنل یک انگل است. مقاومت با کاهش جذب و یا تغییر بازده کاهش (که منجر به کاهش جذب نیز میشود)میانجی گری میشود. غیر فعالسازی موثر و دارو نیز ممکن است، همانطور که به دست آوردن ژنهای nim از باکتریهای دیگر از طریق HGT است. این ژنهای nim آنزیمهای جایگزین ردوکتاز را کدگذاری میکنند تا پیش دارو را به یک جایگزین غیرسمی تبدیل کنند.
نیتروفوران، نیتروفورانتوئین، خواص ضد میکروبی متعددی دارد که هیچ کدام به طور کامل درک نمیشوند. همانند نیتروایمیدازول ها، این یک پرودارو است و در داخل سلول باکتریایی بوسیله عمل nitroreductases فعال میشود. متابولیت های واسطه تولید شده به ریبوزوم باکتریایی و آنزیمهای درگیر در سنتز DNA و RNA، به علاوه دیگر فرایندهای متابولیک متصل میشوند. این طیف گسترده با فعالیت علیه هردو گونه گرم منفی و گرم مثبت است، اگرچه برخی گونههای کلبسیلا و سودوموناس ذاتا مقاوم هستند و یک درمان خط اول برای UTIs های ساده و کمتر است. گمان میرود که مقاومت با جهش در nitroreductases میانجی گری شود.
Tetracyclines مانند داکسی سیکلین نوع دیگری از مهار کنندههای سنتز پروتئین هستند که براساس بخشهای حفاظتشده rRNA ۱۶ S در زیر واحد ۳۰ S عمل میکنند و از ترجمه جلوگیری میکنند. طیف گستردهای دارد و عموما برای درمان عفونتهای مقاربتی (STI)، بیماری لایم، عفونتهای پوستی و MRSA استفاده میشود. مقاومت توسط پمپهای تراوشی مخصوص تتراسایکلین و یا پروتئینهای حفاظت از هدف که تتراسایکلین را هنگامی که به ریبوزوم متصل است، دفع میکنند، میانجی گری میشود.
برچسب های مهم
۲۲ ژوئیه ۲۰۲۱
( رویترز ) یک مطالعه جدید نشان میدهد که میزان مرگ و میر بیش از حد هندی در طی پاندمی کوید19 میتواند تا 4.9 میلیون نفر باشد و شواهد بیشتری را فراهم میکند که نشان میدهد ممکن است میلیون ها نفر در اثر ویروس کرونا جان خود را از دست داده باشند . گزارش مرکز توسعه جهانی مستقر در واشنگتن، که مشاور اقتصادی ارشد سابق هندی، آرویند سوبرامانیان، آن را نوشته بود، شامل مرگ و میر ناشی از همه علل از زمان آغاز این بیماری همهگیر تا ژوئن امسال بود.
آمار رسمی بیش از ۴۱۴،۰۰۰ مرگ در آمریکا و برزیل سومین آمار بالای جهان پس از ایالاتمتحده و برزیل است، اما این مطالعه به درخواستهای روزافزون متخصصان برای بررسی دقیق تلفات در سراسر کشور میافزاید.
دادههای رسمی نشان میدهد که یک افزایش مخرب در عفونتها در آوریل و می، که تا حد زیادی توسط انواع خطرناک و مسری دلتا هدایت میشود، سیستم مراقبتهای بهداشتی را از بین برده و حداقل ۱۷۰۰۰۰ نفر را فقط در ماه می کشتهاست. این گزارش با تخمین بین ۳.۴ میلیون و ۴.۹ میلیون مرگ اضافی در طی این بیماری همهگیر گفت: " آنچه به طور غم انگیزی روشن است این است که بسیاری از مردم، به جای صدها هزار نفر، ممکن است مرده باشند." اما همه مرگ و میرهای بیش از حد را به این بیماری همهگیر نسبت نداده است. نویسندگان در مقاله کاری خود (https://bit.ly/۳xJ۳LJ)که در وب سایت مرکز توسعه جهانی پست شدهاست، توضیح میدهند: " ما بر مرگ و میر همه علل تمرکز میکنیم و مرگ و میر بیش از حد را نسبت به خط پایه پیش از پاندمی تخمین میزنیم، و برای فصلی بودن تنظیم میکنیم."
وزارت بهداشت بلافاصله به ایمیل رویترز پاسخ نداد تا نظر خود را اعلام کند.
برخی کارشناسان گفتهاند که مرگ و میر بیش از حد بهترین راه برای اندازهگیری تلفات واقعی کوید19 است .
سومیا سوامیناتان، دانشمند ارشد سازمان بهداشت جهانی در توییتر گفت: " برای هر کشوری، مهم است که مرگ و میر بیش از حد تنها راه آمادهسازی سیستم سلامت برای شوکهای آینده و جلوگیری از مرگ و میر بیشتر باشد."
نیویورکتایمز گفت که محافظه کارانه ترین برآورد مرگ و میر در هند ۶۰۰۰۰۰ نفر بوده و بدترین سناریو چندین بار است که وجود دارد. دولت این ارقام را رد کردهاست.
کارشناسان بهداشت دلیل اصلی این امر را منابع کمیاب موجود در خانههای وسیع بین ایالتی برای دو سوم جمعیت هند یعنی نزدیک به ۱.۴ میلیارد نفر و همچنین تعداد زیادی مرگ و میر در خانه بدون اینکه مورد آزمایش قرار گیرند میدانند. هند کاهش عفونتهای روزانه از اوج ماه مه را گزارش کردهاست و ۳۰،۰۹۳ مورد جدید سهشنبه در عرض چهار ماه کمترین آمار روزانه خود را داشتهاند. دولت نخستوزیر نارندرا مودو نیز به خاطر کمپین واکسیناسیون آشفتهای که بسیاری میگویند به بدتر شدن موج دوم عفونتها کمک کردهاست، مورد انتقاد قرار گرفتهاست.
تنها بیش از ۸ درصد از هندیشمردگان واجد شرایط هر دو دوز واکسن را دریافت کردهاند. در ماه ژوئیه، دولت به طور متوسط کمتر از ۴ میلیون دوز روزانه تجویز کرد که این مقدار از رکورد ۹.۲ میلیون در ۲۱ ژوئن کمتر بود، یعنی زمانی که "مدی" مبارزه آزادی را برای تلقیح همه ۹۵۰ میلیون بزرگسال آغاز کرد.
۲۲ ژوئیه ۲۰۲۱
(رویترز)براساس دادههای منتشر شده در روز سهشنبه از بررسی ۲۹۰۰۰ نفر در سراسر کشور که در ماههای ژوئن و جولای انجام شد، دو سوم جمعیت هند دارای آنتیبادی بر علیه ویروس کرونا هستند.
چهارمین تحقیق ملی شامل ۸،۶۹۱ کودک ۶ تا ۱۷ ساله برای اولین بار است. نصف آنها seropositive بودند.
این بررسی نشان داد که ۶۷.۶ درصد از بزرگسالان سرم مثبت بودند در حالی که بیش از ۶۲ درصد از بزرگسالان واکسینه نشده بودند. از ماه ژوئیه، تنها بیش از ۸ درصد از Indians واجد شرایط دو دوز واکسن دریافت کرده بودند.
این بررسی نشان داد که در حدود ۴۰۰ میلیون نفر از ۱.۴ میلیارد نفر هندی آنتیبادی نداشتند.
پس از موج دومی که سیستم مراقبتهای بهداشتی را فلج کرد، موارد روزانه هند به پایینترین سطح خود در چهار ماه گذشته رسیدهاست. اما متخصصان به مقامات در مورد بازگشایی سریع شهرها هشدار دادهاند و نگرانی خود را در مورد ازدحام بیش از حد در مکانهای گردشگری ابراز کردهاند.
موج دوم همچنان ادامه دارد. وینوود کومار پاول، یکی از مشاوران ارشد دولت، در یک کنفرانس خبری گفت: " خطر شیوع بیماریهای جدید در آنجا بسیار زیاد است."
... یکی از سه، هر جا که هستی " او گفت: " هنوز هم در معرض خطر است و به همین دلیل پاندمی به هیچ وجه تمام نمیشود."
این مطالعه همچنین ۷،۲۵۲ تن از کارکنان بخش مراقبت بهداشتی را مورد بررسی قرار دادهاست و یافتهاست که ۸۵ درصد از آنها دارای آنتیبادی هستند و یکی از آنها در ۱۰ نفر واکسینه نشده است.
ماه گذشته , دادهها نشان داد که حداقل نیمی از افراد زیر 18 سال در پایتخت مالی هند در بمبئی در معرض کوید19 قرار داشتند و بر علیه آن آنتیبادی داشتند . برخی کارشناسان گفتهاند که موج سوم میتواند کودکان را هدف قرار دهد. بمبئی برای آمادهسازی به دیگر شهرها در ساخت بخشهای بزرگ کودکان پیوستهاست.
۲۲ ژوئیه ۲۰۲۱
(رویترز)یک تغییر ناگهانی در عفونت کرونا ویروس جدید به دلیل واریانت دلتا بسیار مسری و کند شدن میزان واکسیناسیون، دولتها را مجبور کردهاست تا کووید ۱۹ را برای کارکنان بهداشتی و دیگر گروههای پرخطر اجباری کنند.
تعداد رو به رشدی از کشورها همچنین تصریح میکنند که برای شام خوردن بیرون از خانه، در میان دیگران، به یک تزریق یا آزمون منفی نیاز است.
در اینجا به برخی از کشورها دستور واکسن داده شدهاست. استرالیا
استرالیا در اواخر ماه ژوئن تصمیم گرفت تا واکسیناسیون کوید19 را برای کارکنان و کارکنان در هتلهای قرنطینه اجباری کند . این برنامه همچنین واکسیناسیون را برای ورزشکاران پارالمپیک که به توکیو میروند اجباری کردهاست چرا که اعضای واکسینه نشده تیم میتوانند خطر سلامتی را به جان بخرند. بریتانیا
برای کارکنان خانههای مراقبت در انگلستان الزامی است که از ماه اکتبر واکسن کرونا ویروس دریافت کنند.
کلوپهای شبانه انگلیسی و سایر مکانهای با جمعیت زیاد از حامیان میخواهد تا اثبات واکسیناسیون کامل را از پایان سپتامبر ارائه دهند. کشور کانادا
دبیرخانه هیات خزانهداری کانادا در 20 جولای اعلام کرد که در حال بررسی این موضوع است که آیا واکسن کوید19 باید برای نقشها و موقعیتهای خاصی در دولت فدرال مورد نیاز باشد یا خیر .
همه کارکنان بهداشتی در فرانسه باید واکسن COVID۱۹ را دریافت کنند و هر کسی که میخواهد وارد سینما یا سوار قطار شود باید مدرک واکسیناسیون یا تست منفی را تحت قوانین جدید که توسط رئیسجمهور امانوئل مک رون در ۱۲ جولای اعلام شد، نشان دهد.
دولت در روز ۱۹ ژوئیه اعلام کرد که جریمه برنامهریزیشده ۴۵۰۰۰ یورویی برای کسب و کارهایی که بررسی نمیکنند که مشتریان کارت سلامت دارند، بسیار پایینتر خواهد بود. این جریمه از بیش از ۱۵۰۰ یورو شروع خواهد شد و به تدریج برای مجرمان تکراری افزایش خواهد یافت. جریمه فورا اعمال نخواهد شد. کشور یونان
یونان در روز ۱۲ ژوئیه واکسیناسیون را برای کارکنان پرستاری خانه با تاثیر فوری و کارکنان مراقبتهای بهداشتی از ماه سپتامبر اجباری کرد. به عنوان بخشی از تدابیر جدید، تنها به مشتریان واکسینه شده اجازه داده میشود که در خانهها، سینماها، تئاترها و دیگر فضاهای بسته در خانهها بمانند. کشور اندونزی
اندونزی در ماه فوریه تلقیح کوید19 را اجباری کرد , و پایتخت جاکارتا برای رد واکسن , جریمههای تا 5 میلیون روپیه ( 357 دلار ) را تهدید کرد .
ایتالیا
حکمی که توسط دولت ایتالیا در ماه مارس تصویب شد حکم میدهد که کارکنان بهداشتی از جمله داروسازان واکسینه شوند. کسانی که حاضر نیستند تا آخر سال از کار برکنار شوند. قزاقستان
وزارت بهداشت قزاقستان در روز 23 ژوئن اعلام کرد که این کشور واکسیناسیون اجباری کوید19 یا انجام آزمایشها هفتگی برای افرادی که در گروههای بالای 20 سال کار میکنند را انجام خواهد داد .
لهستان
لهستان میتواند واکسیناسیون را برای برخی افراد در معرض خطر کوید19 از آگوست اجباری کند .
روسیه
براساس گزارش مسکو تایمز، پایتخت روسیه از طرحی به نام https://bit.ly/۲TWsroN پرده برداشته است که به موجب آن ۶۰ درصد از کارکنان بخش خدمات تا روز ۱۵ اوت به طور کامل واکسینه خواهند شد.
ساکنان مسکو دیگر نیازی به ارائه یک کد QR ندارند که نشان میدهد آنها واکسینه شدهاند یا ایمنی دارند تا از ۱۹ ژوئیه در کافهها، رستورانها و بارها بنشینند. عربستان سعودی
در ماه می، عربستانسعودی تمام کارگران بخش دولتی و خصوصی را که مایل به شرکت در یک محل کار بودند را ملزم به واکسیناسیون کرد، بدون اینکه مشخص کند چه زمانی این کار انجام خواهد شد.
واکسیناسیون همچنین برای ورود به هر گونه موسسه دولتی، خصوصی، یا آموزشی و استفاده از وسایل حمل و نقل عمومی از آغاز ماه اوت الزامی خواهد بود.
شهروندان سعودی پیش از آنکه بتوانند از 9 اوت به خارج از کشور سفر کنند , به دو دوز واکسن کوید19 نیاز خواهند داشت . ترکمنستان
ترکمنستان
وزارت بهداشت ترکمنستان در روز 7 ژوئیه اعلام کرد که واکسیناسیون کوید19 را برای همه ساکنان 18 سال و بالاتر اجباری کردهاست .
۲۲ ژوئیه ۲۰۲۱
پکن (رویترز)واکسن COVID۱۹ با استفاده از اولین مطالعه منتشر شده در مورد اثر آن در برابر نسخه مسری تر، پاسخهای ایمنی ضعیف تری را علیه واریانت دلتا استخراج کرد.
یک مطالعه آزمایشگاهی براساس نمونههای سرمی از افراد سریلانکا نشان داد که آنتی بادی علیه دامنه اتصال به گیرنده ویروس در افرادی که واکسن BBIBP - CorV سینوفارم را دریافت کرده بودند، در برابر واریانت دلتا ۱.۳۸ برابر کاهش یافت در مقابل نسخه قدیمیتر ویروس کرونا که برای اولین بار در ووهان شناسایی شد. این مطالعه که پیش از بررسی دقیق وب سایت مدراکسی منتشر شد، توسط دانشمندان دانشگاه سریلانکا و همچنین شورای شهرداری کلمبو در سریلانکا و دانشگاه آکسفورد در انگلستان انجام شد.
گونه دلتا، که اولین بار در اواخر سال گذشته در هند یافت شد، از آن زمان به گونه غالب ویروس در سراسر جهان تبدیل شدهاست و در پس افزایش اخیر عفونتهای گزارششده در بسیاری از کشورها از جمله بریتانیا، اندونزی، ایالاتمتحده و کرهجنوبی قرار دارد. این بیماری در بیش از ۹۰ کشور جهان شناسایی شدهاست.
این مطالعه نشان داد که واکسن سینوفارم، که رسما گروه دارویی ملی چین است، کاهش ۱۰ برابری را در میانگین هندسی عیار پادتن بر علیه واریانت بتا، که اولین بار در آفریقای جنوبی یافت شد، نشان داد.
محققان گفتند که ۹۵ % از واکسنهای تغییر یافته سرمی، اما تفاوت قابلتوجهی در سطح آنتیبادی دو نوع از سرم خون افراد واکسینه شده در مقایسه با سرم افرادی که به طور طبیعی آلوده شدهبودند، وجود نداشت.
این مقاله گفت: این پیشنهاد میکند که واکسن سینوفارم ممکن است قادر به القای پاسخهای ضد بدن در برابر دو نوع مشابه با میزان مشاهدهشده پس از عفونت طبیعی باشد.
این واکسن دو مرحلهای یکی از پرمصرفترین واکسنهای کوید19 در چین است و سینوفارم موافقت کرد تا 170 میلیون دوز را برای طرح اشتراک گذاری واکسن جهانی COVAX تا اواسط سال 2022 تامین کند .
برچسب های مهم
۲۲ ژوئیه ۲۰۲۱
( رویترز ) براساس مطالعهای که در لنست منتشر شد , در طول 14 ماه اول این بیماری همهگیر , حدود 1.5 میلیون کودک در سراسر جهان مرگ یک پدر و مادر , پدر بزرگ تحت سرپرستی , یا بستگان دیگری که از آنها مراقبت میکردند را در نتیجه کوید19 تجربه کردند .
برآوردهای یتیمخانه از دادههای مرگ و میر 21 کشور گرفته شدهاست که 77 % مرگ و میر کوید19 جهانی و از بخش جمعیت سازمان ملل متحد را شامل میشود .
دکتر سوزان هیلیس از مراکز ایالاتمتحده میگوید : " برای هر دو مرگ کوید19 در سراسر جهان , یک کودک به حال خود رها میشود تا با مرگ پدر یا مادر خود روبرو شود . " تیم واکنش کنترل و پیشگیری از بیماری کوید19 که رهبری این مطالعه را بر عهده داشت , در بیانیهای گفت . وی افزود که شمار یتیمان کوید19 با پیشرفت بیماری همهگیر افزایش خواهد یافت .
هیلیس گفت: "نیاز فوری به اولویتبندی این کودکان و" حمایت از آنها برای سالها در آینده " وجود دارد.
لوسی کلوور از دانشگاه آکسفورد، یکی از نویسندگان این مقاله میگوید: " و ما باید به سرعت پاسخ دهیم زیرا هر ۱۲ ثانیه یک کودک مراقب خود را به COVID۱۹ از دست میدهد."
۲۲ ژوئیه ۲۰۲۱
یکی از پزشکان گفت که با افزایش تعداد بیماران بستری در بیمارستان کوید19 در نواحی با نرخ پایین واکسیناسیون , بیماران خواهان واکسن هستند , اما اغلب " خیلی دیر " است . برای مثال، در مرکز پزشکی گراندد ویو در بیرمنگام آلاباما، پزشکان در حال درمان بیماران جوان و در غیر این صورت سالم هستند که عفونت کرونا ویروس جدی گرفتهاند.
" یکی از آخرین کارهایی که آنها قبل از لولهگذاری انجام میدهند التماس کردن به من برای واکسن است."
او نوشت: " من دست آنها را میگیرم و به آنها میگویم که متاسفم، اما خیلی دیر شدهاست." " چند روز بعد، وقتی من زمان مرگ را فرا میخوانم، اعضای خانواده آنها را در آغوش میگیرم و به آنها میگویم بهترین راه برای افتخار به عزیزانشان این است که واکسینه شوید و هر کسی را که آنها میدانند تشویق کنید که همان کار را انجام دهد."
او نوشت که اعضای خانواده سپس گریه میکنند و اغلب میگویند که "نمیدانستند"، آنها فکر میکردند که این یک حقه است "و فکر میکردند که ویروس کرونا" فقط آنفولانزا است." و آرزو میکردند که بتوانند برگردند. اما نمیتوانند." " بنابراین، آنها از من تشکر میکنند، و میروند تا واکسن را دریافت کنند. و من به دفترم بر میگردم , یادداشت مرگ آنها را مینویسم , و یک دعای کوچک میکنم که این تلفات جان افراد بیشتری را نجات خواهد داد . " طبق گزارش اسوشیتد پرس , موارد کوید19 در طی دو هفته گذشته در ایالاتمتحده سه برابر شدهاند , و بیمارستان کوید19 دوباره شروع به فشار آوردن بر سیستم مراقبتهای بهداشتی کردهاست . اعضای ستاد، از جمله پزشکان و روحانیون، احساس بازگشت به سختترین ماههای این بیماری همهگیر را دارند. چاد نیلسن، مدیر پیشگیری از عفونت در UF Health Jacksonville در فلوریدا، به آسوشیتد پرس گفت: " کارکنان ما ناامید شدهاند."
این بیمارستان با افزایش تعداد بیماران کوید19 , اعمال جراحی و رویههای انتخابی را لغو میکند . نیلسن گفت: " آنها خسته هستند." "آنها فکر میکنند که این دوباره" دجا وو " است، و کمی خشم وجود دارد زیرا میدانیم که این وضعیت تا حد زیادی قابل پیشگیری است، و مردم از این واکسن سو استفاده نمیکنند."