
امروز پنجشنبه ۲۰ اردیبهشت ۱۴۰۳
دسته بندی سایت
برچسب های مهم
پیوند ها
آمار بازدید سایت
تفسیر و شناسایی سریع رشد باکتریایی بر روی محیط کشت اولیه
تفسیر اولیه رشد باکتری در محیط کشت اولیه، که معمولا از ۲۴ تا ۴۸ ساعت اول انکوباسیون پیروی میکند، فرصتی برای تکنولوژیست آزمایشگاه پزشکی یا میکروبیولوژیست بالینی است تا یک شناسایی اولیه انجام دهد و تصمیم بگیرد که چه تستها و روشهای اضافی باید برای رسیدن به یک شناسایی قطعی انجام شوند. بسیاری از جداول این روش برای آموزش کارکنان مفید هستند، اما نیازی نیست که آنها بخشی از راهنمای روی میز برای استفاده روزانه باشند.
اگر چه در حال حاضر برای شناسایی سریع طیف وسیعی از باکتریهای هوازی و بیهوازی در آزمایشگاههای بالینی سراسر جهان از matrix-assisted laser desorption ionization–time of flight mass spectrometry استفاده میشود، شناسایی طیفسنجی جرمی همچنان باید با ارتباط دادن مورفولوژی کلنی با ظاهر شدن رنگآمیزی گرم ارگانیسم و انجام برخی آزمونهای فنوتیپی سریع همانطور که در این روش ذکر شدهاست، تایید شود.
. بررسی اولیه پلیت های اولیه
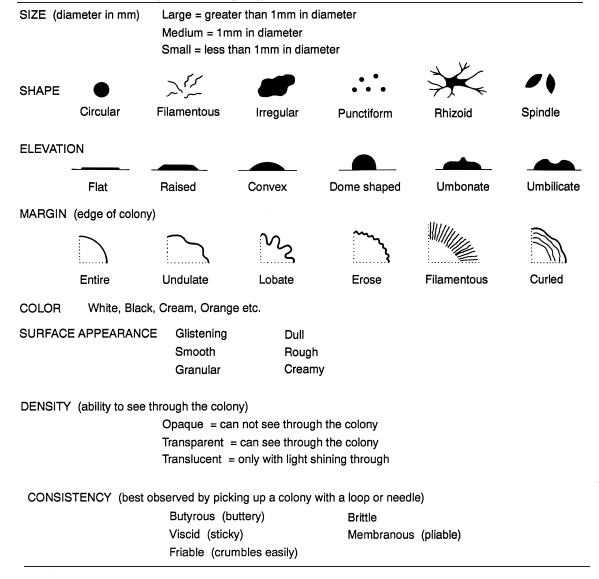
مورفولوژی کلونی را برای هر محیط کشت آگار توصیف کنید
به انواع مختلف کلونی ها در هر پلیت آگار توجه کنید.
)هنگام انجام این ارزیابیهای اولیه، به پلیت های کشت از زوایای مختلف نگاه کرده و از روشنایی مستقیم استفاده کنید
از یک نور با یک لنز ذرهبین برای مشاهده کلونی های کند رشد یا بسیار کوچک استفاده کنید، که اغلب بین کلونی های بسیار بزرگتر به سرعت در حال رشد پنهان میشوند
ب مورفولوژی کلنی های ناخالص هر نوع کلونی را توصیف کنید

باکتری ها میکروارگانیسم های پروکاریوتی و تک سلولی هستند که فاقد رنگدانه های کلروفیل هستند. ساختار سلولی ساده تر از سایر موجودات است زیرا هیچ اندامک متصل به هسته یا غشاء وجود ندارد.
به دلیل وجود دیواره سلولی سفت و سخت، باکتری ها شکل مشخصی را حفظ می کنند، اگرچه از نظر شکل، اندازه و ساختار متفاوت هستند
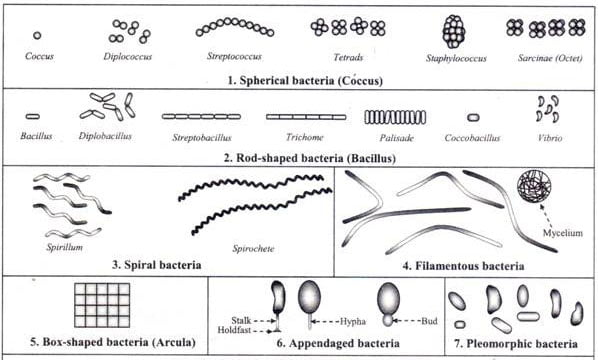
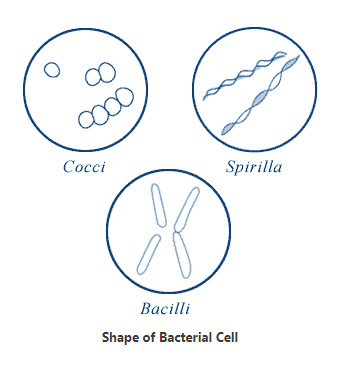
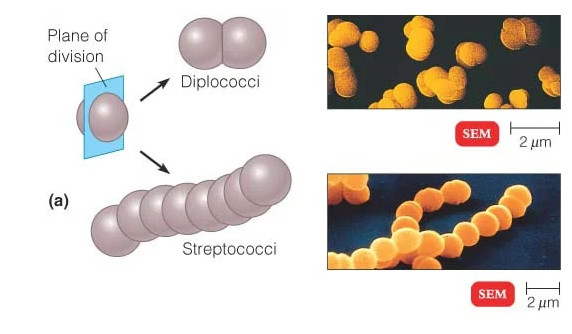
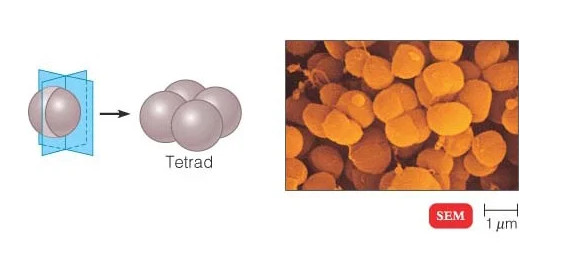
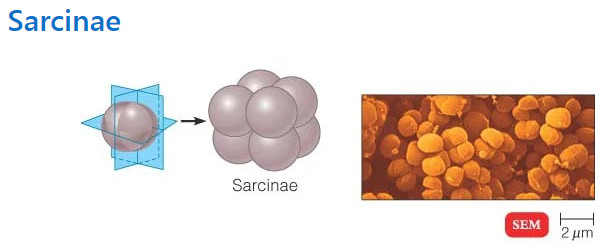
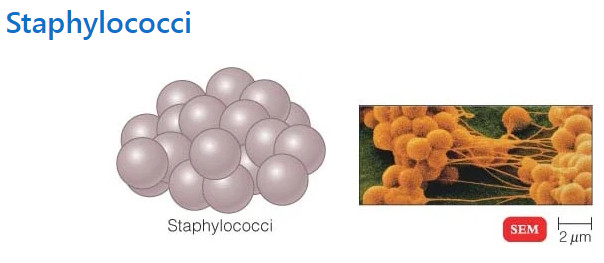
هنگامی که زیر میکروسکوپ نوری مشاهده می شود، بیشتر باکتری ها به سه شکل اصلی ظاهر می شوند: میله ای (باسیلوس)، کره ای (کوکوس) و نوع مارپیچی (ویبریو). در واقع ساختار باکتری ها دارای دو جنبه آرایش و شکل است. تا آنجا که به ترتیب مربوط می شود، ممکن است خوشه های جفتی (diplo)، خوشه های انگور مانند (staphylo) یا زنجیره ای (strepto) باشند. از نظر شکل ممکن است عمدتاً میله ها (باسیل ها)، گرد (کوکسی ها) و اسپیرال ها (مارپیچی) باشند

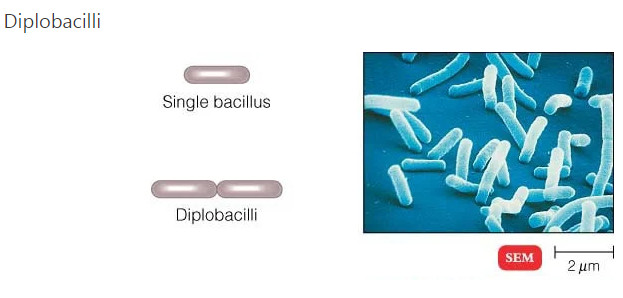
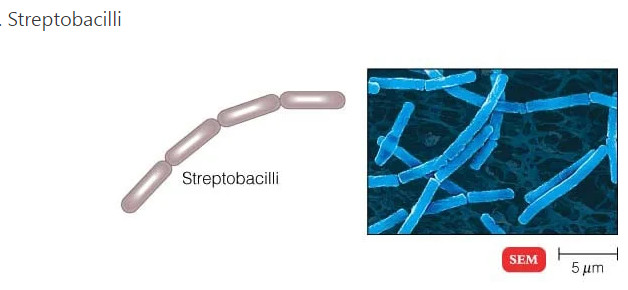
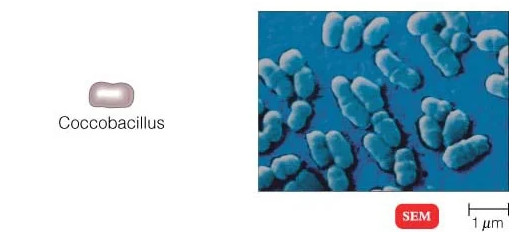
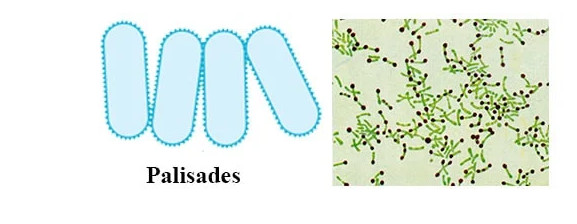
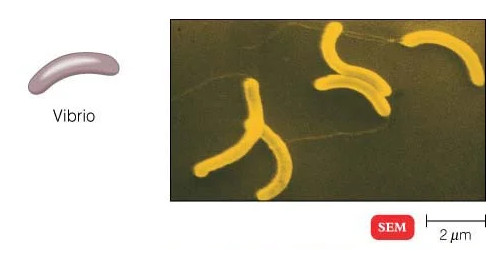
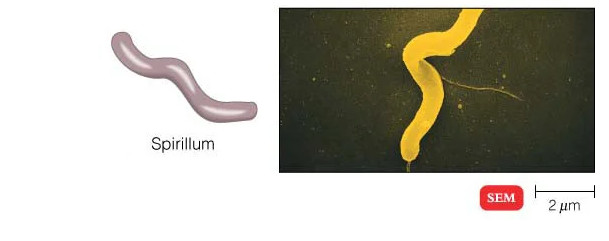
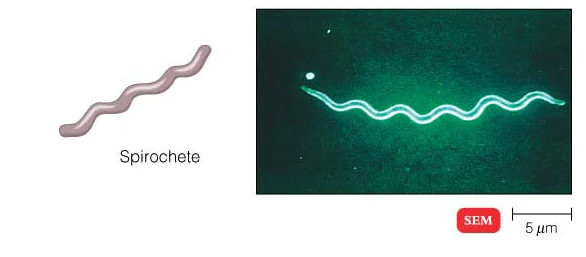
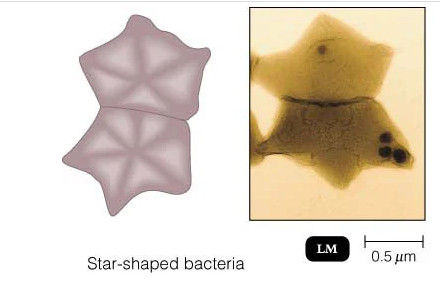
واژینوز باکتریایی چیست؟
حقایقی که هر زنی باید بداند
واژینوز باکتریایی (BV) یک بیماری شایع اما خسته کننده است که در آن تعادل باکتری ها در واژن از همگامی خارج می شود. معمولاً بدن قادر است تعادل ایده آل را حفظ کند. اما اگر تعادل مختل شود، انواع خاصی از باکتری ها می توانند بیش از حد رشد کنند و علائم ایجاد کنند.
BV به راحتی درمان می شود و معمولاً هیچ مشکل دیگری برای سلامتی ایجاد نمی کند. با این گفته، می تواند خطر ابتلا به یک بیماری مقاربتی (STD) را افزایش دهد یا منجر به عوارض زایمان در افراد باردار شود
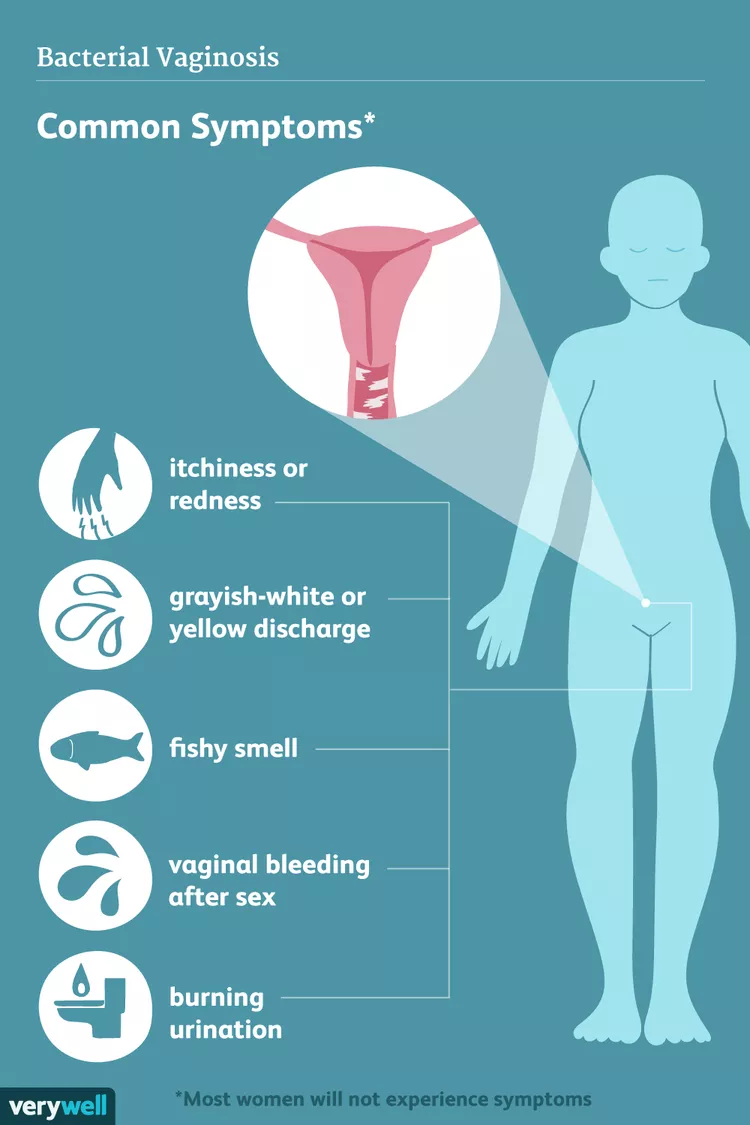
علائم واژینوز باکتریایی
از 21 میلیون زن در ایالات متحده که تصور می شود سالانه به واژینوز باکتریایی مبتلا هستند، تنها حدود سه میلیون نفر در واقع علائم دارند منبع
هنگامی که آنها رخ می دهند، علائم BV خفیف اما پایدار هستند و ممکن است شامل موارد زیر باشد:
ترشحات واژن به رنگ خاکستری مایل به سفید یا زرد
بوی "ماهی" که می تواند پس از مقاربت بدتر شود
احساس سوزش هنگام ادرار کردن
خارش واژن، قرمزی و تورم
خونریزی واژن بعد از مقاربت
در حالی که علائم BV به ندرت جدی هستند، می توانند بافت های واژن را ضعیف کرده و خطر ابتلا به بیماری های مقاربتی مانند سوزاک، کلامیدیا، تریکومونیازیس و HIV را افزایش دهند.
اگر عفونت در دوران بارداری رخ دهد، خطر زایمان زودرس (نارس)، وزن کم هنگام تولد، و در موارد نادر، سقط جنین افزایش می یابد
علل
واژینوز باکتریایی زمانی رخ می دهد که سطح باکتری های "خوب" در واژن به طور ناگهانی کاهش یابد. این به باکتری های "بد" اجازه می دهد تا بیش از حد رشد کنند. باکتری "خوب" اصلی به نام لاکتوباسیلوس، واژن را کمی اسیدی می کند تا باکتری های "بد" نتوانند بیش از حد رشد کنند.
رابطه جنسی می تواند با وارد کردن مقادیر جدید یا بیش از حد باکتری به واژن باعث تحریک BV شود.
برخی از علل شایع تر BV عبارتند از: 3
رابطه جنسی بدون کاندوم
شرکای جنسی متعدد
شرکای جنسی جدید
دیلدو های جنسی مشترک
دوش کردن
حمام های حباب دار (حاوب کف در سطح آب)
دئودورانت های واژن
سیگار کشیدن
دستگاه های داخل رحمی (IUD)
تشخیص
از آنجایی که واژینوز باکتریایی تنها توسط یک عامل ایجاد نمی شود، تشخیص تا حد زیادی بر اساس بررسی تاریخچه پزشکی و علائم همراه با آزمایش ها و روش های مختلف آزمایشگاهی است.
این موارد عبارتند از:: 5
معاینه لگن
آزمایش pH برای بررسی اسیدیته واژن
ارزیابی میکروسکوپی مایعات واژن
معاینه میکروسکوپی به دنبال "سلول های کلو" (به معنی سلول های واژن پر از باکتری است) می شود. از رنگ آمیزی گرم نیز برای تمایز باکتری های "خوب" از "بد" استفاده می شود و به آزمایشگاه اجازه می دهد تا عدم تعادل در فلور واژن را بررسی کند.
ممکن است آزمایشهای اضافی برای رد سایر علل احتمالی مانند عفونت مخمری یا تبخال تناسلی انجام شود
درمان
درمان استاندارد واژینوز باکتریایی یک دوره کوتاه داروهای آنتی بیوتیکی است. آنتی بیوتیک ها دسته ای از داروها هستند که به طور خاص عفونت های باکتریایی را درمان می کنند.
گزینه های خط اول فلاژیل (مترونیدازول) و کلیندامایسین هستند. هر دو در درمان BV بسیار موثر هستند و عوارض جانبی نسبتاً خفیفی دارند.
رژیم های ترجیحی خط اول عبارتند از:
مترونیدازول 500 میلی گرم (میلی گرم) خوراکی دو بار در روز به مدت هفت روز
ژل واژینال مترونیدازول 0.75% یک بار در روز به مدت پنج روز استفاده می شود
کرم واژینال کلیندامایسین 2.0% قبل از خواب به مدت هفت روز استفاده می شود
درمانهای جایگزین عبارتند از شیاف واژینال کلیندامایسین یا قرص تینداماکس (تینیدازول).
عوارض جانبی شامل حالت تهوع، معده درد، سرفه، گلودرد، آبریزش بینی و طعم فلزی در دهان است.
علاوه بر آنتی بیوتیک ها، چندین درمان حمایتی ممکن است کمک کننده باشد. اینها شامل پروبیوتیک ها (باکتری های زنده مفید موجود در ماست و مکمل های پروبیوتیک) است که ممکن است به جلوگیری از عود کمک کند. اسید بوریک (موجود به صورت کپسول و شیاف واژینال) یک داروی قدیمی است که توجه پزشکی را به خود جلب می کند.
در طول درمان، شلوار یا دامن گشادتر بپوشید تا رطوبت و گرمای واژن را کاهش دهید که میتواند رشد باکتریها را افزایش دهد. همچنین می توانید خارش و تورم را با استفاده از یک پارچه خنک روی واژن یا پاشیدن آب سرد به آن کاهش دهید
جلوگیری
به همان اندازه که واژینوز باکتریایی رایج است، کارهایی وجود دارد که می توانید برای کاهش خطر انجام دهید. اینها شامل اقدامات جنسی ایمن و رعایت بهداشت واژن می باشد
برای جلوگیری از واژینوز باکتریایی:
تعداد شرکای جنسی را محدود کنید.
از کاندوم به طور صحیح و مداوم استفاده کنید.
دوش نگیرید.
از حمام های حباب دار و دئودورانت های واژن خودداری کنید.
بعد از ادرار کردن از جلو به عقب پاک کنید.
اگر BV مکرر دارید یا در گذشته BV شدید داشته اید از IUD اجتناب کنید.
برچسب های مهم
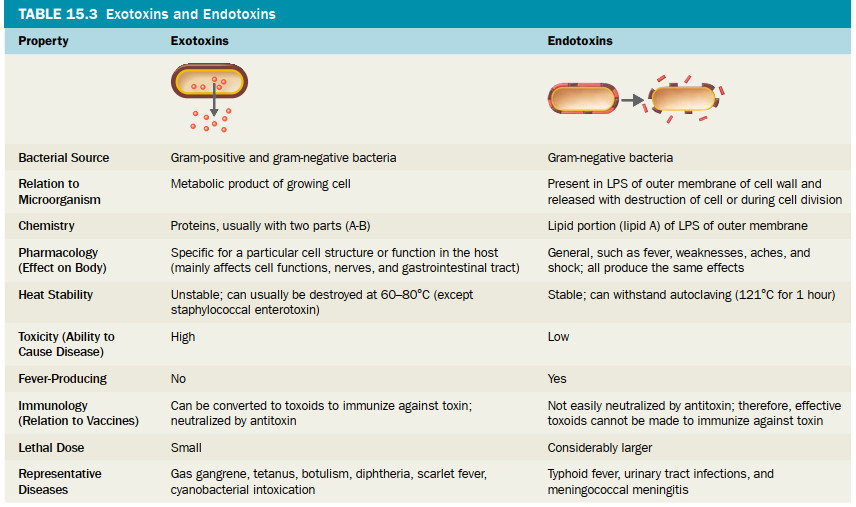
بیماریزایی توانایی ایجاد بیماری با غلبه بر دفاع میزبان است، در حالی که حدت درجه بیماری زایی است. برای ایجاد بیماری، بیشتر پاتوژنها باید به میزبان دسترسی پیدا کنند، به بافتهای میزبان بچسبند، به دفاع میزبان نفوذ کنند یا از آنها فرار کنند و به بافتهای میزبان آسیب برسانند. با این حال، برخی از میکروب ها با آسیب مستقیم به بافت میزبان باعث بیماری نمی شوند. در عوض، بیماری به دلیل تجمع مواد زائد میکروبی است. برخی از میکروب ها، مانند میکروب هایی که باعث پوسیدگی دندان و آکنه می شوند، می توانند بدون نفوذ به بدن باعث بیماری شوند. پاتوژن ها می توانند از طریق چندین راه به بدن انسان و سایر میزبان ها وارد شوند که به آنها دریچه های ورود می گویند ...
بخش های از فصل
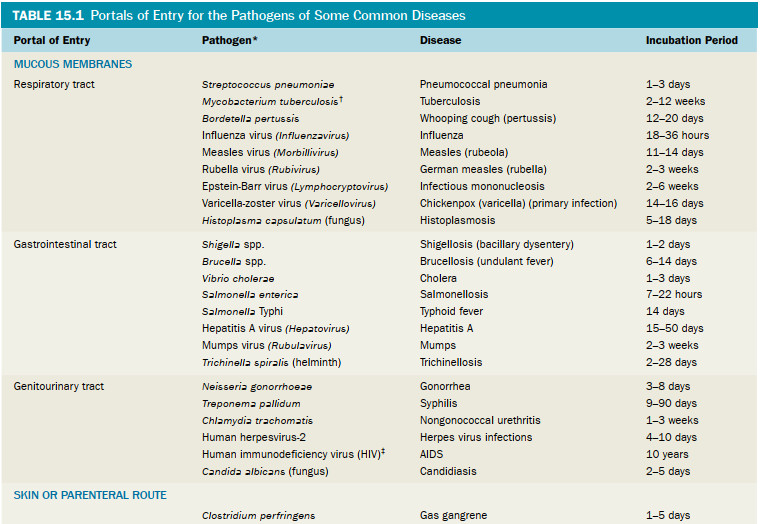
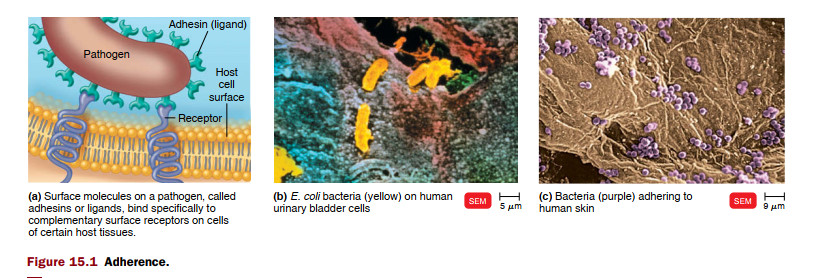
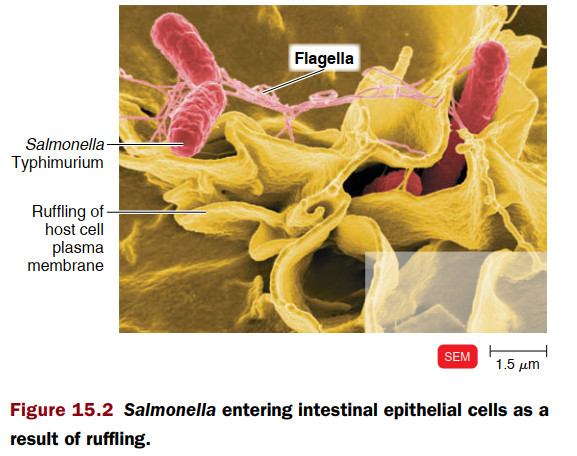
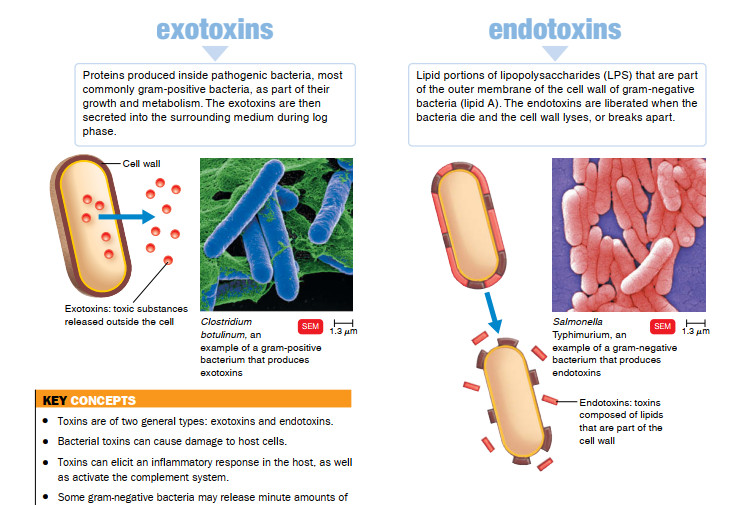
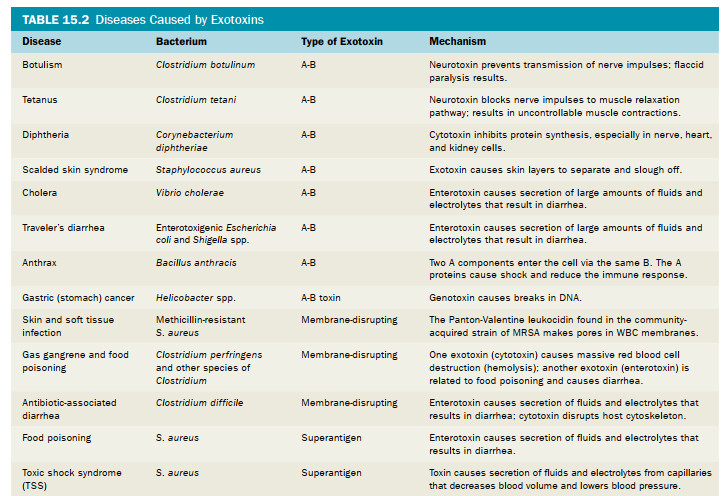
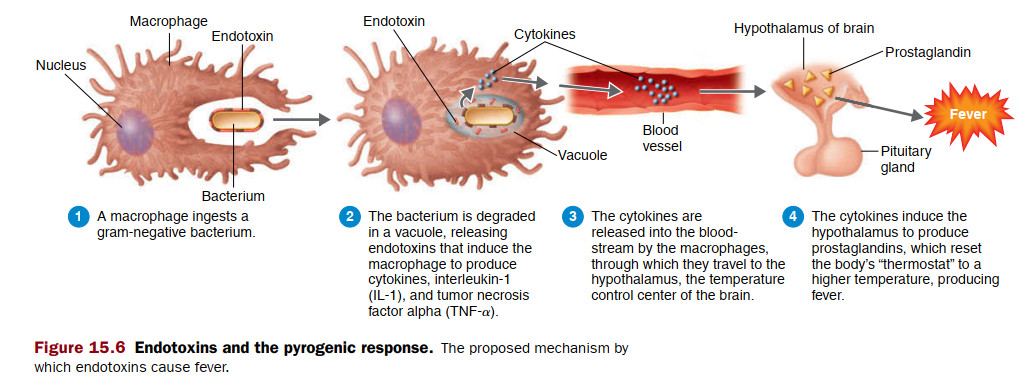
بیماری به هر شرایطی گفته می شود که در آن ساختار یا عملکرد طبیعی بدن آسیب ببیند یا مختل شود.
صدمات یا ناتوانیهای جسمی به عنوان بیماری طبقهبندی نمیشوند، اما میتواند دلایل مختلفی برای بیماری وجود داشته باشد، از جمله عفونت توسط یک پاتوژن، ژنتیک (مانند بسیاری از سرطانها یا کمبودها)، علل محیطی غیرعفونی، یا پاسخهای ایمنی نامناسب. تمرکز ما در این فصل بر روی بیماریهای عفونی خواهد بود، اگرچه هنگام تشخیص بیماریهای عفونی، همیشه در نظر گرفتن علل غیرعفونی احتمالی مهم است.
علائم و نشانه های بیماری عفونت عبارت است از کلونیزاسیون موفق میزبان توسط یک میکروارگانیسم. عفونتها میتوانند منجر به بیماری شوند که باعث ایجاد علائم و نشانههایی میشود که منجر به انحراف از ساختار یا عملکرد طبیعی میزبان میشود.
میکروارگانیسم هایی که می توانند باعث بیماری شوند به عنوان پاتوژن شناخته می شوند .....

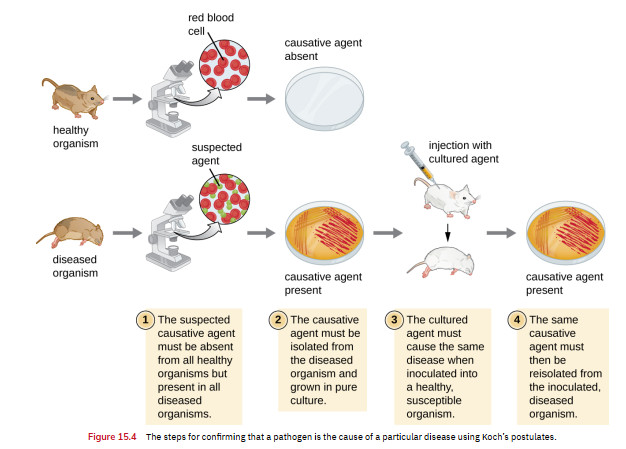
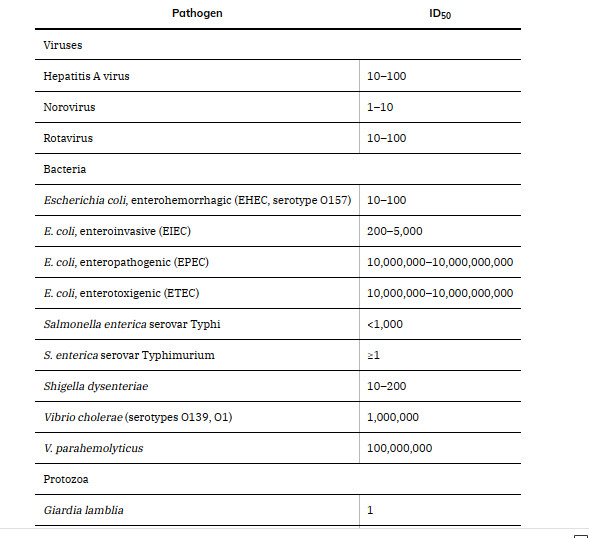
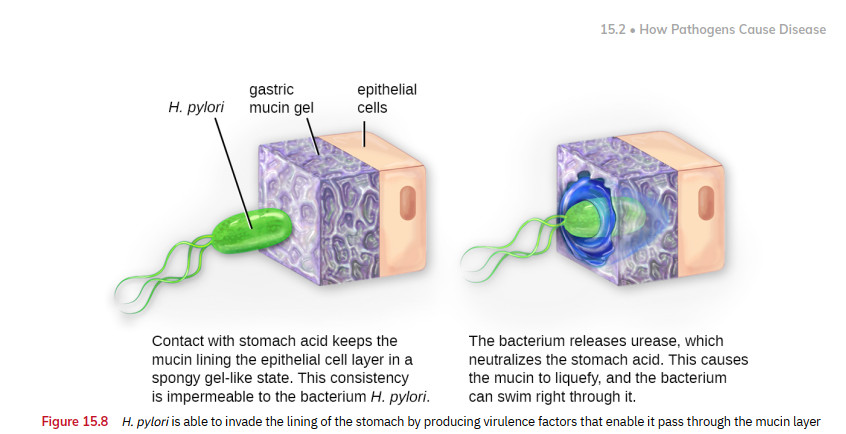
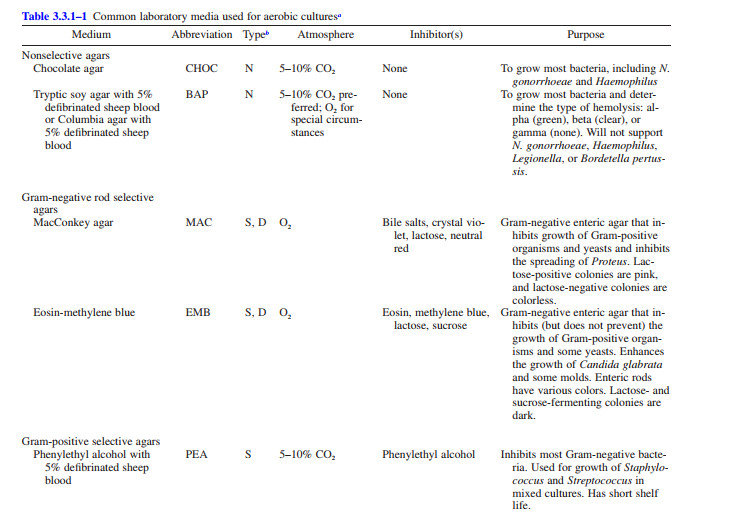
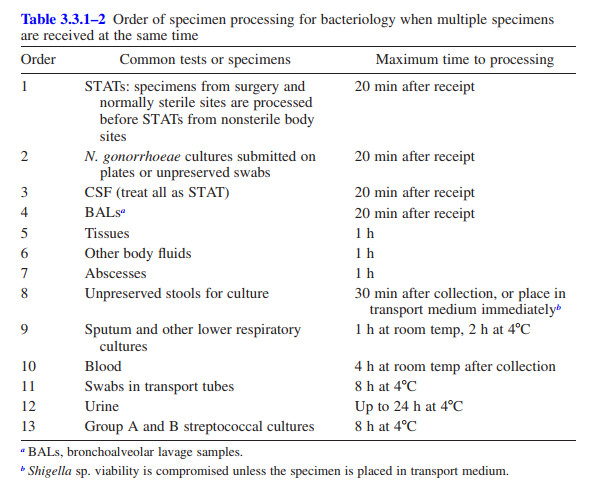
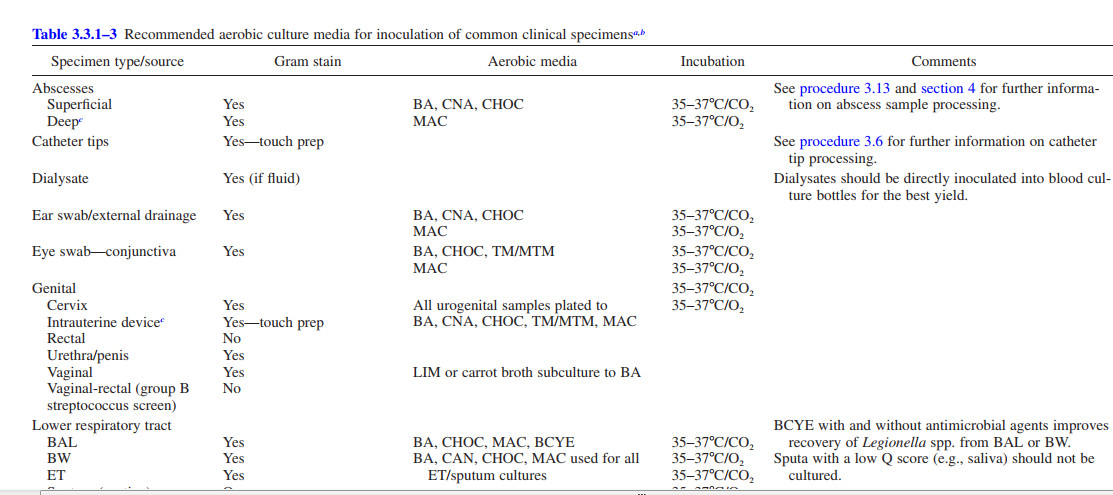
پردازش اولیه نمونه های بالینی برای باکتری شناسی یک تلاش چند وجهی است که شامل تعدادی مراحل تصمیم گیری می شود، از جمله نیاز به پردازش نمونه برای باکتری شناسی بی هوازی، قارچ شناسی، ویروس شناسی و انگل شناسی، بسته به ماهیت نمونه (1). نیاز به آزمایش های مستقیم مانندرنگ آمیزی گرم نیز باید در نظر گرفته شود......
بخش های از فصل کتاب
تحقیقات نشان میدهد میگرن و سردردهای خوشهای با ساعت درونی بدن مرتبط هستند
محققان دریافتند برخی از انواع سردرد بیشتر در زمانهای خاصی از روز و همچنین زمانهای خاصی از سال رخ میدهند
سردرد خوشه ای نوع نادری از سردرد است که باعث ایجاد درد شدید در اطراف چشم می شود. هر انفجار حدود 15 دقیقه طول می کشد، اما یک حمله می تواند بین یک تا سه ساعت طول بکشد. این بیماری در مردان شایع تر از زنان است. برعکس در مورد میگرن صادق است، یک وضعیت سردرد شدید که در زنان سه برابر بیشتر از مردان است.
و در حالی که سردردهای خوشه ای معمولاً در طول شب اتفاق می افتد، میگرن معمولاً در طول روز بروز می کند، متاآنالیز نشان داد.
این متاآنالیز شامل 72 مطالعه در مورد اینکه چگونه به نظر می رسد ریتم شبانه روزی - ساعت داخلی بدن - در هر یک از اختلالات سردرد دخالت دارد، که روی هم بر بیش از 40 میلیون نفر در ایالات متحده تأثیر می گذارد، بود
این مطالعات شامل دادههایی در مورد زمان یا زمان از سال بود که فرد دچار سردرد میشود و اینکه آیا سردرد دقیقاً قبل، در حین یا بلافاصله بعد از خواب ایجاد میشود یا خیر. برخی از مطالعات همچنین شامل تحقیق در مورد اینکه آیا ژنهای خاص مرتبط با ریتم شبانهروزی در افرادی که این نوع سردردها را دارند، شایعتر است یا خیر. یک مطالعه آنالیز ژنتیکی بود که در پستانداران غیرانسانی انجام شد، اما بقیه بر اساس انسان بودند
نتایج روز چهارشنبه در Neurology، مجله پزشکی آکادمی نورولوژی آمریکا منتشر شد.
محققان دریافتند سردردهای خوشه ای با چرخه های شبانه روزی، به ویژه در طول تغییرات فصل در بهار و پاییز، ارتباط نزدیکی دارد. بیش از 70 درصد از افرادی که در 16 مطالعه روی سردردهای خوشه ای شرکت کردند، حملات بیشتری را در این فصول گزارش کردند و گفتند که معمولاً بین ساعات پایانی شب و ساعات اولیه صبح رخ می دهد.
وقتی صحبت از استعداد ژنتیکی شد، مطالعات نشان داد که پنج ژن از 9 ژن مرتبط با سردردهای خوشه ای در تنظیم ریتم شبانه روزی نیز نقش دارند.
چیزی که برای محققان تعجب آور بود این بود که نیمی از سردردهای میگرنی در هشت مطالعه با جزر و مدهای واضح در طول روز و همچنین سال مرتبط بودند. اکثر مردم در طول صبح، روز یا عصر میگرن داشتند و از ساعت 11 شب یک افت شدید در سردرد مشاهده می شد. تا ساعت 7 صبح، آنها همچنین میگرن بیشتر یا بدتری را بین آوریل و اکتبر گزارش کردند.
بسیاری از ژن ها با خطر ابتلا به میگرن مرتبط هستند و این مطالعه نشان داد که 110 مورد از این ژن ها نیز با ریتم شبانه روزی مرتبط هستند.
بوریش گفت که درک ارتباط بین ریتم شبانه روزی و این اختلالات سردرد می تواند به درمان های بهتر منجر شود.
او گفت: «داروهایی که چرخه شبانه روزی را هدف قرار می دهند ممکن است نوع جدیدی از درمان باشد که ما می توانیم به این بیماران ارائه دهیم.
پیوند هورمونی
علاوه بر ریتم شبانه روزی، متاآنالیز دو هورمون را نیز به صفر رساند: کورتیزول و ملاتونین.
دکتر نارایان کیسون، متخصص مغز و اعصاب در کلینیک مایو در روچستر، مینهسوتا، که متخصص در پزشکی سردرد است و در تحقیقات جدید نقشی نداشت، گفت: «ریتمهای شبانهروزی توسط هورمونها هدایت میشوند.
هیپوتالاموس - ناحیه ای از مغز که در درجه اول ساعت بیولوژیکی را کنترل می کند - با غدد تولید کننده ملاتونین، که سیگنال زمان خواب است، و کورتیزول، نشانه بدن که باید بیدار باشد، مرتبط است.
متاآنالیز نشان داد که افرادی که به میگرن مبتلا میشوند، معمولاً نسبت به افرادی که این سردردها را ندارند، ملاتونین کمتری تولید میکنند و در طول حمله حتی کمتر تولید میکنند. افراد مبتلا به سردردهای خوشه ای هم سطح کورتیزول بالاتر و هم سطح ملاتونین پایین تری داشتند.
بوریش گفت که کمبود خواب باعث افزایش سطح کورتیزول می شود، اگرچه او اشاره کرد که به نظر می رسد ارتباط بین سطح ملاتونین و اختلالات سردرد بسیار واضح تر از ارتباط بالقوه کورتیزول است.
این اختلالات سردرد نه تنها تحت تأثیر خواب قرار می گیرند، بلکه برعکس، اختلالات زیادی در خواب نیز ایجاد می کنند. دکتر اندرو چارلز، مدیر برنامه میگرن گلدبرگ UCLA که در مطالعه جدید شرکت نداشت، گفت: آنها ممکن است هر مکانیزم شبانه روزی را که هستند بازخورد داده و تقویت کنند. دشوار است که بدانیم آیا تأثیر کورتیزول به ریتمهای شبانهروزی مرتبط است یا چیزی مرتبط با پاسخ استرس.»
کیسون از کلینیک مایو گفت، در حالی که چرخه های شبانه روزی به وضوح با سردردهای خوشه ای مرتبط است، میگرن وضعیت بسیار پیچیده تری برای طبقه بندی است.
وی با اشاره به وضعیت تعادل در بدن افزود: «عوامل زیادی در میگرن نقش دارند، اما یک چیزی که اغلب مییابیم این است که چیزهایی که باعث تغییر در هموستاز میشوند، تأثیر عمدهای بر خطر ابتلا به میگرن دارند.» این شامل استرس است که باعث افزایش سطح کورتیزول می شود.
سیگار کشیدن، رژیم غذایی، ژنتیک غیرمرتبط با ریتم شبانه روزی، و میزان ورزش یک فرد نیز عواملی هستند که می توانند بر میگرن تأثیر بگذارند، اما به گفته کارشناسان، تحقیقات جدید سرنخ مهمی را ارائه می دهد که می تواند به درمان های بهتر برای برخی افراد منجر شود.
کیسون گفت: «ریتمهای شبانهروزی و تأثیر آن بر میگرن اغلب نادیده گرفته میشوند. "در حالی که میگرن یک اختلال پیچیده است، این بخشی از پازل است که از کاوش بیشتر در مورد روش هایی که می توانیم هم میگرن و هم سردرد خوشه ای را بهتر درمان کنیم، سود می برد."
https://www.nbcnews.com/health/health-news/migraines-cluster-headaches-are-linked-bodys-internal-clock-science-sh-rcna76744
برچسب های مهم
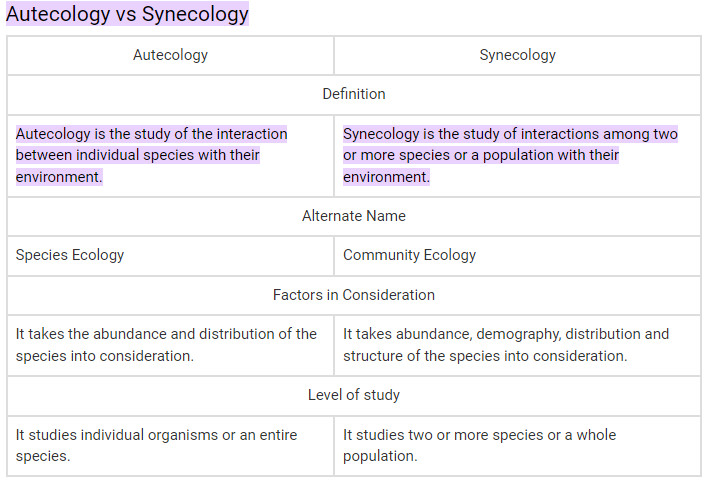
اوتکولوژی چیست؟
اوتکولوژی به مطالعه برهمکنش موجودات با محیط اطرافشان می پردازد تا توزیع و فراوانی آنها را توضیح دهد. این با synecology متفاوت است زیرا ترجیح می دهد سازگاری گونه های خاص گیاهان و حیوانات را مطالعه کند
سینکولوژی چیست؟
سینکولوژی که به عنوان اکولوژی جامعه نیز شناخته می شود، مطالعه تعامل بین گونه ها با در نظر گرفتن عوامل زیادی مانند توزیع، فراوانی، ساختار، جمعیت شناسی و تعاملات موجود بین گونه ها است. این به مطالعه برهمکنش های یک جمعیت بر اساس ویژگی های فنوتیپی و ژنوتیپی آن می پردازد
Autecology در مقابل Synecology
Autecology مطالعه تعامل بین گونه های فردی با محیط خود است. Synecology مطالعه تعاملات بین دو یا چند گونه یا یک جمعیت با محیط خود است
کاربردهای بالقوه باکتریوسین ها در علوم غذایی، داروسازی و پزشکی بالینی
امروزه باکتریها به طور گسترده در علوم غذایی به منظور افزایش طول عمر نگهداری غذا مورد استفاده قرار میگیرند، که مانع از عفونت پاتوژن در بیماریهای حیوانی میشود ، و صنعت داروسازی و جامعه پزشکی برای درمان سرطانهای بدخیم (شکل ۲)
اولین باکتریوسین توسط گراتیا (۱۹۲۵)کشف شد و در سالهای اخیر بسیاری از باکتریوسین ها به طور موفقیت آمیزی توسط دانشمندان شناسایی شدند. باکتریوسین ها به عنوان یک محصول طبیعی در نظر گرفته میشوند زیرا آنها پپتیدها یا پروتئینهایی هستند که توسط باکتریهای حاضر در بسیاری از غذاهای تخمیری یا غیر تخمیری از زمانهای قدیم تولید میشوند.
برچسب های مهم
وقتی کولیسینها وارد سلول هدف میشوند، میتوانند براساس مکانیزمهای باکتریسیدال به سه دسته تقسیم شوند:
(۱)کولیسینهای نوع Pore: تشکیل منافذ یا کانالها در غشای داخلی باعث نشت ترکیبات سیتوپلاسمی، تخریب گرادیان الکتروشیمیایی، از دست دادن یون و مرگ سلول میشوند. این ترکیبات شامل کولیسین A، B، E۱، Ia، Ib، K و N؛
(۲)کولیسینهای نوع نوکلئاز: کولیسینهای حاوی DNase، ۱۶ S rRNase، و tRNase برای هضم غیر اختصاصی DNA و RNA باکتری. اینها شامل کولیسین E۲ تا E۹ هستند.
(۳)کولیسین های نوع پپتیدوگلیکاناز: این پروتئینها میتوانند پیشساز پپتیدوگلیکان را هضم کنند، که منجر به ناتوانی در سنتز پپتیدوگلیکان و مرگ باکتری میشود.
میکروسین Microcins
میکروسین ها پپتیدهای ضد میکروبی آبگریز سنتز شده ریبوزومی با وزن مولکولی کم (۱۰ کیلو دالتون)هستند که توسط پروتئین کولیسینهای با وزن مولکولی بالا ۲۵ - ۸۰ کیلو دالتون تشخیص داده میشوند. میکروسین ها به عنوان پپتیدهای اولیه تولید میشوند، از جمله پپتید رهبر N - ترمینال و پپتیدهای هسته. پپتیدهای پیشساز میکروسین ممکن است در طی بلوغ به یک میکروسین فعال، تحت یک فرآیند اصلاح پس از ترجمه قرار گیرند یا نگیرند. میکروسین ها عمدتا توسط انتروباکتریاسه تولید میشوند که مقاومت زیادی نسبت به گرما، pH شدید و پروتئازها نشان میدهند. مکانیسمهای باکتریسیدال میکروسینها متنوع هستند، از جمله نوع تشکیل حفره، نوع نوکلئاز، مانند عملکردهای DNase و RNase، و بازدارندههای سنتز پروتئین یا تکثیر DNA. هیچ ژن میکروسین ژن لیز کننده مربوطه ندارد و میکروسین ها در خارج از باکتریها از طریق سیستم ترشح انتقالدهنده نوع ۱ ABC (کاست متصل شونده به ATP)ترشح میشوند که از تعدادی پروتئین تشکیل شدهاست.
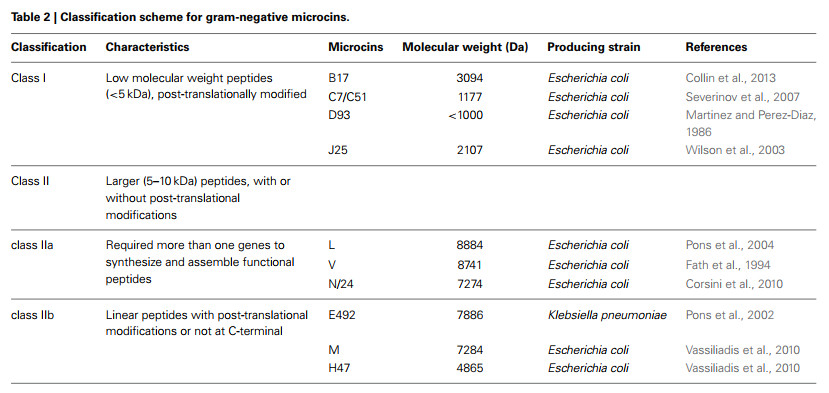
میکروسین ها براساس جرم مولکولی، پیوندهای دی سولفیدی در ساختار و تغییرات پس از ترجمه به دو دسته تقسیم میشوند. میکروسینهای کلاس I، مانند میکروسین B۱۷، C۷ - C۵۱، D۹۳ و J۲۵ از پپتیدهای تغییر یافته پس از ترجمه با وزن مولکولی پایین (۵ کیلو دالتون)هستند. وزن مولکولی میکروسینهای کلاس II بزرگتر (۵ - ۱۰ کیلو دالتون)از وزن مولکولی میکروسینهای کلاس I هستند. میکروسینهای کلاس II را میتوان به دو زیر کلاس، شامل کلاس IIa و IIb، تقسیم کرد. میکروسین های کلاس IIa، مانند میکروسین L، V و N به سه ژن مختلف برای سنتز و تجمع پپتیدهای کاربردی نیاز دارند. میکروسینهای کلاس IIb، مانند میکروسین E۴۹۲، M و H۴۷، پپتیدهای خطی با یا بدون تغییرات پس از ترجمه در پایانه C هستند.
جدول ۲ | طرح طبقهبندی برای میکروسینهای گرم منفی.
باکتریوسین های باکتری های گرم مثبت
بر خلاف کولیسینهای باکتریهای گرم منفی، که پروتئینهای پلاسمید یا کروموزومی کد کننده ۲۵ - ۸۰ کیلو دالتون هستند، باکتریوسین های گرم مثبت خصوصیات مشابهی با میکروسین ها دارند. این باکتریوسین های کد شده توسط ژن، پپتیدهای ضد میکروبی با وزن مولکولی پایین با کمتر از ۶۰ آمینو اسید هستند. در باکتریهای گرم مثبت، باکتریهای اسید لاکتیک، باکتریهای معمول هستند که انواع مختلفی از باکتریوسین ها را در اندازهها، ساختارها، خواص فیزیکوشیمیایی و طیف بازدارندگی مختلف تولید میکنند. به دلیل تنوع زیاد باکتریوسین ها، برخی از تحقیقات روشهای مختلفی را برای طبقهبندی باکتریوسین ها از باکتریهای گرم مثبت نشان میدهند.
باکتریوسین های گرم مثبت معمولا به کلاس I (پپتیدهای تغییر یافته، لنتیبیوتیکها)، کلاس II (پپتیدهای تغییر نیافته، غیر لنتی بیوتیک)و کلاس III (پروتئینهای بزرگ، ناپایداری حرارتی)تقسیم میشوند.
پپتیدهای کلاس I باکتریوسین های تغییریافته پس از ترجمه یا لنتیبیوتیکهای کمتر از ۲۸ آمینواسید پپتیدهای ممبرانوس کوچک (۵ کیلو دالتون)، پپتیدهای خطی یا کروی که شامل لنتیونین، متیل لنتیونین و آمینواسیدهای دهیدراته هستند. پپتیدهای ساختار خطی حالت اختلال در عملکرد غشا و پپتیدهای ساختار کروی با واکنش آنزیمی سلولی هستند. باکتریوسین های کلاس I بعدا به چند لنتی بیوتیک تقسیم میشوند، از جمله پپتید خطی نیسین و مرسازیدین پپتید کروی، لبیرینتوپپتین، مانند لبیرینتوپپتین A۲ پپتید کروی، و ساکتی بیوتیک ها، مانند سابتیلوزین A پپتید کروی.
باکتریوسین های کلاس دو، ۳۰ تا ۶۰ آمینو اسید (۱۰ کیلو دالتون)هستند، که همیشه ویژگیهای منحصر به فرد تحمل گرما، بدون تغییر غیر لنتیونین و بار مثبت را نشان میدهند. باکتریوسین های کلاس II توسط کوتر و همکاران (۲۰۱۳)به پنج زیر کلاس تقسیم میشوند. .. باکتریوسین های کلاس IIa پپتیدهای فعال لیستریا با توالی آمینواسیدی مشترک YGNGVXaaC در N - ترمینال هستند و شامل پدیوسین PA - ۱ و کارنوباکتریوسین X هستند. باکتریوسین های کلاس IIb به دو پپتید تغییر نیافته مختلف برای تشکیل یک کمپلکس اتصالی کاملا فعال، مانند لاکتاسین F و ABP - ۱۱۸ نیاز دارند. باکتریوسین های نوع IIc باکتریوسین های پپتیدی حلقوی مانند کارنوسیکلین A و انتروسین AS - ۴۸ هستند. باکتریوسین های کلاس IID خطی، غیر پدیوسین، باکتریوسین های تک پپتیدی، از جمله اپیدرمیسین NI۰۱ و لاکتوکوکوسین A هستند. باکتریوسین های کلاس IIe، تغییرات پس از ترجمه غیر ریبوزومی در منطقه غنی از سرین انتهای کربوکسیل، مانند میکروسین E۴۹۲ هستند. از آنجا که میکروسین E۴۹۲ از کلبسیلا پنومونیه جدا شد، در حالی که باکتری گرم مثبت نبود، باکتریوسین های کلاس IIe باید به میکروسین های باکتری گرم منفی طبقهبندی شوند.
باکتریوسین های کلاس III وزن مولکولی بزرگ (kDa ۳۰)، پروتئینهای ناپایدار گرمایی هستند. کلاس ۳ میتواند به دو گروه مجزا تقسیم شود. گروه A باکتریوسین ها آنزیمهای باکتریولیتیک هستند که با لیز کردن سلول مانند انترولیزین A، سویههای حساس را از بین میبرند. باکتریوسین های گروه ب، پروتئینهای غیرلیتیکی مانند کازئی سین ۸۰ و هلوتیسین جی.
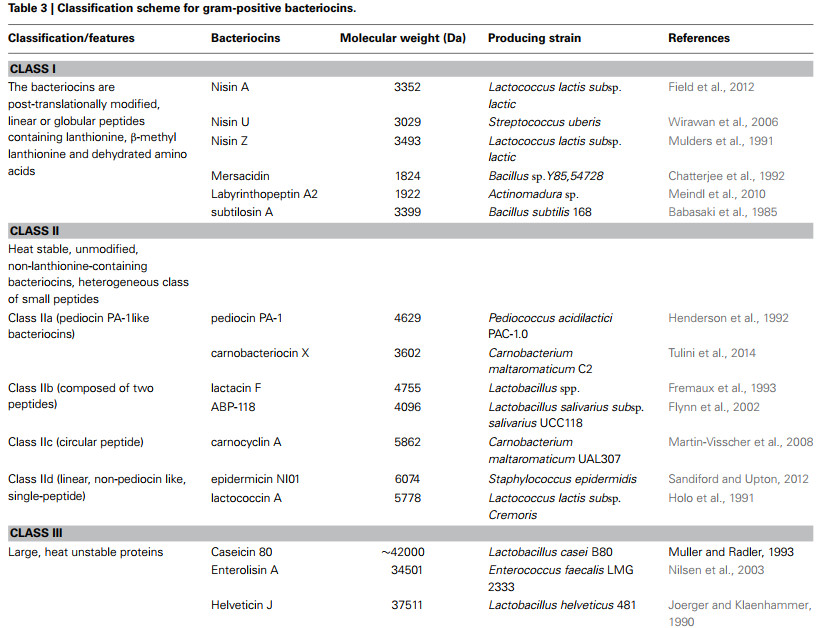
برچسب های مهم
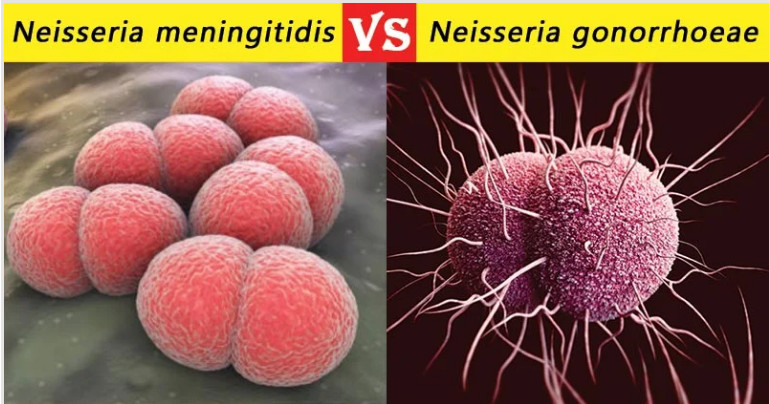
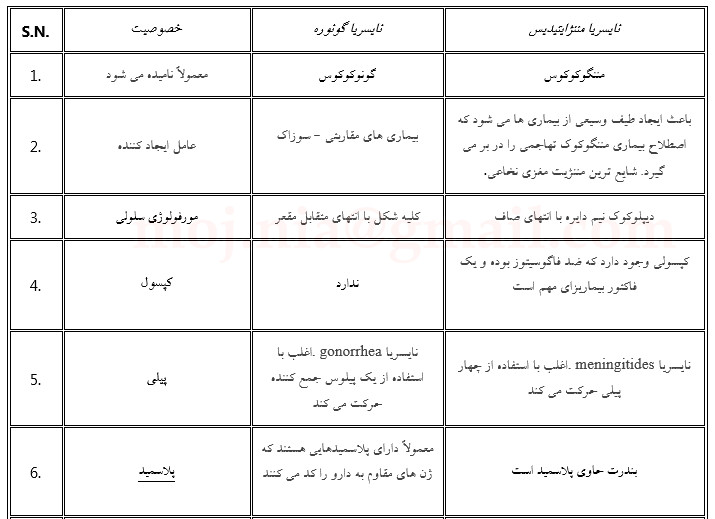
نایسریا مننژیتیدیس و نایسریا گونوره، پاتوژن های اجباری انسانی هستند که باعث ایجاد سندرم های بیماری متفاوت می شوند. آنها هر دو دیپلوکوک گرم منفی، غیر اسپور، اکسیداز مثبت هستند و تمایز آنها بر اساس خصوصیات مورفولوژیکی و کشت دشوار است
برچسب های مهم
| Basic Characteristics | Properties ( Neisseria gonorrhoeae) |
| Capsule | Negative (-ve) |
| Catalase | Positive (+ve) |
| Gas | Negative (-ve) |
| Gram Staining | Negative (-ve) |
| H2S | Negative (-ve) |
| Hemolysis | Negative (-ve) |
| Nitrate Reduction | Negative (-ve) |
| Oxidase | Positive (+ve) |
| Pigment | Negative (-ve) |
| Shape | Diplococci |
| Fermentation of | |
| DNase | Negative (-ve) |
| Fructose | Negative (-ve) |
| Glucose | Positive (+ve) |
| Lactose | Negative (-ve) |
| Maltose | Negative (-ve) |
| Mannose | Negative (-ve) |
| Sucrose | Negative (-ve) |
| Enzymatic Reactions | |
| Tributyrin | Negative (-ve) |
برچسب های مهم
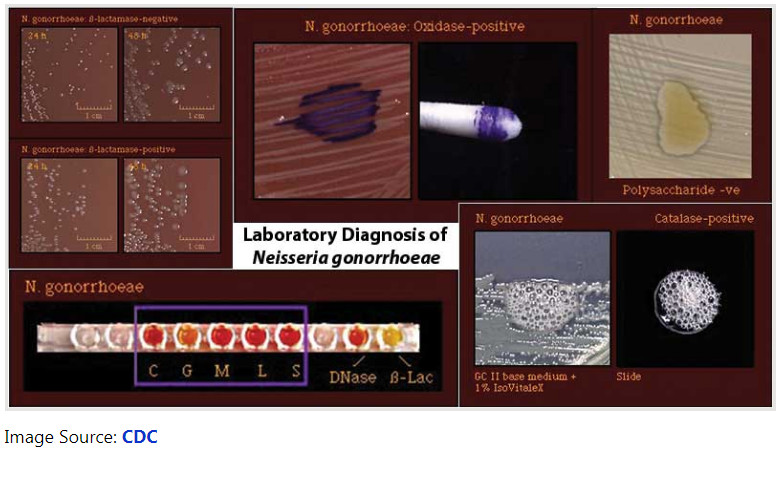
نایسریا گونوره تشخیص آزمایشگاهی، درمان، پیشگیری
Neisseria gonorrhoeae یک پاتوژن اجباری انسانی و عامل ایجاد کننده سوزاک است.
در ایالات متحده، این دومین بیماری مسری شایع است که سالانه بیش از 350000 مورد گزارش می شود.
سندرم ها شامل سرویکسیت در زنان و اورتریت، فارنژیت و پروکتیت در هر دو جنس است. در صورت عدم درمان، زنان ممکن است عواقب شدید بیماری التهابی لگن، درد مزمن لگن، حاملگی خارج از رحم و ناباروری لولهها را تجربه کنند، در حالی که مردان ممکن است به اپیدیدیمیت، پروستاتیت و تنگی مجرای ادرار مبتلا شوند
انتخاب و جمع آوری نمونه
انتخاب و روش جمعآوری نمونه به روش آزمایشی مورد استفاده در آزمایشگاه و سن، جنس و گرایش جنسی بیمار بستگی دارد.
مجرای ادرار: هنگامی که بیماران ترشح دارند ترشحات مجرای ادرار را نشان می دهند. اگر ترشحی وجود نداشت، مجرا را به صورت عمودی فشرده کنید تا مجرای ادرار دیستال باز شود و یک سواب نازک و مرطوب شده با آب (کلسیم آلژینات یا داکرون) با سیم انعطاف پذیر به آرامی (3 تا 4 سانتی متر در نرها یا 1 سانتی متر تا 2 سانتی متر در ماده ها) وارد کنید. ، به آرامی بچرخانید و به آرامی عقب بکشید.
ادرار: از بیماران بخواهید که فقط 10 تا 15 میلی لیتر اول ادرار را جمع آوری کنند. برای افزایش احتمال تشخیص ارگانیسم، بیماران نباید حداقل 2 ساعت قبل از جمع آوری نمونه ادرار خود را تخلیه کنند.
دهانه رحم: برای مشاهده دهانه رحم، اسپکولوم را در واژن قرار دهید. یک سواب به طول 1 تا 3 سانتیمتر را در کانال آندو سرویکس قرار دهید و به مدت 10 تا 30 ثانیه بچرخانید تا اگزودا جذب شود.
واژینال: در صورت وجود ترشحات واژن جمع آوری کنید. نمونه های شستشوی واژن برای دختران قبل از بلوغ ارجح و قابل قبول است. در صورت عدم امکان، یک سواب پنبه ای استریل را به دیواره خلفی واژن بمالید و اجازه دهید سواب نمونه را جذب کند.
رکتوم: نمونه ها را می توان blindly یا ترجیحاً از طریق آنوسکوپ تهیه کرد. سواب 2 تا 3 سانتی متری را داخل کانال مقعد قرار دهید. اجتناب از مواد مدفوع، چرخش به کریپت های نمونه درست در داخل حلقه مقعد. اجازه دهید سواب به مدت 10 ثانیه نمونه را جذب کند
اوروفارنکس: سوابهای استریل را روی حلق خلفی و کریپتهای لوزهها بمالید یا از نوزادان آسپیراسیون نازوفارنکس بگیرید.
ملتحمه: هر گونه اگزودا یا چرک موجود در چشم باید با دقت با سواب استریل خارج شود. برای مالش ملتحمه آسیب دیده باید از سواب دوم مرطوب شده با نمک استفاده شود. این سواب باید به یک ویال از محیط انتقال شکسته شود.
مایعات بدن استریل: محل سوراخ شدن پوست را با ید (1٪ تا 2٪ یا محلول 10٪ پوویدون ید [1٪ ید آزاد]) تمیز کنید. در صورت استفاده از تنتور ید، برای جلوگیری از سوختگی، آن را با اتانول 70 درصد حذف کنید. انجام آسپیراسیون از راه پوست برای مایعات جنب، پریکارد، صفاقی یا سینوویال. در صورت امکان از مجموعه غیر هپارینیزه استفاده کنید
حمل و نقل و جابجایی
برای به حداقل رساندن اثرات بازدارندگی مواد ناشناخته در نمونه، سواب ها باید مستقیماً روی محیط رشد تلقیح شوند یا بلافاصله پس از نمونه برداری در محیط انتقال سواب قرار گیرند.
اگر محیط تلقیح شده به آزمایشگاه محلی منتقل می شود، پلیت ها نباید بیش از 5 ساعت در یک فضای غنی شده با CO2 با استفاده از یک شیشه شمع یا یک سیستم تجاری تولید کننده CO2 در دمای اتاق نگهداری شوند.
در صورت نیاز به حمل و نقل در مسافت های طولانی، نمونه ها باید روی محیط های موجود در یک سیستم تولید کننده CO2 تلقیح شوند، به مدت 18 ساعت تا 24 ساعت انکوبه شوند و قبل از ارسال روی صفحه رشد قابل مشاهده داشته باشند
میکروسکوپ
اسمیر مستقیم برای رنگ آمیزی گرم ممکن است به محض جمع آوری نمونه سواب از مجرای ادرار، دهانه رحم، واژن یا رکتوم انجام شود.
رنگ آمیزی گرم اسمیر از اگزوداهای مجرای ادرار یا ترشحات اندوسرویکال، دیپلوکوک های درون سلولی گرم منفی، غیر متحرک و معمولی را نشان می دهد
کشت
روش آزمایشگاهی ترجیحی فعلی برای تشخیص عفونت N. gonorrhoeae جداسازی و شناسایی عامل است.
نمونه های اولیه باید روی آگار شکلاتی غیرانتخابی و آگار انتخابی حاوی عوامل ضد میکروبی که مانع رشد باکتری ها و قارچ های کامنسال می شوند تلقیح شوند.
محیط رشد:
اصلاح شده Thayer Martin Medium (آگار شکلاتی حاوی آنتی بیوتیک ها (وانکومایسین، کولیستین، تری متوپریم و نیستاتین)) اغلب مورد استفاده قرار می گیرد.
محیط اصلاح شده نیویورک سیتی (MNC) نیز برای کشت نایسریا گونوره استفاده می شود.
پلیت های تلقیح شده باید در دمای 35 تا 37 درجه سانتیگراد در یک جو مرطوب غنی شده با CO2 (3 تا 7 درصد) انکوبه شوند.
برای آزمایشات اضافی باید از کشت 18 تا 24 ساعته به عنوان تلقیح استفاده شود.
توجه: پلیت ها نباید بیش از 48 ساعت انکوبه شوند زیرا بیشتر کشت های قدیمی در شرایط نگهداری دوام نمی آورند. اتولیز ممکن است در طی انکوباسیون طولانی مدت اتفاق بیفتد
جدایه ها باید حداقل یک بار در محیط غیرانتخابی پس از جداسازی اولیه قبل از استفاده در یک آزمایش تشخیصی که به کشت خالص یا تلقیح سنگین نیاز دارد، زیر کشت قرار گیرند.
شناسایی احتمالی:
شناسایی احتمالی N. gonorrhoeae بر روی جداسازی یک دیپلوکوک گرم منفی اکسیداز مثبت، کاتالاز مثبت استوار است که از محل های تناسلی ادراری که در محیطهای انتخابی رشد میکنند، بازیابی شده است
تست های تاییدی
تست های تاییدی شامل تست های بیوشیمیایی، تست های سوبسترای آنزیمی کروموژنیک، تست های ایمنی و روش های اسید نوکلئیک می باشد.
واکنش های بیوشیمیایی:
تست اکسیداز: مثبت
گلوکز را تخمیر می کند اما مالتوز، ساکارز یا لاکتوز را تخمیر نمی کند
تست DNase: منفی
آزمایش بتا گالاکتوزیداز (ONPG): منفی است
تست گلوتامیل آمینوپپتیداز (GAP): منفی
آزمایش سوبسترای آنزیمی:
هیدروکسی پرولیآمینوپپتیداز مثبت
تست حساسیت ضد میکروبی
نظارت بر حساسیت های ضد میکروبی N. gonorrhoeae برای بررسی شکست درمان و ارزیابی اثربخشی درمان های توصیه شده در حال حاضر مهم است.
مقاومت آنتی بیوتیکی در نایسریا گونوره به شدت درمان موفق سوزاک را به خطر انداخته است.
پنی سیلین ها، تتراسایکلین ها و ماکرولیدهای جدیدتر کاربرد محدودی دارند و اسپکتینومایسین (و در بسیاری از نقاط جهان کینولون ها) به دلیل مقاومت حذف شده اند.
از درمانهای معمولاً توصیهشده، فقط سفالوسپورینهای نسل سوم و بهویژه سفتریاکسون اثربخشی خود را حفظ کردهاند، اما حساسیت به این آنتیبیوتیکها نیز کاهش یافته است
درمان
درمان فعلی توصیه شده توسط CDC یک آنتی بیوتیک درمانی دوگانه است.
این شامل یک دوز تک تزریقی سفتریاکسون (یک سفالوسپورین نسل سوم) همراه با آزیترومایسین است که به صورت خوراکی تجویز می شود. آزیترومایسین برای پوشش اضافی سوزاک که ممکن است به سفالوسپورین مقاوم باشد اما نسبت به ماکرولیدها حساس باشد ترجیح داده می شود.
شرکای جنسی (که توسط CDC به عنوان تماس جنسی در 60 روز گذشته تعریف شده است) نیز باید مطلع شوند، آزمایش شوند و تحت درمان قرار گیرند.
مهم است که اگر علائم پس از دریافت درمان عفونت N. gonorrhoeae ادامه یابد، باید یک ارزیابی مجدد انجام شود
پیشگیری از عفونت
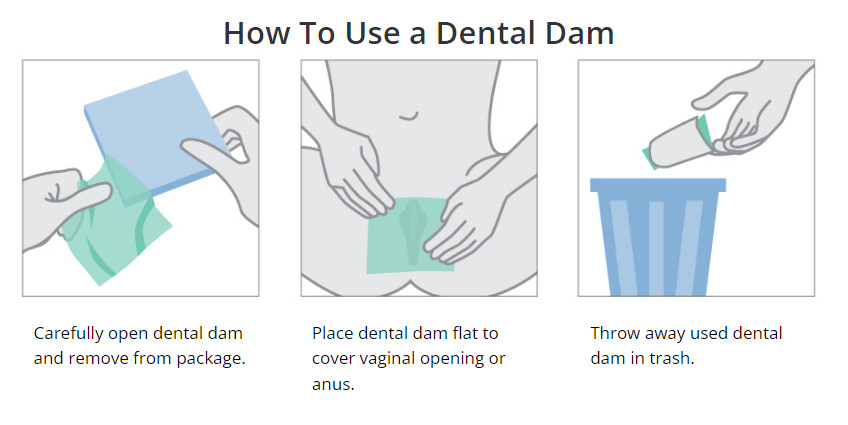
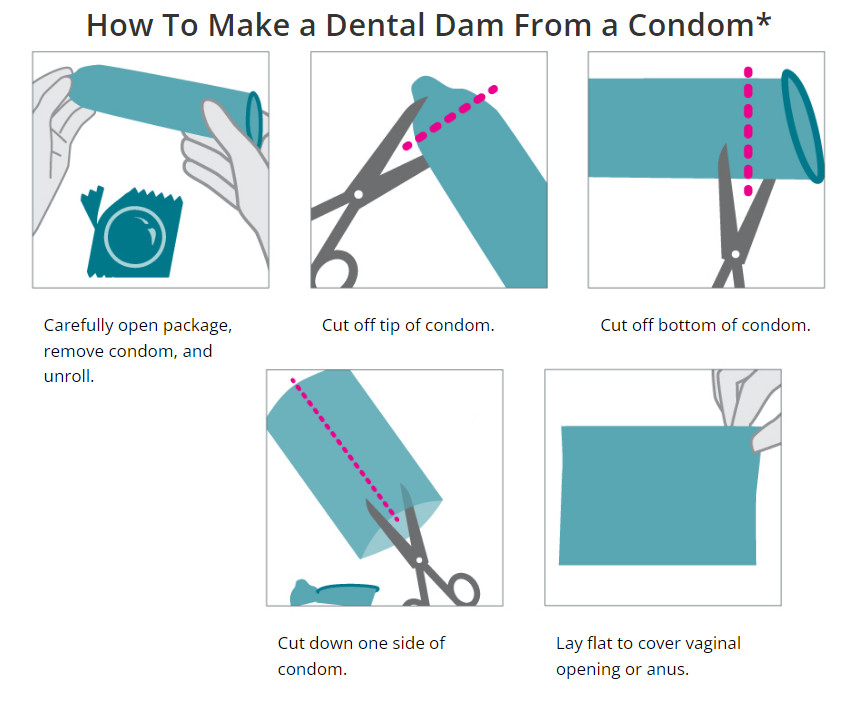
انتقال را می توان با استفاده از موانع لاتکس (مانند کاندوم یا سدهای دندانی dental dams) در طول رابطه جنسی و با محدود کردن شرکای جنسی کاهش داد.
در هنگام رابطه جنسی دهانی و مقعدی نیز باید از کاندوم و dental dams استفاده شود.
پرهیز از رابطه جنسی
داشتن یک شریک جنسی تک همسر که به این عفونت مبتلا نیست
برای به حداقل رساندن خطر انتقال سوزاک به دیگران، حداقل تا هفت روز پس از اتمام درمان از داشتن رابطه جنسی خودداری کنید
سد های دندانی ورقه های لاتکس یا پلی اورتان هستند که بین دهان و واژن یا مقعد هنگام رابطه جنسی دهانی استفاده می شوند
برچسب های مهم
Thayer-Martin آگار یک محیط انتخابی است که برای جداسازی گنوکوک ها (Neisseria gonorrheae) از نمونه های حاوی فلور مخلوطی از باکتری ها و/یا قارچ ها استفاده می شود. نمونه ادراری تناسلی آگار اصلاح شده تایر مارتین (MTM) یک پایه آگار GC حاوی وانکومایسین، کولیستین، نیستاتین و تری متوپریم لاکتات (VCNT) است. جداسازی انتخابی نایسریا گونوره با سرکوب اکثر دیپلوکوک های گرم منفی، باسیل های گرم منفی، ارگانیسم های گرم مثبت و مخمر به دست می آید
محیط Thayer-Martin حاوی مواد ضد میکروبی است که مانع از رشد ارگانیسمهایی غیر از N. gonorrhoeae میشود.
وانکومایسین باکتری های گرم مثبت را مهار می کند
کولیستین باکتری های گرم منفی از جمله کامنسال نایسریا را مهار می کند.
تری متوپریم از تجمع گونه های پروتئوس جلوگیری می کند.
نیستاتین یک عامل ضد قارچ است
بیشتر سویه های نایسریا نیازمند رشد پیچیده ای هستند. گونوکوک ها قادر به رشد در آگار خون معمولی نیستند
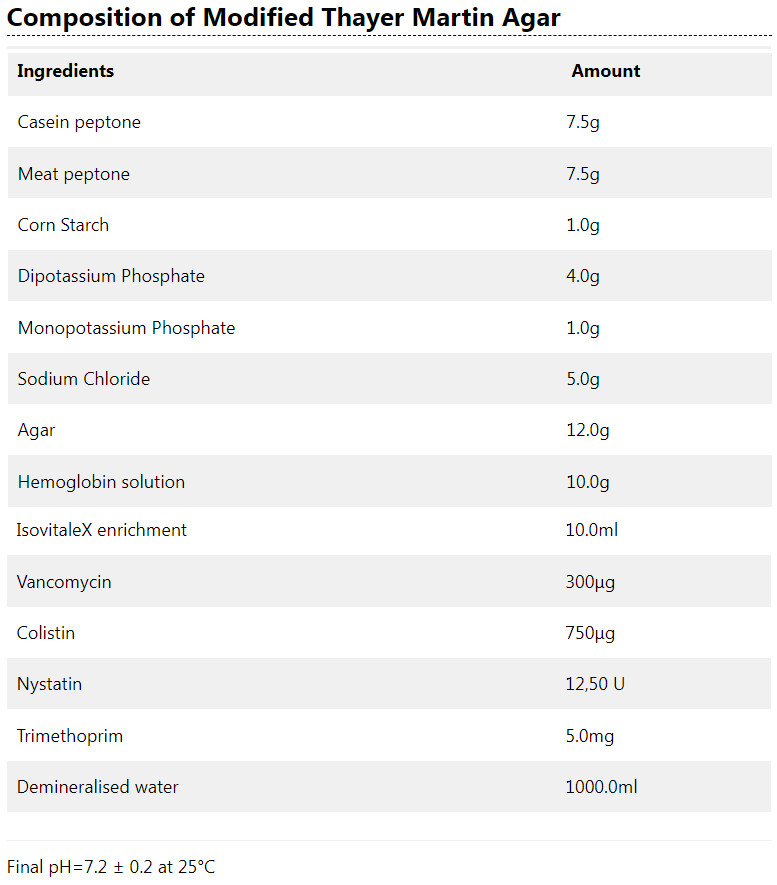
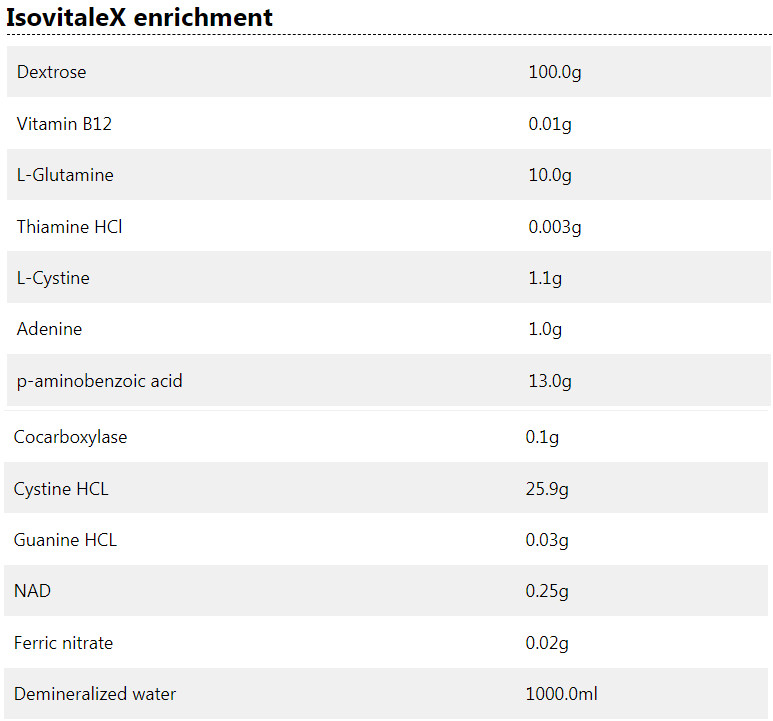
تهیه تایر مارتین آگار اصلاح شده
تهیه پایه GC Agar
اجزای پایه متوسط GC را به آب مقطر اضافه کنید و حجم را به 730.0 میلی لیتر برسانید. خوب مخلوط کنید. به آرامی حرارت دهید تا به جوش بیاید. اتوکلاو در دمای 121 درجه سانتیگراد به مدت 15 دقیقه. تا دمای 45-50 درجه سانتیگراد خنک شود.
تهیه محلول هموگلوبین
هموگلوبین را به آب مقطر اضافه کنید و حجم آن را به 250.0 میلی لیتر برسانید. کاملا مخلوط کنید. اتوکلاو در دمای 121 درجه سانتیگراد به مدت 15 دقیقه. تا دمای 45-50 درجه سانتیگراد خنک شود.
آماده سازی غنی سازی IsoVitaleX (10 میلی لیتر)
اجزاء را به آب مقطر اضافه کنید و حجم را به 10.0 میلی لیتر برسانید. کاملا مخلوط کنید. فیلتر استریل کنید.
تهیه محلول آنتی بیوتیک VCNT (10 میلی لیتر)
اجزاء را به آب مقطر اضافه کنید و حجم را به 10.0 میلی لیتر برسانید. کاملا مخلوط کنید. فیلتر استریل کنید.
آماده سازی محیط
به 730.0 میلی لیتر از پایه سرد شده و استریل GC آگار، 250.0 میلی لیتر محلول هموگلوبین استریل را به صورت آسپتیک اضافه کنید. 10.0 میلی لیتر IsoVitaleX غنی شده و 10.0 میلی لیتر محلول آنتی بیوتیک VCNT. کاملا مخلوط کنید و در ظروف پتری استریل بریزید یا در لوله های استریل پخش کنید
کشت و جداسازی
نمونه (مجرای ادراری یا اندوسرویکال) مستقیماً در پلیت های کشت تلقیح می شود (سواب هایی با شفت های پلاستیکی یا سیمی ، داکرون یا آلژینات کلسیم برای جمع آوری نمونه برای کشت گونوکوک استفاده می شود).
پلیت کشت تلقیح شده باید به سرعت در یک محیط غنی شده با CO2 (3٪ - 10٪) قرار داده شود و در دمای 35-37 درجه سانتیگراد انکوبه شود.
کلنی های کوچک مات، خاکستری مایل به سفید تا بی رنگ، برجسته، درخشان و صاف دیده می شود.
کنترل کیفیت
سویه N. meningitidis QC را به مدت 18-24 ساعت در MTM در دمای 35-37 درجه سانتی گراد با 5% CO2 (یا در شیشه شمع) انکوبه کنید.
MTM را برای مورفولوژی کلنی خاص مشاهده کنید.
به عنوان یک آزمایش استریل بودن محیط، یک پلیت بدون تلقیح را به مدت 48 ساعت در دمای 35-37 درجه سانتیگراد با 5% CO2 (یا در یک شیشه شمع) انکوبه کنید
نتیجه و تفاسیر
N. meningitidis باید به صورت کلونی های بزرگ، گرد، صاف، محدب، بی رنگ تا خاکستری مات روی MTM بدون تغییر رنگ محیط ظاهر شود.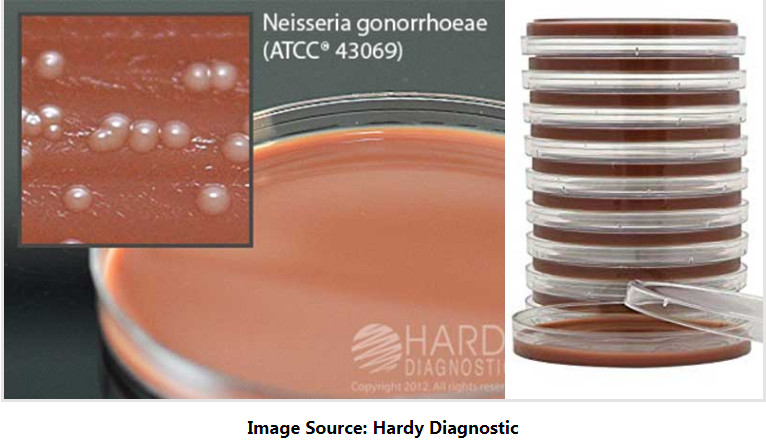
برچسب های مهم
باکتریوسین ها نوعی از پپتیدهای ضد میکروبی سنتز شده ریبوزومی هستند که توسط باکتریها تولید میشوند و میتوانند گونههای باکتریایی مرتبط یا غیر مرتبط با باکتریهای تولید شده را بکشند و یا مهار کنند، اما به خود باکتریها توسط پروتئینهای ایمنی ویژه آسیب نخواهند رساند. باکتریوسین ها به دلیل ویژگیهای خاص تنوع زیاد ساختار و عملکرد، منابع طبیعی و پایدار بودن در برابر گرما، به یکی از سلاحها علیه میکروارگانیسمها تبدیل میشوند. بسیاری از مطالعات اخیر باکتریوسین ها را برای کاربرد در تکنولوژی غذایی خالص و شناسایی کردهاند که هدف آنها گسترش زمان نگهداری مواد غذایی، درمان بیماریهای پاتوژن و درمان سرطان و حفظ سلامت انسان است. بنابراین باکتریوسین ها ممکن است به یک داروی بالقوه برای جایگزینی آنتیبیوتیکها به منظور درمان عوامل بیماری زای مقاوم به چند دارو در آینده تبدیل شوند.
بسیاری از مواد ضد باکتریایی توسط حیوانات، گیاهان، حشرات و باکتریها تولید میشوند، مانند پراکسید هیدروژن، اسیدهای چرب، اسیدهای آلی، اتانول، آنتیبیوتیکها و باکتریوسین ها. پپتیدهای ضد میکروبی یا پروتئینهای تولید شده توسط باکتریها به عنوان باکتریوسین طبقهبندی میشوند. مواد مغذی فراوان در محیط تولید میکروبی انواع باکتریوسین ها را برای رقابت در فضا و منابع تحریک میکنند. باکتریوسین ها فراوان هستند، تنوع زیادی دارند، و ژنهایی که پپتیدها یا پروتئینهای ضد میکروبی سنتز شده به صورت ریبوزومی را کد میکنند، که دیگر میکروبیوتای مرتبط (طیف محدود)یا غیر مرتبط (طیف گسترده)را به عنوان یکی از سلاحهای سیستم دفاعی ذاتی باکتریها میکشند
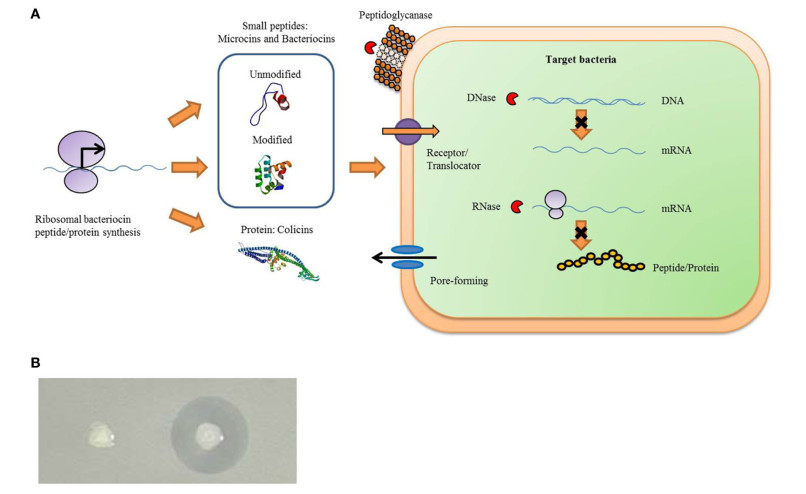
شکل 1 | باکتریوسین ها به عنوان یک سیستم ایمنی باکتریایی طبیعی عمل می کنند. گرم مثبت و گرم منفی می توانند انواع مختلفی از باکتریوسین ها را تولید کنند که به باکتری های تولید کننده باکتریوسین اجازه می دهد تا توانایی مهار رشد باکتری های حساس را داشته باشند. (الف) فرآیند کلی تولید باکتریوسین و عملکردهای ضد باکتریایی. باکتریوسین ها پروتئین ها یا پپتیدهایی هستند که توسط ریبوزومی سنتز می شوند. هنگامی که توسط باکتری های تولید کننده باکتریوسین آزاد می شود، می تواند با گیرنده مربوطه در سطح باکتری های حساس ترکیب شود تا باکتری ها را از بین ببرد. مکانیسمهای حساس باکتریکشی شامل نوع تشکیل منافذ، نوع نوکلئاز با عملکرد DNase و RNase، و نوع پپتیدوگلیکاناز و غیره است. (ب) هنگامی که سویههای تولیدکننده باکتریوسین روی باکتری حساس LB سافت آگار رشد میکنند، یک ناحیه مهاری در اطراف سویههای تولیدکننده باکتریوسین (کلنی سمت راست) ایجاد میشود. با این حال، هیچ منطقه مهاری در اطراف سویه های غیر تولید کننده باکتریوسین (کلنی چپ) وجود ندارد
بیش از ۹۹ % باکتریها میتوانند حداقل یک باکتریوسین تولید کنند که بیشتر آنها شناسایی نشده اند. توانایی کشتن باکتریوسین ها یک استراتژی موفق برای حفظ جمعیت و کاهش تعداد رقبا برای به دست آوردن مواد مغذی بیشتر و فضای زندگی در محیط است. برخلاف بیشتر آنتیبیوتیکها که متابولیت های ثانویه هستند، باکتریوسین ها به طور ریبوزومی سنتز شده و به پروتئازها حساس هستند در حالی که به طور کلی برای بدن انسان و محیط اطراف آن مضر هستند.
اکثر نگهدارندهها و آنتیبیوتیکها که به صورت تجاری در دسترس هستند، از طریق سنتز شیمیایی تولید میشوند و مصرف طولانیمدت آنها میتواند سلامت انسان را تحتتاثیر قرار دهد، زیرا تعداد باکتریها در روده را کاهش میدهد. بر خلاف نگهدارندههای شیمیایی و آنتیبیوتیکها، باکتریوسین های "به طور کلی ایمن" (GRAS) مانند نیسین، وعده استفاده ایمن به عنوان نگهدارنده غذا در سبزیجات، لبنیات، پنیر، گوشت و دیگر محصولات غذایی را میدهند چون آنها آلودگی میکروارگانیسمها را در طول فرآیند تولید مهار میکنند.
طبقهبندی باکتریوسین ها
باکتریوسین های حاصل از باکتریهای گرم منفی
کلی سین Colicins
کولیسینها پروتئینهای ضد باکتریایی هستند که توسط باکتریها تولید میشوند و میتوانند سویههای باکتریایی مرتبط با گونههای تولید شده را بکشند تا رقبای محیطی را برای کسب مواد غذایی و فضای زندگی کاهش دهند. کولیسینها در سه حوزه خاص، یک حوزه انتقال آمینوترمینال (T) ، که در انتقال در طول غشای خارجی از طریق پروتئین ترانس لوکاتور دخیل است، سازماندهی میشوند. یک ناحیه گیرنده مرکزی (R) که با یک گیرنده خارجی باکتریایی متصل میشود؛ و یک دامنه سیتوتوکسیک انتهای کربوکسیل (C)که فعالیت ضد باکتریایی دارد.
به منظور جلوگیری از مسمومیت با کولیسینهای خودساخته، پروتئینهای ایمنی اختصاصی به طور همزمان برای غیر فعال کردن کولیسینها تولید خواهند شد. وقتی یک سطح غشا خارجی باکتریایی دارای پروتئین گیرنده کولیسین و سیستم پروتئینی ترانسکلولاتور است، کولیسین ها به باکتری منتقل میشوند که آن را میکشد و به عنوان سویههای حساس شناخته میشوند. برای یک کولیسین خاص،پروتئین غیر گیرنده باکتریها به عنوان گونههای مقاوم طبقهبندی میشوند. باکتریهای با کمبود سیستم پروتئینی ترانسکلولاتور به عنوان سویههای مقاوم طبقهبندی میشوند که پروتئینهای ایمنی تولید میکنند و به عنوان سویههای ایمن طبقهبندی میشوند. سویههای مقاوم، تحمل کننده و ایمن باکتریها به وسیله کولیسینهای مربوطه کشته نمیشوند. کولیسین های زیادی به صورت متوالی یافت میشوند که بیشتر آنها بر روی پلاسمیدها کد گذاری میشوند در حالی که تعداد کمی در کروموزومها قرار دارند. یک خوشه معمول از ژن کولیسین، پروتئین سم، پروتئین ایمنی و ژن لیز کننده را کد میکند. پروتئین لیز کننده که به عنوان پروتئین آزاد کننده باکتریوسین (BRP)شناخته میشود، میتواند باعث آزاد شدن کولیسین ها از باکتری شود.
با توجه به انتقال در سراسر سیستم غشای خارجی (ترانسلوکاتور)، کولیسینها به دو گروه طبقهبندی میشوند:
گروه A و B
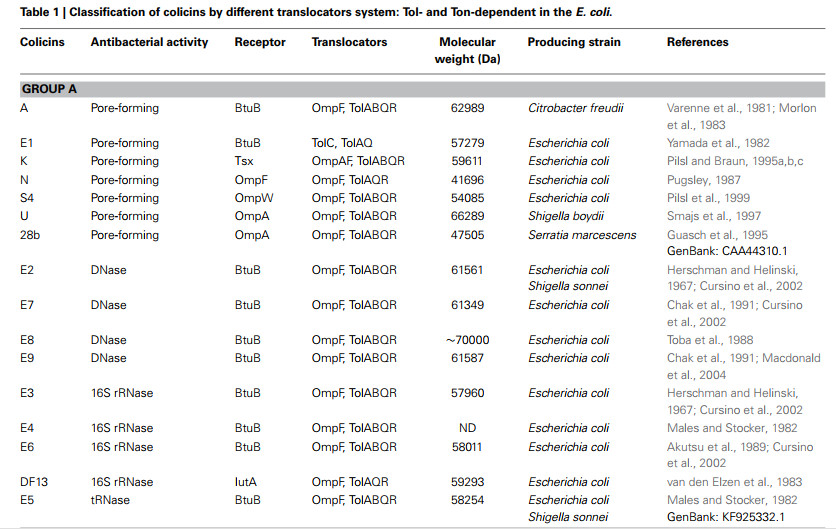
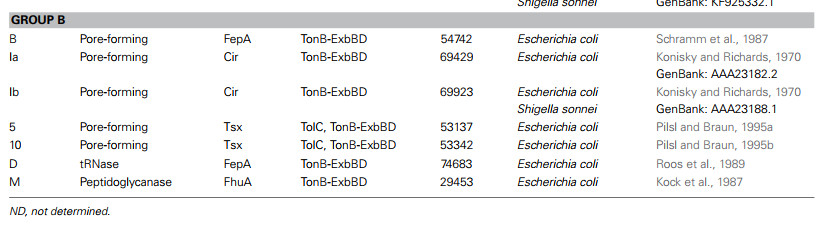
گروه A از سیستم پروتئین Tol (سیستم Tol)برای نفوذ به غشای خارجی باکتریهای حساس استفاده میکند، برای مثال: کولیسینهای E۱ تا E۹، کولیسین A، K، N… باکتریوسین های گروه B از سیستم تئون (سیستم Ton)برای نفوذ به غشای خارجی باکتریهای حساس استفاده میکنند، برای مثال: کولیسین ۵، ۱۰، B، D، M، V، Ia، Ib. .. به طور کلی، گروه A بر روی پلاسمیدهای کوچک با یک ژن لیز کننده کد گذاری میشوند و میتوانند از باکتری آزاد شوند، در حالی که گروه B بر روی پلاسمیدهای بزرگ بدون یک ژن لیز کننده کد گذاری میشوند.
برچسب های مهم