
امروز جمعه ۲۱ اردیبهشت ۱۴۰۳
دسته بندی سایت
برچسب های مهم
پیوند ها
آمار بازدید سایت

برای ارزیابی اثر دو داروی ترکیبی ضد میکروبی، روشی که در حال حاضر در حال استفاده است، سنجش چک بورد در میکروپلیت ۹۶ خانهای است، که تخمین خوبی از اثر ترکیب دارو - دارو در بدن انسان میدهد. روشهای مناسب و تلفیقی در مقالات علمی متعددی توصیف شدهاند که به نوبه خود، پر زحمت و وقت گیر هستند، به ویژه برای تنظیم آمادهسازی میکروپلیت ۹۶ خانهای. هر دارو از هر ترکیبی باید به صورت جداگانه در چند مرحله تهیه و توزیع شود، و اغلب استفاده از آن را از نظر مواد مصرفی و زمان کار محدود کند. در روش ما، نقاط قوت تکنیکهای تلفیقی قبلی حفظ میشوند، اگرچه سختی و زمان اجرا به شدت کاهش مییابند. به هیچ دستگاه آزمایشگاهی ویژهای نیاز نیست. تمام روشهای روش ما را می توان به دستورالعمل CLSI یا EUCAST ارجاع داد. این روش چند مرحله اصلی را فراهم میکند که می توان آنها را به صورت زیر خلاصه کرد:
آمادهسازی مایه تلقیح میکروارگانیسم و سه غلظت داروهای ضد میکروبی. توزیع آسان تمام معرفها در میکروپلیت ها با یک پیپت چند کاناله. ارزیابی تراکم نوری میکروارگانیسم (OD)توسط میکروپلیت خوان و محاسبه درصد رشد برای هر یک از ۷۷ ترکیب.
مقدمه
وقتی دو یا چند دارو به طور همزمان با هم تست میشوند، میتوانند تاثیرات فنوتیپی مختلفی داشته باشند: synergism، additivity، antagonism و یا indifference. برای ارزیابی اثر ترکیب بین دو داروی ضد میکروبی، میکروبیولوژیست از روش رقیقسازی آگار و روش انتشار دیسک استفاده میکند. یک روش دیگر که در حال حاضر در حال استفاده است، سنجش چک بورد در میکروپلیت ۹۶ خانه است، که برآورد خوبی از اثر ترکیب دارو - دارو در بدن میدهد [ ۱، ۲ ]. دومی از یک محیط مایع و یک میکرورقت چک بورد دو بعدی برای ارزیابی ترکیبات عوامل ضد میکروبی علیه موجودات زنده استفاده میکند. در روش چکبورد، دو آنتی میکروب در رقتهای متوالی دوگانه آزمایش میشوند، و غلظت هر یک از داروها هم به تنهایی و هم به صورت ترکیبی مورد آزمایش قرار میگیرد. بنابراین، می توان اثر داروی منفرد را تعیین کرد، اما بالاتر از همه، اثر تولید شده توسط ترکیب آنها هم مشخص می شود. ماهیت تعامل بین دو ماده ضد میکروبی به صورت جبری یا هندسی تعیین میشود [ ۱ ]. روش بسیار مورد استفاده، مناسب و تلفیقی در روشهای میکروبیولوژی بالینی ویرایش سوم clinical Microbiology Procedures Handbook توصیف شدهاست، که به نوبه خود، پر زحمت و وقت گیر است، به ویژه برای تنظیم آمادهسازی میکروپلیت ۹۶ چاهک. هر دارو از هر ترکیبی باید به صورت جداگانه در چند مرحله تهیه و توزیع شود، و اغلب استفاده از آن را از نظر مواد مصرفی و زمان کار محدود کند. در روش ما، ما از نقاط قوت پروتکل ذکر شده قبلی استفاده میکنیم اما سختی و زمان اجرای آن را کاهش میدهیم و تنها از سه غلظت داروهای ضد میکروبی استفاده میکنیم و بر خلاف یک پیپت تک کاناله، رباطهای چند کاناله را توزیع میکنیم. علاوه بر این، هیچ تجهیزات آزمایشگاهی ویژهای مورد نیاز نیست.
تمام روشهای روش ما در برخی موارد با برخی اصلاحات به دستورالعمل CLSI [ ۳ ] یا EUCAST [ ۴ ] اشاره دارد. اگرچه بیشتر روشهای تداخل دارویی در گردش کار آزمایشگاهی بالینی مورد استفاده قرار نمیگیرند، تستهای متعددی که برای این منظور ایجاد شدهاند، در عمل آزمایشگاههای تحقیقاتی بسیار مفید هستند.
علاوه بر این، این امکان وجود دارد که نه تنها مولکولهای ضد میکروبی را با یکدیگر تست کنیم بلکه در ترکیب با ترکیباتی که معمولا خودشان خواص ضد میکروبی ندارند نیز آزمایش کنیم.
با بحران ایجاد شده در سالهای اخیر، بیشتر آنتیبیوتیکها یا داروهای ضد قارچی به دلیل افزایش مقاومت ضد میکروبی با شکست مواجه شدهاند. استفاده از مولکولها در ترکیب میتواند کلید توسعه فرمولاسیونهای جدیدی باشد که لزوما نیاز به کشف مولکولهای جدید ندارند.
جزئیات روش
مواد
کلونی های باکتریایی ایزوله شده.
دو antimicrobics یا ترکیبی از محلولهای استوک یا پودر. مولر هینتون براث (MHB).
محیط کشت مولر هینتون (CAMHB)تغییر یافته با کاتیون. محیط کشت براث مولر هینتون تنظیم شده با کاتیون دو برابر غلظت(۲ XCAMHB). مواد ضد میکروبی برای محلولهای استوک عامل ضد میکروبی. آب مقطر استریل.
استریل ۰.۹ % NaCl.
مخزن پیپتV شکل استریل و یا پلیت پتری دیش استریل به قطر ۹۰ میلی متر یا ۱۰۰ میلی متر کنترلکننده پیپت الکترونیکی یا کنترلکننده پیپت دستی.
پیپت سرولوژیکی استریل: ۲، ۵، ۱۰، ۲۵، ۵۰ میلیلیتر.
tips انتقال پیپت های دستی یا الکترونیکی تک کاناله (۱۰۰۰، ۲۰۰ و ۱۰ میکرولیتر). tip های 200 ماکرولیتر پیپت دستی یا الکترونیکی چندکاناله (۸ یا ۱۲ کانال) tipهای پیپت استریل: ۱۰۰۰، ۲۰۰ و ۱۰ میکرولیتر.
میکروپلیت های ۹۶ خانهای استریل، کف گرد شفاف، تیمار نشده و به طور جداگانه با در پوش، یا کف صاف صاف، بدون تیمار ۵۰، ۱۵ و ۱.۵ میلیلیتر ویال های پلاستیکی یکبار مصرف استریل.
۱۰۰ و ۲۵۰ میلیلیتر فلاسک شیشهای میکروبیولوژیکی. لیدها برای فلاسک شیشهای و یا پنبه آبگریز باکتریایی. ظرف شیشهای.
تجهیز
اتوکلاو. mixer vortex. همزن مغناطیسی.
انکوباتور شیکر مداری هوای محیط 35+-2 درجه سانتی گراد. انکوباتور هوای محیط 35+-2.
میکروپلیت خوان 96 چاهکی دارای یک فیلتر نوری ۶۰۰ نانومتر یا نزدیک به ۶۰۰ نانومتر
روش
روز اول
تهیه محیط کشت، محلولهای استوک دارویی / ترکیبی و مایه تلقیح میکروبی
آمادهسازی محیطهای کشت ۱. مقدار مناسبی از محیط کشت پودر دار را وزن کنید. ۲. با استفاده از یک همزن مغناطیسی، پودر را در آب دیونیزه حل کنید تا زمانی که حجم مورد نیاز به دست آید (دستور العمل گزارششده در بسته درج یا در برگه ثبت را ببینید)و سپس با اتوکلاو در دمای ۱۲۱ درجه سانتی گراد به مدت ۱۵ دقیقه استریل کنید.
محیط کشت مورد نیاز عبارتند از:
۱۰ میلی لیتر MHB. ۵۰ تا ۱۰۰ میلیلیتر ازCAMHA دوبرابر غلظت
آمادهسازی ۱۰۰ میلیلیتر محلول نمکی استریل (NaCl ۰، ۹ %)
۱. با استفاده از یک همزن مغناطیسی، ۰.۹ گرم NaCl را در ۱۰۰ میلیلیتر آب دیونیزه شده حل کرده و سپس با اتوکلاو در ۱۲۱ درجه سانتیگراد به مدت ۱۵ دقیقه استریل کنید.
تهیه مواد ضد میکروبی یا ترکیبی از پودر ۱. مقدار مناسبی از پودر داروی A و دارو B را وزن کرده و هر کدام را در حلال مناسب خود مطابق با درخواست CLSI در فصل زیر حل کنید: "محلول و مواد ضد میکروبی برای آمادهسازی محلول های Stock عوامل ضد میکروبی" و یا طبق توصیه دستورالعملهای EUCAST اگر آنتیبیوتیک یا ترکیب در دستورالعمل ذکر نشده است، از حلالی استفاده کنید که ترکیب را پایدارتر نگه میدارد (این اطلاعات اغلب در برگههای ثبت موجود است).
آمادهسازی مایه تلقیح میکروبی ۱. با یک حلقه استریل یک کلونی ایزوله را از یک پلیت آگار مغذی بیرون بکشید. ۲. کلونی را در ۱۰ میلیلیتر از MHB تلقیح کنید. ۳. باکتریها را در دمای ۳۵ درجه سانتیگراد در انکوباتور شیکر مداری در دور ۲۰۰ rpm تحت شرایط هوازی به مدت ۱۸ ساعت کشت دهید.
توجه: پس از ۱۸ ساعت انکوباسیون، تحت شرایط ذکر شده، کشت به غلظت ۱۰۹ CFU / ml خواهد رسید.
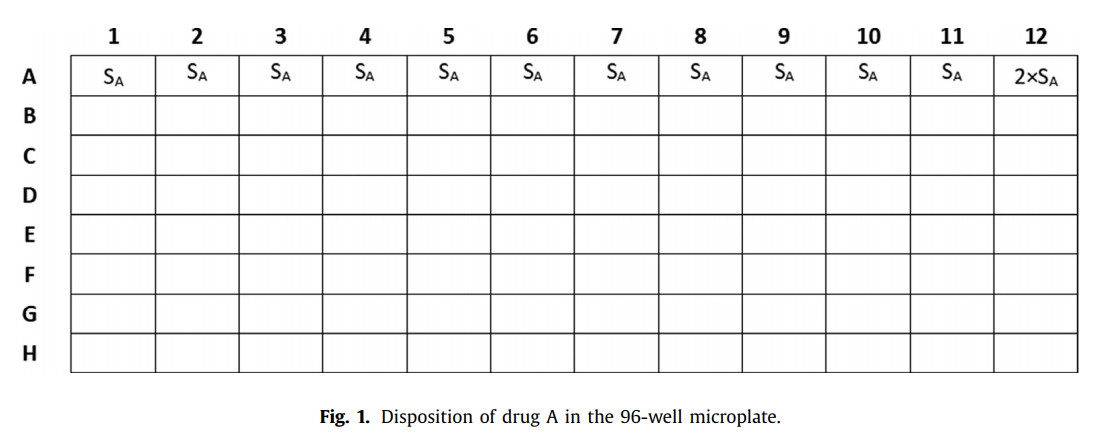
شکل ۱. جابجایی دارو A در میکروپلیت ۹۶ خانه.
روز دوم
روز دوم
تهیه پلیت برای اندازهگیری تعامل دو دارو با استفاده از سنجش چک بورد
۱. ۱۰۰ میکرولیتر از محیط CAMHB دوبرابر غلظت را در یک مخزن V شکل یا ظرف پتری استریل قرار دهید و به هر چاه میکروپلیت، با پیپت چند کاناله، که توسط ستون از چپ به راست و یا برعکس پیش میرود، تقسیم کنید.
تهیه و توزیع دارو الف.
۱. ۱.۵ میلیلیتر از محلول استوک (SA)را در محیط CAMHB دوبربر غلظت آماده کنید تا محلول ۴ برابر متمرکزتر از بالاترین غلظت داروی A مورد آزمایش بدست آید. ۲. ۵۰۰ میکرولیتر از محلول استوک (۲ SA)را در محیط CAMHB دو برابر آماده کنید تا محلول ۸ برابر متمرکزتر از بالاترین غلظت داروی A مورد آزمایش بدست آید. ۳. ۱۰۰ میکرولیتر از SA را در سطر A از ستونهای ۱ - ۱۱ پخش کنید. ۴. ۱۰۰ میکرولیتر از SA دوبرابر را در چاه A۱۲ تلقیح کنید. (شکل ۱)
توجه: هدف از افزودن محلول Stock دو برابر SA حفظ غلظت ثابت داروی A در طول رقیقسازی متوالی بعدی (نقطه ۹).
اولین رقت سریال دارو A
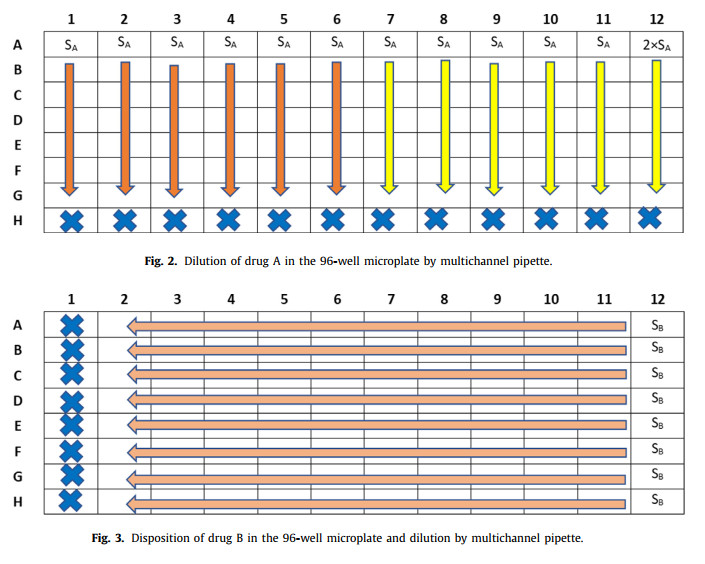
۱. دارو A را از ردیف A به G با استفاده از یک پیپت چند کاناله که روی ۱۰۰ میکرو لیتر تنظیم شدهاست رقیق کرده و حجم باقیمانده را از ردیف G خارج کنید.
نکته: با یک پیپت ۸ کاناله، در دو مرحله با استفاده از ۶ tip رقیق کنید. اولی از ۶ - ۱ و سپس از ۱۲ - ۷. هنگامی که با گام دوم شروع میکنید، tip ه را تغییر دهید (شکل ۲).
تهیه و توزیع دارو B
۱. ۱ میلیلیتر از محلول استوک (SB)را در محیط CAMHB دوبرابر آماده کنید تا محلول ۴ برابر متمرکزتر از بالاترین غلظت دارو B که باید تست شود، به دست آید. ۲. ۱۰۰ میکرولیتر از SB را در هر ستون ۱۲ چاه تخلیه کنید. (شکل ۳).
رقت سریال دوم دارو B
۱. دارو B را رقیق کنید ستون ۱۲ - ۲ با استفاده از یک پیپت چند کاناله که بر روی ۱۰۰ میکرو لیتر تنظیم شدهاست و حجم باقیمانده گرفتهشده از ستون ۲ را حذف کنید.
تلقیح پلیت
۱. از ۱۰ تا ۴۰ میلیلیتر مایه تلقیح باکتریایی ۱۰۶ CFU / ml در ۰، ۹ % NaCl، از کشت روز قبل آماده کنید (فصل: آمادهسازی مایه تلقیح میکروبی). ۲. ۱۰۰ میکرولیتر مایه تلقیح را در یک مخزن V شکل یا ظرف پتری استریل قرار دهید و با استفاده از یک پیپت چند کاناله به هر چاه میکروپلیت انتقال دهید.
توجه: قبل از رقیق کردن کشت باکتریایی در مرحله ۱۰، با vortex برای حداقل ۲۰ ثانیه مخلوط شود. غلظت مایه تلقیح نهایی در میکروپلیت برابر ۵* ۱۰۵ CFU / ml خواهد بود. یک پلیت مشابه، بدون باکتری و با معرفهای مشابه، باید برای به دست آوردن کنترل عدم رشد بکاربرده شود. علاوه بر این، پلیت mirror به عنوان پسزمینه در تجزیه و تحلیل دادهها مفید است (به عنوان مثال، هنگامی که رسوبات ترکیبی ممکن است در طول انکوباسیون ظاهر شوند).
تلقیح پلیت
۱. میکروپلیت را با پوشش خود در یک انکوباتور استاتیک در دمای ۳۵ درجه سانتیگراد به مدت ۱۸ - ۲ ساعت قرار دهید.
توجه: اگر یک تغییر بیش از حد در حجم در طول انکوباسیون وجود داشته باشد، می توان میکروپلیت را با مهر و موم کردن فیلم مهر و موم کرد. همچنین یک سینی با آب میتواند به انکوباتور اضافه شود تا از محیط خشک به نفع تبخیر از ظرف جلوگیری شود.
روز سوم
آنالیز نوری با استفاده از یک میکروپلیت خوان
۱. محتوای چاهک ها را با استفاده از یک پیپت چند کاناله ترکیب کنید. ۲. میکروپلیت را در یک میکروپلیت خوان قرار دهید. ۳. چگالی نوری (OD)را در ۶۰۰ nm یا در حدود ۶۰۰ nm بخوانید (به عنوان مثال ۵۹۵ یا ۶۰۵).
تجزیه و تحلیل دادهها
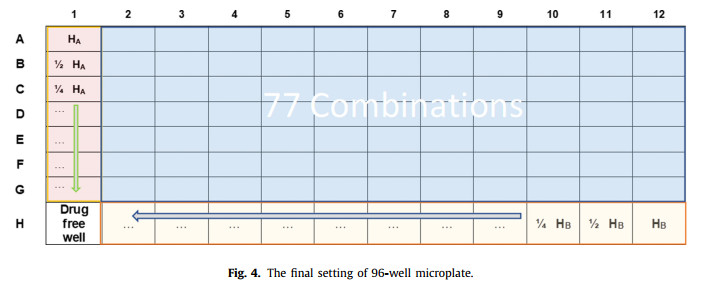
با توجه به تراکم نوری، محاسبه درصد رشد برای هر چاه امکان پذیر است. براساس توزیع معرفهای ساختهشده، صفحه به صورت زیر سازماندهی شدهاست (شکل ۴):
در ستون ۱ از چاههای A تا G، رقتهای سریال دوگانه از دارو A وجود دارد.
A۱ چاهی است که در آن دارو A بالاترین غلظت را دارد (HA).
در H خام از ستونهای ۱۲ - ۲، رقتهای سریالی دوگانه دارو B وجود دارد.
H۱۲ چاهی است که در آن دارو B بالاترین غلظت (HB)را دارد.
H۱ خوب نشاندهنده کنترل رشد باکتری بدون دارو است (رشد ۱۰۰ %). تمام چاههای دیگر میکروپلیت تمام ۷۷ ترکیب ممکن تشکیلشده توسط ترکیب رقتهای متوالی هر آنتیبیوتیک را نشان میدهد.
درصد رشد در هر چاه به صورت زیر محاسبه شد:

توجه: در جایی که هیچ رشدی مشاهده نمیشود یا مقداری که قبلا با استفاده از همان روش تعیین شدهاست، که در آن معرفهای بدون باکتری قرار داده شدهاند.
با توجه به دادهها، محاسبه حداقل غلظت بازدارنده (MIC)برای هر ترکیب نیز امکان پذیر است. MIC به عنوان پایینترین غلظت دارو تعریف میشود که رشد باکتری را بیش از ۸۰ % کاهش میدهد.
مدلهای تعامل دارویی
چندین مدل میتوانند برای تجزیه و تحلیل دادههای بهدستآمده از روش جدید سنجش چک بورد و ارزیابی ماهیت تعامل آزمایشگاهی مورد استفاده قرار گیرند. برخی مثالهای کاربردی را می توان از مقاله زیر برون یابی کرد:
در این مطالعات، دادهها توسط مدلهای غیرپارامتری مبتنی بر مدل جمع ¬ آوری وام و تئوری استقلال Bliss مورد تجزیه و تحلیل قرار گرفتند [ ۸ ].