
امروز جمعه ۲۱ اردیبهشت ۱۴۰۳
دسته بندی سایت
برچسب های مهم
پیوند ها
آمار بازدید سایت
۱.۱ آنتیبیوتیک
آنتیبیوتیکها سنگ بنای داروهای مدرن هستند و به طور گسترده در سراسر جهان توسعهیافته و در حال توسعه در انسان و برای اهداف دامپزشکی و کشاورزی مورد استفاده قرار میگیرند. آنها داروهایی هستند که رشد و تکثیر یک باکتری را از بین میبرند و برای درمان عفونتهای باکتریایی در بدن به کار میروند. آنها متمایز از آنتیسپتیکها (که برای استریل کردن بافت زنده و کاهش خطر عفونت به جای درمان عفونت به کار میروند)و ضدعفونیکنندهها (ضد میکروبی غیر انتخابی که طیف وسیعی از میکروارگانیسمها را میکشد، نه فقط باکتریها، و در سطوح غیر زنده به کار میروند)هستند. هم چنین آنها سم نیستند چون سموم به عنوان یک ماده سمی که توسط یک میکروارگانیسم، گیاه و یا حیوان تولید میشود و موجب بیماری در بدن میشود، تعریف میشوند. آنتیبیوتیکها باعث آسیب مستقیم به سلولهای انسانی نمیشوند. آنتیبیوتیکها میتوانند به صورت وریدی (از طریق سرنگ یا کاتتر)، عضلانی (از طریق سرنگ)، خوراکی (از طریق قرص، کپسول یا مایع)و یا موضعی (مانند کرم، لوسیون، اسپری یا قطره)تجویز شوند. Intravenous موثرترین مسیر است زیرا سطح خونی درمانی فوری آنتیبیوتیک را ایجاد میکند، اما روشهای دهانی اغلب ترجیح داده میشوند چون کمتر تهاجمی هستند، نیازی به بستری در بیمارستان ندارند، و اغلب به سطوح خونی فوق بازدارنده دست مییابند ۲.
آنتیبیوتیکها امروزه میتوانند در یک آزمایشگاه مورد استفاده قرار گیرند اما اغلب بر پایه ترکیباتی هستند که به طور طبیعی توسط میکروارگانیسمها برای آسیب رساندن یا کشتن باکتریها در محیط خود تولید میشوند. در واقع همه میکروارگانیسمها ترکیبات آنتیبیوتیک تولید نمیکنند، تنها حدود ۲۰ گونه وجود دارند که آنتیبیوتیک تولید میکنند که در حال حاضر تولید انبوه دارند و در پزشکی مورد استفاده قرار میگیرند ۳. به طور معمول این میکرو ارگانیسمهای ساکن خاک هستند، اگرچه جستجو برای آنتیبیوتیکهای جدید در حال حاضر شروع به تغییر به میکروب دریایی کردهاست. هر دوی این محیطها تنوع و تراکم بالای میکروارگانیسمها را نشان میدهند. تولید آنتیبیوتیک را می توان به عنوان مکانیسمی در کنار باکتریها و یا دفاع از آنها در نظر گرفت که امکان بقای تولید کننده آنتیبیوتیک را فراهم میآورد. ترکیبات آنتی بیوتیک همچنین میتوانند به عنوان مولکولهای سیگنالینگ بین سلولهای باکتریایی عمل کنند و رفتار باکتریایی مانند تشکیل بیوفیلم را تنظیم کنند. ۶. بنابراین، آنها نقش مهمی در طبیعت دارند که انسانها برای منفعت ما و استفاده از آنتیبیوتیکهای یکپارچه در پزشکی انسان و حیوان انتخاب کردهاند. تعیین کمیت دقیق تاثیر کلی آنتیبیوتیکها بر پویایی عفونت و تمایز بین اثرات عوامل دیگر مانند معرفی واکسن یا بهبود بهداشت دشوار است. با این وجود، استفاده از آنتیبیوتیک با کاهش مرگ و میر ناشی از بیماریهای مسری در سال و افزایش میانگین امید به زندگی در ارتباط است.
۱.۲ تاریخچه آنتیبیوتیکها
تنها به تازگی و در یک جدول زمانی نسبتا کوتاه است که آنتیبیوتیکها در جامعه ما تثبیت شدهاند تا عفونتهای باکتریایی را درمان کنند (شکل ۱ - ۱). درست ۱۱۰ سال پیش، پل ارلیخ (زیست شیمی دان آلمانی، ۱۸۵۴ - ۱۹۱۵)اصطلاح "گلوله جادویی" را زمانی ابداع کرد که در مورد یک ماده شیمیایی که میتواند به طور انتخابی عوامل بیماری زا را در بدن بدون آسیب رساندن به بیمار هدف قرار دهد و بکشد، نظریهپردازی کرد. اولین آنتیبیوتیک جادویی "واقعی" علیه باکتریهایی که به طور بالینی علیه عفونتهای باکتریایی استفاده میشدند، در واقع سالها قبل از استفاده از این اصطلاح مورد استفاده قرار میگرفت. پیوسیانین یک عصاره تهیهشده از باکتری گرم منفی سودوموناس آئروژینوزا توسط اممریچ و لو در سال ۱۸۹۹ بود. این ماده بر علیه تعدادی از باکتریهای بیماری زا فعال بود اما از آنجا که اثر بخشی آن متناقض بود و برای انسانها تا حدی سمی بود، رها شد . ارلیخ، که اکنون پدر بنیانگذار شیمیدرمانی و در مقیاس بزرگ است، با استفاده از صفحات سیستماتیک دارویی، گلوله جادویی خود ("ترکیب ۶۰۶")را علیه باکتری سیفیلیس، ترپونما پالیدوم ایجاد کرد. ترکیب ۶۰۶، یا سالوارسان، پس از کشف آن در سال ۱۹۰۹، رایجترین داروی تجویز شده بود. پرونتوسیل یک آنتیبیوتیک اولیه دیگر بود، ترکیبی که به عنوان بخشی از screen توسط شیمیدانان بایر جوزف کلیر و فریتز میتزش سنتز شد و نشان داده شد که خواص ضد باکتریایی در برابر تعدادی از بیماریها توسط گرهارد دوماگ دارد.. جز فعال سولفانامید قبلا در صنعت رنگ مورد استفاده قرار گرفته بود و پیش از این اختراع نشده بود و امکان تولید مشتقات سولفونامید توسط شرکتهای مختلف را فراهم میکرد. سولفونامیدها قدیمیترین گروه از آنتیبیوتیکها هستند و نسخههای جدید هنوز هم تولید میشوند و امروزه مورد استفاده قرار میگیرند.
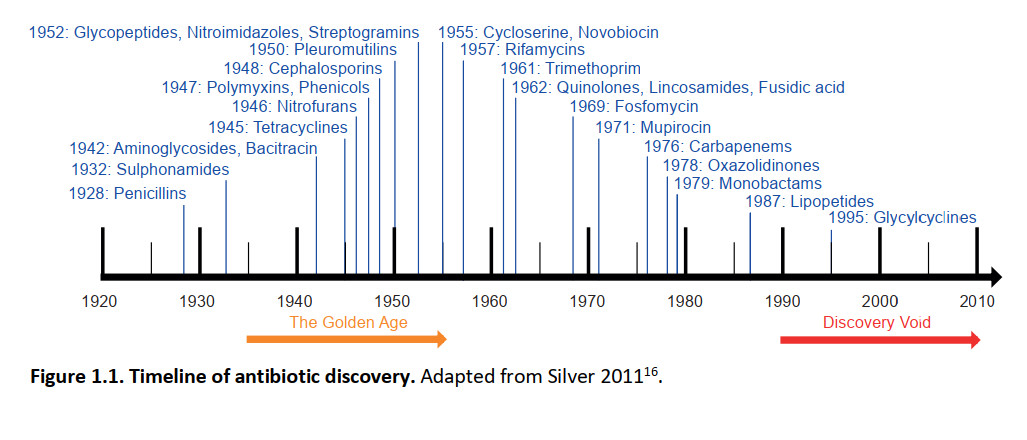
شکل ۱ - ۱: خط زمانی کشف آنتیبیوتیک.
احتمالا معروفترین آنتیبیوتیک، و یکی از قدیمیترین آنتیبیوتیکهای تولید انبوه، پنیسیلین است که در سال ۱۹۲۸ در داستان معروف الکساندر فلمینگ (باکتریشناس اسکاتلندی، ۱۸۸۱ - ۱۹۵۵)و یک پنجره باز کشف شد.
احتمالا شناختهشدهترین آنتیبیوتیک و یکی از قدیمیترین آنتیبیوتیکهای تولید شده به صورت انبوه، آنتیبیوتیک است.
پنیسیلین، در سال ۱۹۲۸ در داستان معروف الکساندر فلمینگ (باکتریشناس اسکاتلندی، ۱۸۸۱ - ۱۹۵۵)و یک پنجره باز کشف شد. یک قارچ مرموز از میان یک پنجره باز و پلیت های آلوده عبور کرده بود که برای مطالعه استافیلوکوکوس مورد استفاده قرار میگرفت، که به عنوان عامل عفونت در انسان شناخته میشد، و این قارچ موفق به توقف رشد این باکتری شده بود.
خواص ضد میکروبی کپکها از قبل شناخته شدهبودند، اما فلمینگ به طور قابلتوجهی در تلاشهای خود برای تصفیه ترکیب دقیق مسئول این اثر، وقف شد. پنیسیلین سرانجام در سال ۱۹۴۵ با غلبه بر سالوارسان در ۱۵ سالگی به تولید انبوه رسید. آنتیبیوتیکهای پنیسیلین تا به امروز هنوز بیشترین داروی تجویز شده در سطح جهان هستند. تولید انبوه پنیسیلین با کشف استرپتومایسین در سال ۱۹۴۳ همزمان شد، یک آنتیبیوتیک جدا شده از باکتری خاک، استرپتومایسس گریزئوس که میتوانست میکوباکتریوم سل، علت سل را درمان کند. این وقایع آغاز "عصر طلایی آنتیبیوتیکها" را نشان داد (شکل ۱.۱): هجده نوع آنتیبیوتیک جدید بین سالهای ۱۹۴۴ تا ۱۹۷۰ کشف شد. پس از آن نرخ کشف با تنها چهار کلاس جدید در دهه ۱۹۷۰ و یک کلاس در دهه ۱۹۸۰ شروع به کاهش کرد. از آن زمان تا کنون هیچ نوع آنتیبیوتیک جدیدی کشف نشده است.
تنها "کشفهای مجدد" رخ دادهاند که شامل اصلاحات آنتی بیوتیکهای از قبل شناختهشده هستند (جدول ۱.۱). کاهش در کشف طبقات جدیدی از آنتیبیوتیکها به دلیل ظهور و گسترش مقاومت آنتیبیوتیکی مشکلساز است، که در آن عفونتهای باکتریایی دیگر نمیتوانند با همان داروهایی که زمانی موثر بودند درمان شوند. از آنجایی که آنتیبیوتیکها از دنیای امروز جداییناپذیر هستند، نگرانیهایی در مورد دوره پس از آنتیبیوتیک وجود دارد. با توجه به این موضوع، تحقیقات فوقالعادهای در سراسر جهان برای کشف آنتیبیوتیکهای جدید، توسعه جایگزینهایی برای آنتیبیوتیکها، و درک تکامل و گسترش مقاومت آنتیبیوتیکی در حال انجام است.
جدول ۱.۱ منابع آنتیبیوتیکها.
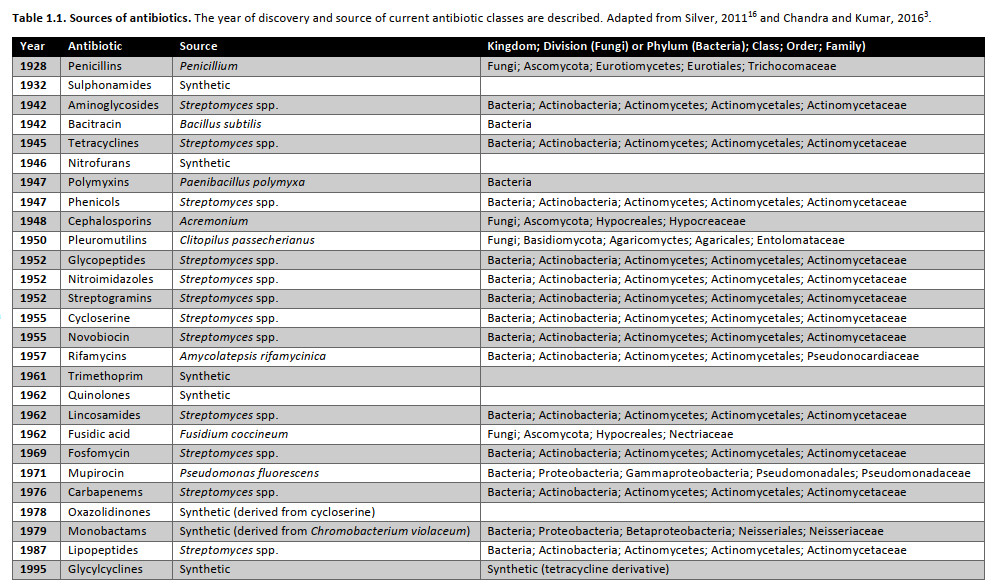
سال کشف و منبع کلاسهای فعلی آنتیبیوتیک توضیح داده میشود.
۱.۳ آنتیبیوتیکهای مربوط به کلینیک
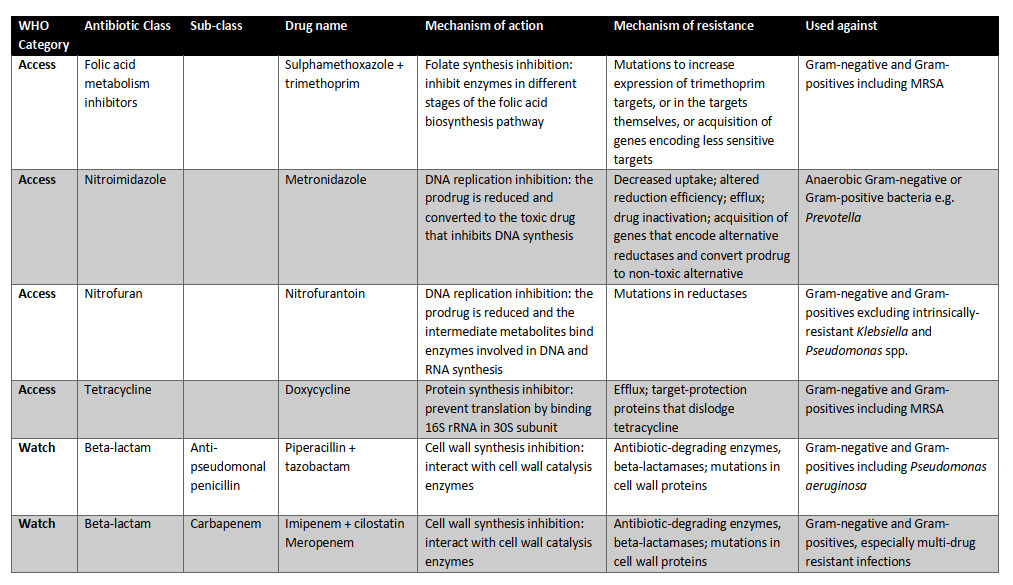
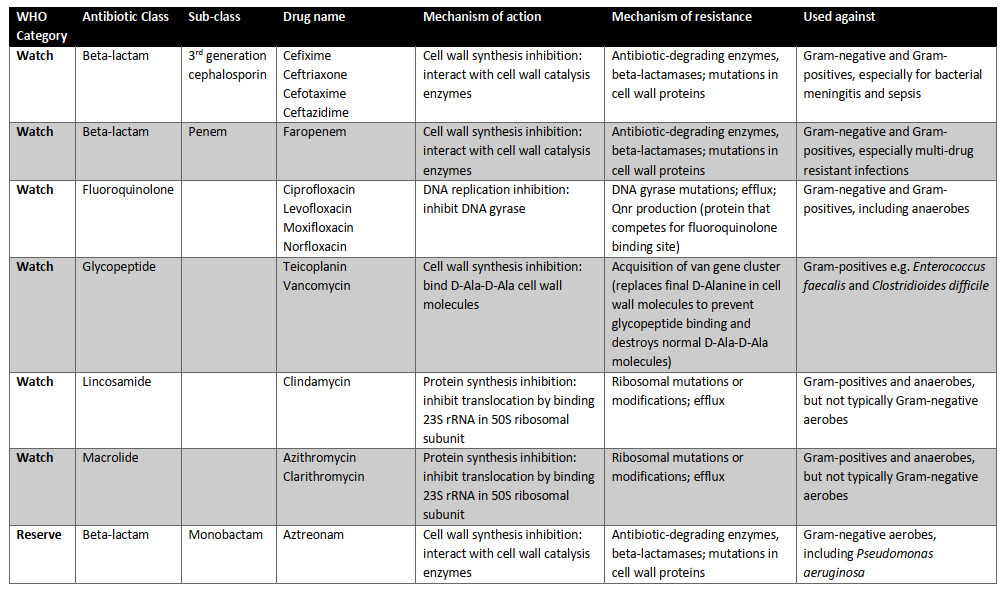
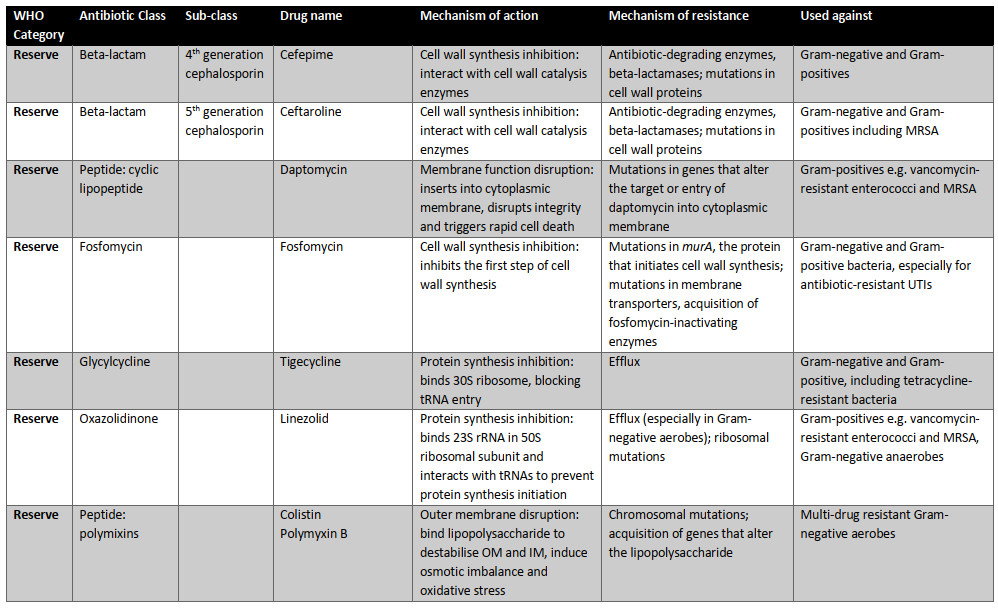
امروزه، ۱۷ گروه از آنتیبیوتیکها برای سازمان بهداشت جهانی ضروری هستند (جدول ۱.۲). سه دسته از آنتیبیوتیکهای ضروری وجود دارد: دسترسی (اولین یا دومین خط گزینههای دفاعی برای عفونتهای شایع)؛ مراقب باشید (پتانسیل مقاومت بالاتر اما هنوز هم به عنوان تیمار خط اول یا دوم توصیه میشود)؛ و رزرو (گزینه "آخرین راهحل" برای عفونتهای جدی مقاوم به آنتیبیوتیک). هر آنتیبیوتیک مکانیسم عمل متفاوتی دارد (شکل ۱.۲)، مکانیسم مقاومت و میتواند انواع مختلف پاتوژن های باکتریایی را هدف قرار دهد (جدول ۱.۲). این ممکن است شامل باکتریهای گرم منفی و گرم مثبت باشد که توسط تکنیک رنگآمیزی گرم که توسط هانس کریستین گرم در سال ۱۸۸۴ ایجاد شد تعیین شدهاست. علاوه بر این، باکتریها میتوانند به شدت هوازی یا بیهوازی باشند، به این معنی که نبود یا حضور اکسیژن به ترتیب سمی است، یا جایی بین آنها. آنتیبیوتیکها مانند آمینوگلیکوزیدها بر اجزای مسیر تنفس هوازی تکیه میکنند و چنین تصور میشود که طیف فعالیت آنها تنها شامل باکتریهای هوازی است نه بیهوازی. آنتیبیوتیکهای ضروری در زیر با جزئیات بیشتر مورد بحث قرار میگیرند، از جمله طیف گزارششده آنها از فعالیت.
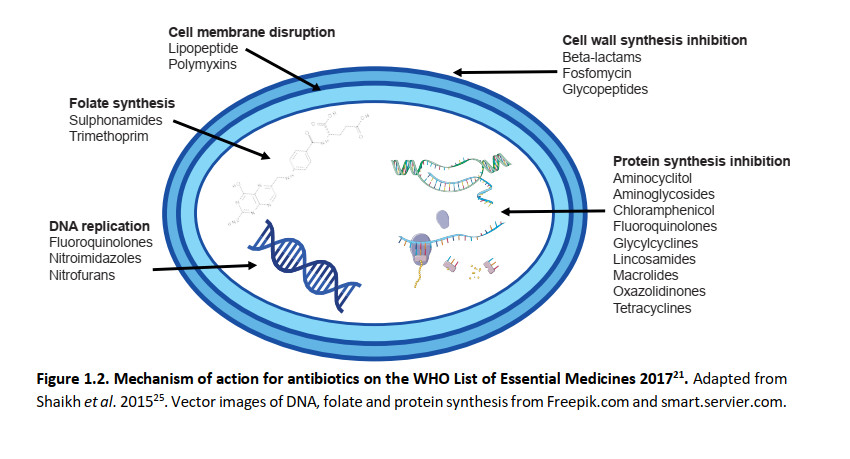
شکل ۱.۲ مکانیسم عمل آنتیبیوتیکها در فهرست داروهای ضروری سال ۲۰۱۷ سازمان بهداشت جهانی
جدول ۱.۲ آنتیبیوتیکهای موجود در نسخه بیستم فهرست داروهای ضروری سازمان بهداشت جهانی (۲۰۱۷). این آنتیبیوتیکها توسط WH O برای درمان عفونتهای باکتریایی ضروری هستند. سه دسته وجود دارد: دسترسی (گزینههای خط اول یا دوم برای عفونتهای مشترک)؛ مراقب باشید (پتانسیل مقاومت بالاتر اما هنوز هم به عنوان تیمار خط اول یا دوم توصیه میشود)؛ و رزرو (گزینه "آخرین راهحل" برای عفونتهای جدی مقاوم به آنتیبیوتیک). به گفته سازمان بهداشت جهانی، آنتیبیوتیکهای دسترسی، داروهای خط اول یا دوم برای بیماریهای عفونی مشترک هستند و باید به صورت گسترده در دسترس، مقرونبهصرفه، به طور مناسب فرموله شده و کنترل کیفی باشند. آنتیبیوتیکهای خط اول معمولا طیف باریکی هستند: آنها تنها طیف محدودی از باکتریها را هدف قرار میدهند، مانند باکتری بیماری زای مورد نظر و احتمالا برخی از اعضای نزدیک. آنها همچنین باید دارای پتانسیل مقاومت پایین و نسبت سود به ریسک مثبت باشند یعنی خطر آسیب به بیمار در مقایسه با درمان بالقوه عفونت آنها پایین است. آنتیبیوتیکهای طیف گسترده، که طیف وسیع تری از باکتریها را هدف قرار میدهند، به طور کلی به عنوان گزینههای خط دوم استفاده میشوند، مانند داروهایی با پتانسیل مقاومت بالاتر یا نسبت سود به ریسک کمتر (به عنوان مثال آنها ممکن است عوارض جانبی مشترک یا جدی تری داشته باشند).
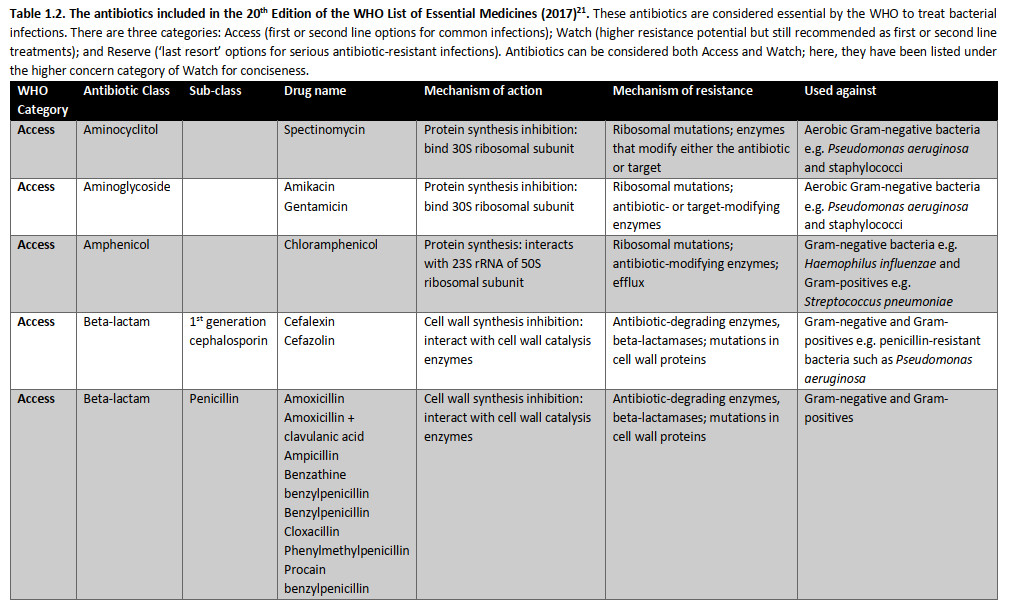
آنتیبیوتیکهای آمینو سیتوکلیتول، مانند اسپکتینومایسین، زیر واحد ۳۰ S ریبوزوم باکتریایی را متصل میکنند و سنتز پروتئین را مختل میکنند.
آمینوگلیکوزیدها مانند آمیکاسین و جنتامایسین از طریق مکانیسم مشابه عمل میکنند. برای انجام این کار، آنها باید از طریق غشا سیتوپلاسمی خود وارد سلول شوند، فرایندی که به ترانسپوت باکتریایی فعال وابسته به انرژی نیاز دارد.
این امر به نوبه خود نیازمند اکسیژن و نیروی محرکه پروتون فعال است.
بنابراین این داروها فقط برای باکتریهایی که قادر به تنفس هوازی هستند موثر هستند و آمینوگلیکوزیدها در مقابل باکتریهای بیهوازی که برای زنده ماندن بدون اکسیژن سازگار شدهاند و اجزای مورد نیاز معمول برای انتقال این داروها به داخل سلولهای خود را ندارند، غیرفعال محسوب میشوند. بنابراین، این داروها طیف گستردهای در نظر گرفته میشوند اما تنها برای طیف وسیعی از باکتریهای هوازی هستند.
اگرچه این آنتیبیوتیکها برای انسان سمی شناخته میشوند و میتوانند باعث کاهش شنوایی شوند، اما به عنوان خط اول درمان عفونتهای تنفسی در بیماران فیبروز کیستیک در نظر گرفته میشوند.
آنها همچنین برای درمان عفونتهای مقاوم به چند دارو (MDR)، اغلب به عنوان بخشی از درمان ترکیبی با بتالاکتام ها مورد استفاده قرار میگیرند، زیرا این دسته از آنتیبیوتیکها وقتی با هم استفاده شوند، اثر سینرژیک دارند. مقاومت آمینوگلیکوزیدی توسط جهشهای ریبوزومی، آنزیمهایی که آنتیبیوتیک یا آنزیمهایی که هدف را تغییر میدهند، میانجی گری میشود.
کلرآمفنیکل، یک amphenicol، یک آنتیبیوتیک طیف وسیع در نظر گرفته میشود و با rRNA ۲۳ S زیر واحد ریبوزومی ۵۰ S میانکنش میدهد و از سنتز پروتئین جلوگیری میکند. این روش خط اول برای عفونتهای چشمی مانند ورم ملتحمه است که میتواند توسط باکتریهایی از جمله هموفیلوس آنفلوانزا، استرپتوکوک پنومونیه و موراکسلا کاتارالیس ایجاد شود. مقاومت به کلرامفنیکل توسط جهشهای ریبوزومی یا آنزیمهای تغییر دهنده کلرامفنیکل میانجی گری میشود. همچنین میتواند به دلیل مقاومت با واسطه برونریزی باشد. جهش در اجزای سیستمهای برونریزی میتواند تمایل به مولکولهای خاصی از جمله آنتیبیوتیکها را افزایش دهد که منجر به افزایش مقاومت میشود.
بتالاکتام ها گروه متنوعی از آنتیبیوتیکها با چندین زیر گروه هستند.
این شامل پنیسیلینها، سفالوسپورین ها، کارباپنم ها و مونوباکتام ها است. آنتیبیوتیکهای بتا لاکتام ساختار شیمیایی مشابه دی - آلانیل - D - Alanine (D - Ala - D - Ala)دارند که یک "بلوک سازنده" دیوارهای سلول باکتریایی است. این بدان معنی است که بتالاکتام ها میتوانند با آنزیمهایی که سنتز دیواره سلولی را کاتالیز میکنند، از سنتز مناسب دیواره سلولی جلوگیری کنند و منجر به ناپایداری اسمزی و مرگ سلول باکتریایی شوند.
زیر ردههای مختلف بتالاکتام ها با اصلاح ساختار استاندارد بتالاکتام که آن گروه خاص را تعریف میکند، طبقهبندی میشوند.
پنیسیلینها و سفالوسپورین های نسل اول در لیست دسترسی آنتیبیوتیکها قرار دارند.
هر دوی این زیر طبقات از بتالاکتام ها معمولا طیف باریکی در نظر گرفته میشوند. اما طیف آن از دارویی به دارویی دیگر متفاوت است. برای مثال آموکسیسیلین در مقایسه با پنیسیلین اصلی طیف وسیع و یا طیف وسیع تری دارد.
Penicillins، به ویژه آموکسیسیلین، اولین داروی خط اول درمان عفونتهای باکتریایی شایع مانند عفونتهای دندانی، گوش، تنفسی و گلو هستند، از این رو جایگاه آنها به عنوان پر مصرف ترین داروها در دنیا است.
ژنهایی که آنزیمهای بتالاکتاماز را کد میکنند، که آنتیبیوتیکهای بتالاکتام را تجزیه میکنند، برخی از رایجترین ژنهای مقاومت آنتیبیوتیکی (ARG ها)بیش از ۱۰۰۰ ژن بتالاکتاماز مختلف هستند. بتالاکتام ها میتوانند در کنار یک مهار کننده بتالاکتاماز، مانند آموکسیسیلین با کلاولانیک، برای جلوگیری از عملکرد مناسب یک آنزیم بتالاکتاماز داده شوند. این ترکیب بازده آموکسیسیلین را افزایش میدهد. سفالوسپورین های نسل اول، مانند سفالکسین و سفازولین، اغلب به عنوان گزینههای خط دوم به عنوان جایگزین پنیسیلین در موارد مقاومت یا آلرژی استفاده میشوند. مقاومت بتا - لاکتامی همچنین میتواند با جهش یا تغییر در هدف آنتیبیوتیک (پروتئینهای متصل شونده به پنیسیلین (PBPs)در دیواره سلول)یا در پورینها میانجی گری شود، که به آنتیبیوتیکهای بتا - لاکتامی اجازه ورود به سلول را میدهد.
متابولیسم اسید فولیک مانع از ترکیب سولفامتوکسازول و تری متوپریم در برابر بسیاری از عفونتهای باکتریایی مختلف میشود. باکتریها باید از نو ترکیب شوند تا بتوانند به عنوان عوامل مشترک برای مسیرهای مختلف بیوسنتزی عمل کنند. بدون این عوامل رشد آنها مهار میشود. سولفونامیدها، مانند سولفامتوکسازول و تری متوپریم، یک آنتیبیوتیک دی آمینوپیریمیدین، آنزیمهای درگیر در مراحل مختلف مسیر سنتز اسید فولیک را مهار میکنند و در نتیجه این ترکیب به عنوان سینرژیستی در نظر گرفته میشود. این یک درمان خط اول شایع برای عفونتها از جمله عفونتهای مجاری ادراری (UTIs)، اسهال مسافرتی، عفونتهای پوستی استافیلوکوکوس اورئوس مقاوم به متی سیلین (MRSA)، عفونتهای دستگاه تنفسی و وبا است. مقاومت در برابر تری متوپریم توسط جهشهایی میانجی گری میشود که بیان اهداف تری متوپریم را افزایش میدهد به طوری که تعداد آنتیبیوتیکها بیشتر شده و اثر آن محدود میشود. جهشهایی که خود اهداف را تغییر میدهند یا به دست آوردن ژنهایی که اهداف با حساسیت کمتر را رمزگذاری میکنند نیز منجر به مقاومت به تریمتوپریم میشوند. مقاومت سولفونامید رایج است و عمدتا به دلیل ژنهای حامل پلاسمید است که آنزیمهای جایگزین را کدگذاری میکنند که حساسیت کمتری به آنتی بیوتیکها دارند. این یک روش انتقال افقی ژن (HGT)است: حرکت ژنها بین سلولهای باکتریایی که عبور عمودی را نادیده میگیرند.
نیتروایمیدازول، مترونیدازول، سنتز DNA را مهار میکند و باعث آسیب DNA در سلولهای باکتریایی بیهوازی میشود. باکتریهای هوازی سرسخت فاقد پروتیین حامل الکترون با پتانسیل احیای منفی کافی برای فعال کردن فرم پرودارو پس از ورود به سلول هستند در نتیجه مترونیدازول دارای طیف مخالف با آمینوگلیکوزیدها است. این اولین گزینه برای عفونتهای ناشی از باکتریهای بیهوازی مانند آبسههای دندانی (به عنوان مثال توسط پرووتلا یا استرپتو کوکوس) و یا واژینوز باکتریایی ناشی از گارنل یک انگل است. مقاومت با کاهش جذب و یا تغییر بازده کاهش (که منجر به کاهش جذب نیز میشود)میانجی گری میشود. غیر فعالسازی موثر و دارو نیز ممکن است، همانطور که به دست آوردن ژنهای nim از باکتریهای دیگر از طریق HGT است. این ژنهای nim آنزیمهای جایگزین ردوکتاز را کدگذاری میکنند تا پیش دارو را به یک جایگزین غیرسمی تبدیل کنند.
نیتروفوران، نیتروفورانتوئین، خواص ضد میکروبی متعددی دارد که هیچ کدام به طور کامل درک نمیشوند. همانند نیتروایمیدازول ها، این یک پرودارو است و در داخل سلول باکتریایی بوسیله عمل nitroreductases فعال میشود. متابولیت های واسطه تولید شده به ریبوزوم باکتریایی و آنزیمهای درگیر در سنتز DNA و RNA، به علاوه دیگر فرایندهای متابولیک متصل میشوند. این طیف گسترده با فعالیت علیه هردو گونه گرم منفی و گرم مثبت است، اگرچه برخی گونههای کلبسیلا و سودوموناس ذاتا مقاوم هستند و یک درمان خط اول برای UTIs های ساده و کمتر است. گمان میرود که مقاومت با جهش در nitroreductases میانجی گری شود.
Tetracyclines مانند داکسی سیکلین نوع دیگری از مهار کنندههای سنتز پروتئین هستند که براساس بخشهای حفاظتشده rRNA ۱۶ S در زیر واحد ۳۰ S عمل میکنند و از ترجمه جلوگیری میکنند. طیف گستردهای دارد و عموما برای درمان عفونتهای مقاربتی (STI)، بیماری لایم، عفونتهای پوستی و MRSA استفاده میشود. مقاومت توسط پمپهای تراوشی مخصوص تتراسایکلین و یا پروتئینهای حفاظت از هدف که تتراسایکلین را هنگامی که به ریبوزوم متصل است، دفع میکنند، میانجی گری میشود.
برچسب های مهم