
امروز جمعه ۲۱ اردیبهشت ۱۴۰۳
دسته بندی سایت
برچسب های مهم
پیوند ها
آمار بازدید سایت
اصطلاح فارماکودینامیک آنتیبیوتیک به روشی اشاره دارد که در آن آنتیبیوتیکها با ارگانیسمهای هدف خود تعامل دارند تا اثرات خود را اعمال کنند: آیا آنتیبیوتیک ارگانیسم را میکشد یا فقط از رشد آن جلوگیری میکند؟ آیا بهتر است که به طور همزمان مقدار زیادی آنتیبیوتیک تجویز شود یا برای مدت طولانی تری به غلظتهای پایینتر دست پیدا کنیم؟ متخصصان بالینی به طور فزایندهای این ملاحظات را در به حداکثر رساندن موفقیت درمان، به ویژه برای عفونتهای دشوار برای درمان و در بیماران با ضعف سیستم ایمنی، مهم میدانند.
تست Susceptibility
به طور معمول، فرد حساسیت یک ارگانیسم خاص به آنتیبیوتیک را براساس حداقل غلظت بازدارنده (MIC)برای ترکیب ارگانیسم - آنتیبیوتیک قضاوت میکند. از لحاظ کلاسیک، آزمایشگاه میکروبیولوژی MIC را با ترکیب غلظت استاندارد ارگانیسم که بیمار با افزایش غلظت آنتیبیوتیک رشد کردهاست تعیین میکند. از لحاظ تاریخی این کار در لولههای آزمایش انجام شد (شکل ۱ - ۴)، اما امروزه این کار بیشتر در صفحات میکرودیلوشن یا با سیستمهای خودکار انجام میشود. مخلوط برای حدود یک روز انکوبه میشود، و تکنسین آزمایشگاه لولهها یا صفحات (با چشم غیر مسلح یا کامپیوتر)را برای نشانههای حالت ابری بررسی میکند، که نشاندهنده رشد ارگانیسم است. مخلوط با کمترین غلظت آنتیبیوتیک که در آن هیچ رشد قابلمشاهدهای وجود ندارد، MIC فرض میشود. برای هر جفت ارگانیسم - آنتیبیوتیک، یک MIC قطع خاص وجود دارد که حساسیت را تعریف میکند. این MIC خاص نقطه شکست نامیده میشود. جدول ۱ - ۴ مثالهایی از نحوه تفاوت نقاط شکست برای ترکیبات مختلف ارگانیسم / پاتوژن و حتی براساس محل عفونت را نشان میدهد. توجه داشته باشید که تنها به این دلیل که یک آنتیبیوتیک کمترین MIC را برای یک پاتوژن دارد به این معنی نیست که بهترین انتخاب است - آنتیبیوتیکهای مختلف غلظتهای مختلفی را در بدن در مکانهای مختلف به دست میآورند. بنابراین، MICs آنتیبیوتیک برای یک ارگانیسم منفرد نباید در انتخاب درمان در داروهای مختلف مقایسه شود.
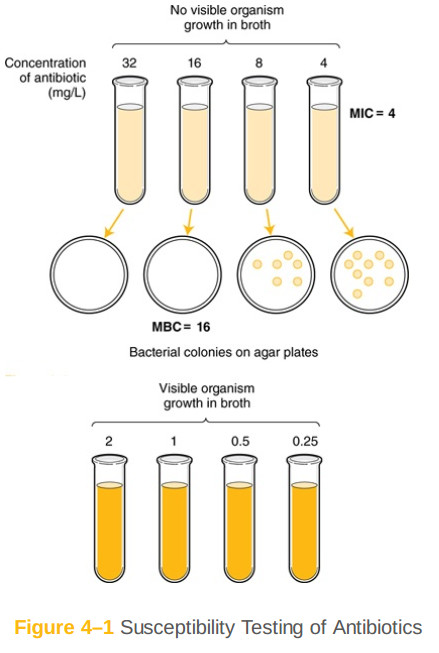
شکل ۱ - ۴: تست حساسیت آنتیبیوتیکها
جدول ۴ - ۱ مثالهایی از نقاط شکست حساسیت آنتی بیوتیک
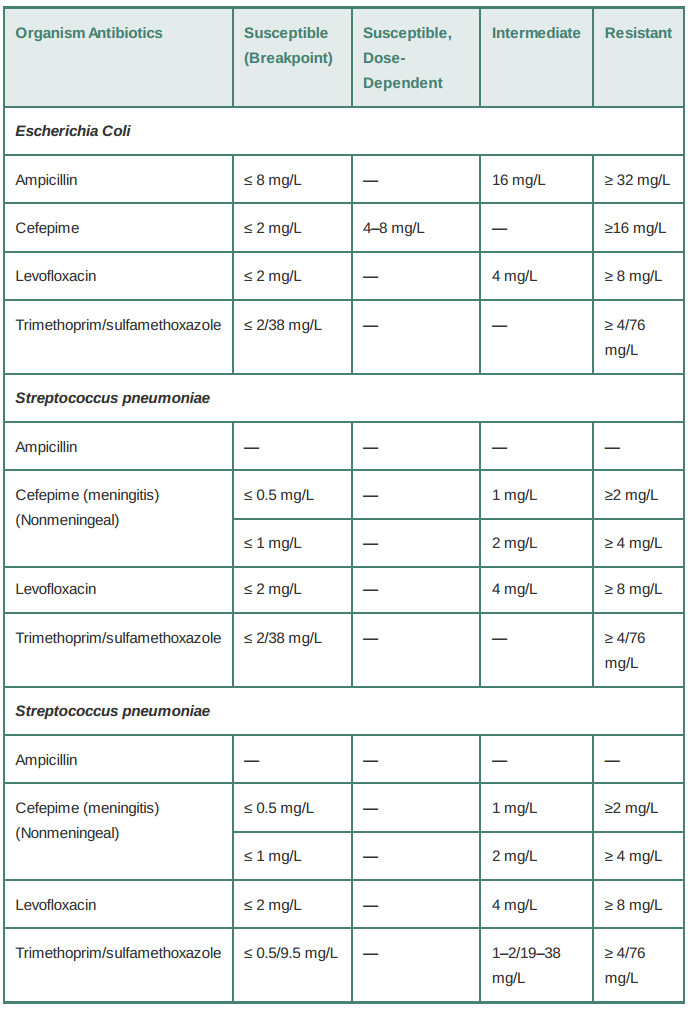
مقادیر MIC اغلب توسط درمانگرانی که تلاش میکنند بهترین درمان را برای بیماران خود انتخاب کنند اما ممکن است به طور ناخواسته تفاوتهای فارماکوکینتیک و فارماکودینامیک بین عوامل را نادیده بگیرند، به اشتباه تفسیر میشوند. برای مثال، در جدول ۱ - ۴، توجه داشته باشید که نقطه شکست لوفلوکساسین در برابر اشرشیاکلی ۲ mg / L و برای آمپیسیلین ۸ mg / L است. بنابراین اگر یک جدایه ای کولای در جریان خون بیمار دارای MIC ۱ mg / L برای لوفلوکساسین اما ۲ mg / L برای آمپیسیلین باشد، این بدان معنی نیست که لوفلوکساسین انتخاب بهتری برای آن بیمار است. لوفلوکساسین یک داروی وابسته به غلظت است که معمولا به مقدار ۵۰۰ - ۷۵۰ میلیگرم در روز تجویز میشود. آمپیسیلین یک داروی وابسته به زمان است که معمولا به صورت ۱ - ۲ گرم در هر ۴ - ۶ ساعت تجویز میشود. غلظتهای بسیار بالاتر آمپیسیلین در بدن (با توجه به دوزهای بالاتر)به این معنی است که ارگانیسمهایی با MIC بالاتر نسبت به آمپیسیلین هنوز به آن حساس هستند. به عبارت دیگر، این دو عدد به طور مستقیم قابلمقایسه نیستند. در واقع، اگر MIC ۸ mg / L برای هر دو دارو بود، ارگانیسم نسبت به لوفلوکساسین مقاوم و نسبت به آمپیسیلین حساس در نظر گرفته میشد.
همچنین در جدول ۱ - ۴ به دستههای "حساس"، "حساس"، "وابسته به دوز"، "متوسط" و "مقاوم" توجه کنید. "Susceptible" و "مقاوم" خود explanatory هستند، اما اصطلاحات دیگر به چه معناست؟ "Intermediate " یک دامنه ضعیف تعریفشده که در آن درمان موفق ممکن است در برخی شرایط امکان پذیر باشد، مانند زمانی که دارو به طور همزمان حذف میشود (برای عفونت دستگاه ادراری)و یا در صورتی که دوز بالاتری داده شود. این بیشتر یک ناحیه خاکستری است که برای جدا کردن دو اصطلاح قطعی ساخته شدهاست تا یک تعریف علمی. "Susceptible، وابسته به دوز" دقیقا همان چیزی است که به نظر میرسد - ارگانیسم ممکن است نسبت به دوزهای بالای دارو حساس باشد اما به احتمال زیاد نسبت به دوزهای پایین مقاوم باشد. این امر به این دلیل ایجاد شد که بسیاری از این داروها در دوزهای مختلف مورد استفاده قرار میگیرند و دوز کم سفپیم مانند ۱ g IV q۱۲h ممکن است برای درمان عفونت اشریشیاکلی با MIC ۲ mg / L کافی باشد اما یک دوز مانند ۲ g IV q۱۲h ممکن است در صورتی که MIC ۴ mg / L باشد مورد نیاز باشد. همه اینها ممکن است مانند قوانین سخت و سریع به نظر برسند، اما آنها واقعا احتمال این را دارند که بیشتر بیماران در مواجهه با ترکیب دارویی - باگ خاصی برای عفونتشان چگونه رفتار خواهند کرد. برخی حتی با MICs های بالا هم موفق میشوند، و برخی حتی با MICs های پایین هم شکست میخورند.
در نهایت، آگاه باشید که روشهای دیگر آزمایش حساسیت وجود دارند، از جمله انتشار دیسک و آزمایشها E-tests,، اما روشهای رقیقسازی در براث معمولا استاندارد طلایی در نظر گرفته میشوند.
متوقف کننده استاتیک در برای کشنده یا سیدال
در MIC آنتیبیوتیک رشد را مهار میکند اما ممکن است واقعا ارگانیسم را بکشد یا نکشد. آنتیبیوتیکها که رشد ارگانیسم را بدون کشتن آن مهار میکنند، باکتریواستاتیک (یا fungistatic در مورد قارچ)نامیده میشوند. اگر آنتیبیوتیکها حذف شوند، موجودات زنده میتوانند دوباره شروع به رشد کنند. با این حال، آنتیبیوتیکهای باکتریواستاتیک معمولا در درمان عفونتها موفق هستند چون به سیستم ایمنی بیمار این امکان را میدهند که به دام بیفتد و موجودات زنده را از بین ببرد. دیگر آنتیبیوتیکها باکتریسیدال در نظر گرفته میشوند. عمل آنها باعث مرگ موجودات زنده بدون کمک سیستم ایمنی میشود.
برای بیشتر عفونتها، نتایج استفاده از داروهای باکتریواستاتیک مناسب در مقابل داروهای باکتریسیدال مشابه هستند؛ اما برای برخی از عفونتها داروهای باکتریسیدال ترجیح داده میشود. چنین عفونتهایی شامل اندوکاردیت، مننژیت، عفونت در بیماران نوتروپنیک و احتمالا استئومیلیت هستند. سیستم ایمنی ممکن است به دلیل موقعیت آناتومیک و یا سرکوب سیستم ایمنی بیمار، در مبارزه با این عفونتها چندان موثر نباشد. فعالیت باکتری کشی با گرفتن یک نمونه از محیط کشت در غلظتهای مختلف و در زیر و گسترش محیط کشت بر روی پلیت های آگار تعیین میشود (شکل ۱ - ۴). کلونی های باکتریایی روی صفحات شمارش میشوند و غلظت متناظر با ۹ / ۹۹ % کاهش (۳ - log)در مایه تلقیح باکتریایی اصلی، حداقل غلظت باکتری کشی (MBC)در نظر گرفته میشود. زمانی که MBC چهار برابر یا کمتر از MIC باشد، دارو به عنوان باکتری کشی در نظر گرفته میشود؛ اگر نسبت MBC / MIC بزرگتر از چهار باشد به صورت باکتریواستاتیک در نظر گرفته میشود. آزمایش MIC در بسیاری از آزمایشگاهها استاندارد است؛ آزمایش MBC سختتر است و معمولا در عمل بالینی انجام نمیشود. جدول ۲ - ۴ داروها را لیست کرده و نشان میدهد که آیا آنها به طور کلی باکتریواستاتیک یا باکتریسیدال در نظر گرفته میشوند. با این حال لازم به ذکر است که این فعالیت میتواند بسته به عامل بیماری زا، دوز مصرفی و مرحله رشد باکتری متفاوت باشد.
جدول ۴ - ۲ پارامترهای فارماکودینامیکی آنتیبیوتیک
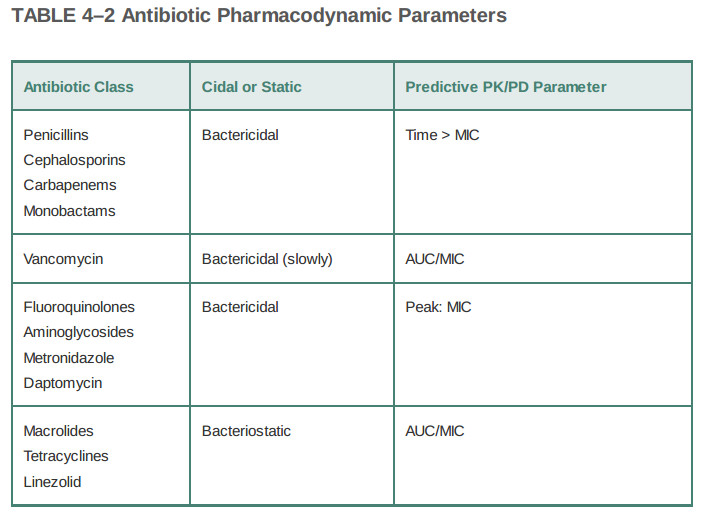
روابط Pharmacokinetic / فارماکودینامیک
علاوه بر تفاوت در اینکه آیا آنها میکرو ارگانیسمها را میکشند یا فقط مانع از رشد آنها میشوند، آنتیبیوتیکها نیز در نحوه بروز اثرات خود در طول زمان متفاوت هستند. مطالعات دقیق نشان دادهاند که برای آنتیبیوتیکهای خاص، فعالیت علیه میکروارگانیسمها با مدتزمان زمانی که غلظت دارو بالاتر از MIC باقی میماند (فعالیت وابسته به زمان)مرتبط است. برای سایر آنتیبیوتیکها، فعالیت ضدباکتریایی نه با زمان بالای MIC بلکه با نسبت غلظت بیشینه دارو به MIC (فعالیت وابسته به غلظت یا مستقل از زمان)مرتبط است. برای برخی آنتیبیوتیکها بهترین پیشبینیکننده فعالیت نسبت سطح زیر منحنی غلظت - زمان (AUC)به MIC است. شکل ۲ - ۴ این پارامترهای فارماکوکینتیک / فارماکودینامیک (PK / PD)را به صورت شماتیک نشان میدهد، و جدول ۲ - ۴ نشان میدهد که کدام پارامتر پیشبینیکننده بیشترین تاثیر برای کلاسهای آنتیبیوتیک است. پیامدهای عملی این یافتهها در طراحی برنامههای آنتیبیوتیک است: آمینوگلیکوزیدها امروزه به طور مداوم به عنوان یک دوز بزرگ روزانه برای نفوذ در فعالیت وابسته به غلظت داده میشوند، در حالی که برخی از پزشکان داروهای بتالاکتام مانند سفتازیدیم را به دلیل فعالیت وابسته به زمان مصرف میکنند. همانطور که مقادیر هدف برای این پارامترها که کارایی را پیشبینی میکنند یافت میشوند، ممکن است افزایش در شخصی سازی دوز آنتیبیوتیکها برای رسیدن به این مقادیر هدف وجود داشته باشد.
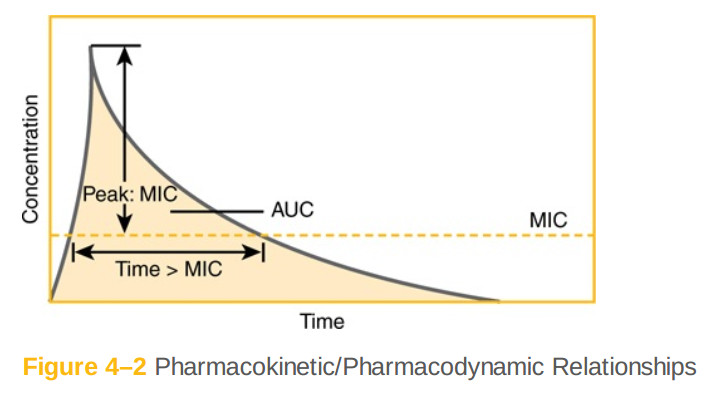
شکل ۴ - ۲ روابط فارماکوکینتیک / فارماکودینامیک