
امروز پنجشنبه ۲۰ اردیبهشت ۱۴۰۳
دسته بندی سایت
برچسب های مهم
پیوند ها
آمار بازدید سایت
با ظهور sequencing نسل بعدی، ما توانایی بیسابقهای برای مطالعه تومور و ژنوم میزبان و همچنین طیف وسیعی از میکرو ارگانیسمهایی که در موجودات زنده وجود دارند، داریم. شواهد نشان میدهد که این میکروبها ممکن است نسبت به برخی سرطانها حساسیت نشان دهند و همچنین ممکن است بر پاسخ به درمان تاثیر بگذارند. یک نمونه بارز از این مورد با ایمونوتراپی دیده میشود، که برای آن میکروبهای روده در تاثیرگذاری بر پاسخهای درمانی در مدلهای پیش بالینی و گروههای بیمار دخیل بودهاند. با این حال، این میکروبها ممکن است بر پاسخ به انواع دیگر درمان نیز تاثیر بگذارند و همچنین ممکن است بر سمیت مربوط به درمان تاثیر بگذارند. براساس این تاثیرات، علاقه زیادی به هدف قرار دادن این میکروبها در درمان سرطان و دیگر بیماریها وجود دارد. با این حال، پیچیدگیهایی وجود دارد، و درک عمیقتر تعاملات میزبان - میکروبیوم برای تحقق پتانسیل کامل چنین رویکردهایی حیاتی است. این مفاهیم و ابزارهایی که از طریق آنها چنین یافتههایی میتوانند به کلینیک ترجمه شوند در اینجا مورد بحث قرار خواهند گرفت.
در حال حاضر مقالات فراوانی وجود دارد که نشان میدهد اختلال در هومئوستاز جوامع میکروبی (به نام دیس بیوزیس)با شرایط پاتولوژیک از بیماریهای عصبی گرفته تا بیماریهای متابولیک و قلبی - عروقی و اختلالات گوارشی ارتباط دارد. علاوه بر این، نتایج حاصل از مطالعات متعدد نشان میدهد که ارتباطی بین میکروبیوتای کامنسال و سرطان وجود دارد، از جمله شواهد اخیر مبنی بر نقش میکروبیوتای دستگاه گوارش (روده)در تعدیل پاسخهای ایمنی سرطان و دادههایی که نشان میدهند جوامع میکروبی درون میکرومحیط تومور میتوانند به اثربخشی درمانی کمک کنند. به طور مهمی، استراتژیهای هدف قرار دادن میکروبیوتا در سراسر طیف بیماریهای انسانی، با برخی شواهد از موفقیت به کار گرفته میشوند؛ با این وجود، پیچیدگیهایی وجود دارد و هنوز سوالات زیادی در مورد چگونگی هدف قرار دادن دستگاه گوارش و microbiotas تومور وجود دارد. با این حال، ما بر تاثیر میکروبیوتای همسفرگی در گستره سلامت و بیماری تاکید میکنیم و در مورد نقش در حال ظهور روده و میکروبیوتای تومور در پاسخ به درمان سرطان بحث میکنیم و اینکه آیا تلفیق آنها میتواند به عنوان یک جایگزین مناسب برای درمانهای ضد سرطان معمولی عمل کند یا خیر.
دیسبیوزیس روده و توسعه سرطان
میکروبیوم روده به طور فزایندهای به خاطر تاثیر آن در سلامتی و بیماری شناخته شدهاست . این امر در مورد سرطان نیز صادق است، که در آن باکتریها و ویروسهای ویژهای در دیسپلازی سلولی و سرطانزایی دخیل بودهاند (شکل ۱)
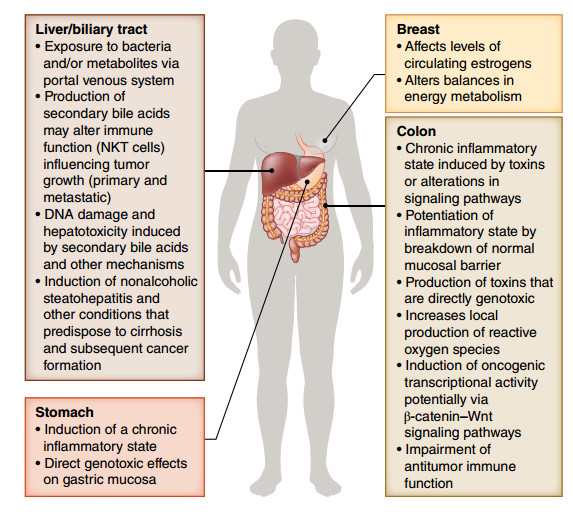
باکتریهای روده سرطان زای شناختهشده عبارتند از: سالمونلا تایفی و گونه های هلیکوباکتر در سرطان صفراوی و هلیکوباکتر پیلوری در سرطان معده
در بیشتر این موارد، اعتقاد بر این است که سرطانزایی ثانویه به ایجاد یک حالت التهابی مزمن موضعی است؛ با این حال، برخی باکتریها، از جمله هلیکوباکتر پیلوری، اثرات ژنوتوکسیک مستقیم دارند و میتوانند مسیرهای سیگنال دهی داخل سلولی کلیدی را تغییر دهند که رشد و تکثیر سلولهای مخاطی را تنظیم میکنند. قابلذکر است که هلیکوباکتر پیلوری هم با آدنوکارسینوم معده و هم با التهاب لنفوئیدی مخاط مرتبط است (لنفوم MALT)و توسط سازمان بهداشت جهانی (WHO)به عنوان سرطانزای کلاس ۱ شناخته میشود.
علاوه بر این، شواهدی نیز وجود دارد که از این عقیده حمایت میکند که دیسبیوزیس تعمیمیافته در میکروبیوتای روده ممکن است به سرطانزا کمک کند. ارتباط بین دورههای مکرر آنتیبیوتیک و توسعه انواع تومورهای دستگاه گوارش و غیر گوارشی در مطالعات بزرگ مورد - شاهدی نشانداده شدهاست. مکانیسمهایی که دیسبیوزیس از طریق آنها بر تومورزایی و / یا رشد تومور در انواع سرطان تاثیر میگذارد متعدد و متنوع هستند (شکل ۱)؛ با این حال، هنوز شناخت جامع mechanistic در دست نیست و مطالعات برای درک بهتر چگونگی تاثیر میکروبهای رودهای بر سرطان در حال انجام است.
برتری شواهد حامی نقش سببی برای دیسبیوزیس روده به عنوان تعدیلکننده توسعه سرطان در سرطان روده بزرگ (CRC)است (شکل ۱).
برای مثال، میکروبیوتای تومور (که میکروبیوتای مرتبط با سرطان آدنوما است)به وضوح متفاوت از میکروبیوتای سالم مجاور است، و شواهد مدلهای پیش بالینی نشان میدهد که پیوند مدفوع از بیماران مبتلا به CRC یا سرطان کلورکتال میتواند تشکیل پولیپ را القا کند، سیگنالهای پیش سرطانزا را تحریک کند، و محیط ایمنی موضعی را در موشها در مقایسه با کنترل تغییر دهد.
علاوه بر این، شواهدی از مدلهای پیش بالینی مختلف و برخی مطالعات انسانی، دیسبیوزیس را به عنوان یک محرک تومورزا در CRC نشان داده است. گونههای خاص باکتریایی میتوانند یک حالت التهابی را تحریک کنند که میتواند سرطانزایی را از طریق القا توکسینهای پیش التهابی (مانند آنهایی که توسط باکتریها تولید میشوند)، افزایش تولید گونههای فعال اکسیژن و تغییر در مسیرهای سیگنال دهی (فوزوباکتریوم نوکلئوتوم) در تومورهای انسانی و در مدلهای موشی، افزایش دهند، یا ممکن است برای جلوگیری از عملکرد ایمنی تومور عمل کنند (فوزوباکتریوم نوکلئاتوم).
حالت التهابی مزمن ممکن است به خودی خود موجب دیسبیوزیس شود، زیرا نقص ژنتیکی در ژنهای کلیدی تعدیلکننده التهاب، تجمع باکتریهای ویژهای از جمله اشرشیاکلی را افزایش میدهد. متناوبا، تولید متابولیت هایی که به طور مستقیم ژنوتوکسیک هستند (مانند تولید کلی باکتین از اشرشیاکلی یا سم اتساع سیتولئال توسط کمپیلوباکتر ژژونی نشانداده شدهاست که باعث ایجاد سرطان در موش میشود. در نهایت، اجزای فوزوباکتریوم نوکلئاتوم ، از جمله کمپلکس چسبندگی FadA (FadAc)، میتوانند مسیر سیگنال دهی - کاتین - وین را در ردههای سلولی سرطان روده بزرگ انسان فعال کنند که منجر به تغییرات نسخهبرداری انکوژنیک میشود.
برچسب های مهم