
امروز جمعه ۲۱ اردیبهشت ۱۴۰۳
دسته بندی سایت
برچسب های مهم
پیوند ها
آمار بازدید سایت
استفاده از عوامل بیولوژیک به عنوان سلاح در جنگ و تروریسم در طول تاریخ ثبت شدهاست.

هنگامی که لباسها و پتوهای آلوده به واریولا در قرن ۱۵ به بومیان آمریکای جنوبی تحویل داده شدند، سربازان اروپایی از آبله به عنوان اسلحه بیولوژیکی استفاده کردند. در طول جنگهای فرانسه و سرخ پوست های آمریکایی (۱۷۵۴ - ۱۷۶۷)، سربازان انگلیسی از پتوهای آلوده به واریولا برای شروع شیوع آبله در میان سرخپوستان ، استفاده کردند. بیش از نیمی از قبایل درگیر در این بیماری همهگیر شدند.
با توقف واکسیناسیون عادی آبله در اوایل دهه ۱۹۸۰، انتشار تدریجی این بیماری میتواند به طور بالقوه فاجعهآمیز باشد. در طول چند دهه گذشته، نگرانی فزایندهای در مورد استفاده از عوامل ویروسی به عنوان سلاحهای کشتار جمعی وجود داشتهاست، به خصوص به این دلیل که آنها به طور بالقوه در یک جمعیت حساس بسیار مسری هستند، نسبت مرگ و میر بالایی دارند، و، به جز آبله، استراتژیهای واکسیناسیون محدودی وجود دارد. عوامل ویروسی بالقوه شامل آبله، ویروسهای تب خونریزی دهنده، ویروس Nipah، ویروس آنسفالیت اسبی ونزوئلا، و hantaviruses هستند. برخی دیگر مانند آنفولانزا نیز عوامل بالقوه ای هستند.
ویروس تب خونریزی دهنده ویروسی: Viral Hemorrhagic Fever Viruses
تب خونریزی ویروسی (VHF)به گروهی از عوامل ویروسی اشاره دارد که تعدادی از ویژگیها را به اشتراک میگذارند. .آنها همه ویروسهای RNA احاطه شده با انولوپ هستند و به یک منبع میزبان حیوان یا حشره نیاز دارند. آنها از نظر جغرافیایی محدود به مناطق خاصی از جهان هستند که در آنجا عفونت انزوتیک ایجاد میکنند. بیماری انسان به صورت تک گیر است و معمولا به دنبال قرار گرفتن تصادفی در معرض بزاق، ادرار یا مدفوع حیوانات آلوده، گزش حشرات، و یا گاهی از انسان به انسان به خاطر قرار گرفتن در معرض بافت آلوده و یا مایعات بدن است
عوامل VHF عبارتند از arenaviruses ها [ تب لاسا و ویروسهای تب خونریزی دهنده آمریکای جنوبی (SAHF)]، bunyaviruses [Hantvirus و ویروس تب خونریزی دهنده کریمه کنگو (CCHF)]، فلاوی ویروسها [ تب خونریزی دهنده دانگ (DHF)، آنسفالیت آلوده به کنه، و ویروسهای تب زرد ]، و ویروس فیلو ویروسها (ابولا و ماربورگ).
arenaviruses [Lassa fever and South American hemorrhagic fever viruses (SAHF)], bunyaviruses [Hantavirus and Crimean-Congo hemorrhagic fever virus (CCHF)], flaviviruses [Dengue hemorrhagic fever (DHF), tick-borne encephalitis, and yellow fever viruses], and filoviruses (Ebola and Marburg viruses).
در بیشتر موارد، تنها درمان و واکسیناسیون محدودی برای افراد آلوده و یا در معرض این عوامل وجود دارد. اگر چه هیچ مدرک آشکاری مبنی بر خلعسلاح این عوامل وجود ندارد، اما این امکان وجود دارد که آنها را بتوان با aerosolization منتشر کرد و به عنوان سلاحهای کشتار جمعی مورد استفاده قرار داد.
ویژگیهای اپیدمیولوژیک این گروه از ویروسها در جدول زیر گزارش شدهاست

عفونت طبیعی با یک عامل VHF در مناطق جغرافیایی محدود دیده میشود و انتقال به انسان معمولا از گزش پشه یا کنه یا تماس مستقیم حیوانات آلوده و یا استنشاق آئروسل های آلوده پیروی میکند. انتقال به انسانها پس از تماس با تجهیزات پزشکی آلوده با ویروس ابولا توصیف شدهاست و انتقال انسان به انسان با ویروسهای ابولا / ماربورگ، CCHF، تب لاسا و جونین رخ میدهد.
به عنوان یک گروه، عوامل VHF به hematogenously چندین عضو گسترش مییابند که در آنجا بستر عروقی را هدف قرار میدهند و باعث آسیب میکرو واسکولار و تغییرات مشخص در نفوذ پذیری عروقی میشوند. علایم شدید عفونت از اثر متقابل نفوذپذیری عروقی، آزاد شدن سیتوکین های پیش التهابی، عوامل سیتوتوکسیک و اتوآنتی بادی ها، فعال شدن کمپلمان و اختلال انعقادی سیستمیک ناشی میشود. بیماران مبتلا به DHF سطوح افزایشیافته گیرنده فاکتور نکروز تومور (TnF)، اینترلوکین IL-8 و اینترفرون (IFN) گاما را نشان میدهند و غلظتهای کمتر IL - ۶ را نشان میدهند که با افزایش نفوذپذیری عروقی مرتبط است. سطوح افزایشیافته IL - ۲، IL - ۱۰، ، و IFN در افراد آلوده به ویروس ابولا نشان داده شدهاند. اگر چه نکروز در کبد و دیگر بافتها مشهود است اما نفوذ سلولهای التهابی اغلب وجود ندارد.
از لحاظ بالینی، VHF معمولا با تب، myalgias، سردرد و خستگی همراه است (جدول ۲).
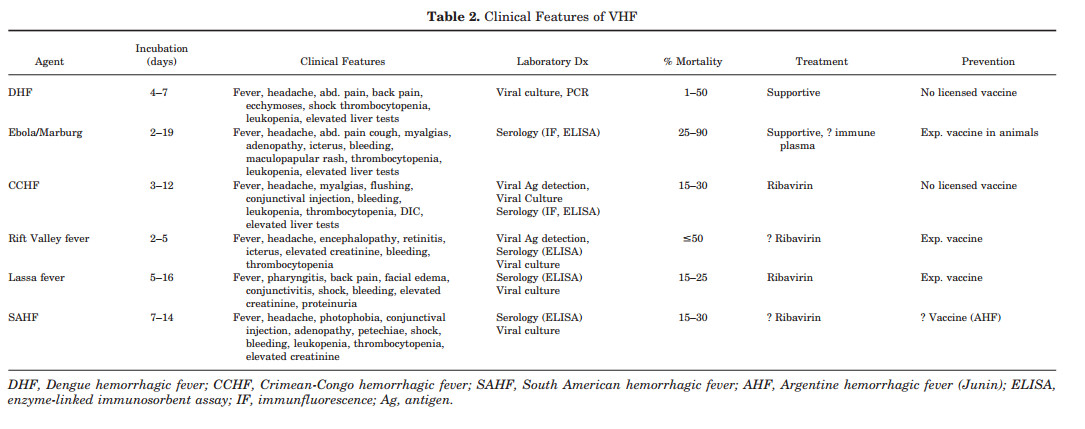
دورههای Incubation معمولا کوتاه بوده و از ۲ تا ۱۹ روز طول میکشد. اغلب آنها تب ناگهانی همراه با سردرد شدید و myalgias شدید دارند. درد در سینه، کمر و شکم در DHF، ابولا / ماربورگ و تب لاسا رخ میدهد. Conjunctival injection معمولا در تب لاسا، CCHF و SAHF مشاهده میشود. نارسایی کلیوی در تب لاسا و تب دره ریفت دیده میشود و آسیب کبدی قابلتوجهی در تب DHF، ابولا / ماربورگ و CCHF مشاهده میشود. وجود پروتیینوری به پیشبینی تب لاسا و SAHF کمک میکند. به استثنای تب لاسا، ترومبوسیتوپنی و لکوپنی قابلتوجه شایع هستند و خونریزی آشکار را می توان مشاهده کرد.
تشخیص VHF را می توان با استفاده از تشخیص آنتیژن ویروسی در CCHF و تب دره ریفت , با واکنش زنجیرهای پلیمراز در DHF و Ebola , از نظر سرمی ( ایمونوفلورسنس یا الایزا ) در ابولا / ماربورگ , تب دره ریفت , تب لاسا یا SAHF , تایید کرد .
به استثنای DHF، مهار میکروبیولوژیک تخصصی (سطح ایمنی زیستی ۴)برای کنترل ایمن این عوامل مورد نیاز است. درمان پزشکی نیازمند مراقبتهای ویژه در بیمارانی است که به شدت بیمار هستند و وضعیت همودینامیک، خونی، عصبی و کلیوی بیمار را تحت نظر دارند. اگر چه مراقبت حمایتی درمان اصلی DHF است، اما نشانداده شدهاست که ریباویرین داروی ضد ویروسی در تب CCHF و تب لاسا مفید بوده و احتمالا در تب ریفت و تب خونریزی دهنده آرژانتین موثر است (جدول ۲). نشاندادهشده که پلاسمای نقاهت حاوی آنتیبادیهای خنثیکننده، بقا را در افراد مبتلا به اشکال خاصی از SAHF (تب خونریزی دهنده بولیوی و ونزوئلا)و احتمالا افراد مبتلا به ابولا بهبود میبخشد. به استثنای DHF، خون و ترشحات بیماران مبتلا به VHF حاوی مقادیر زیادی ویروس است. از این رو این بیماران مشکلات قابلتوجهی در کنترل عفونت بیمارستانی دارند. دستورالعملهای مدیریت و کنترل VHF در جای دیگری بررسی شدهاند. با وجود درمان تهاجمی، مرگ و میر برای بیماران VHF بالا باقی میماند، از ۱ % با تب دنگی بدون عارضه تا ۹۰ % با ابولا (جدول ۲). عوارض دراز مدت ممکن است شامل ناشنوایی عصبی هشتم و آلوپسی در تب لاسا و رتینیت در تب ریفت باشد. نگرانی بزرگتر، عدم وجود واکسنهای تایید شده یا رژیمهای شیمیدرمانی قطعی برای جلوگیری از عفونت است. یک واکسن ویروسی زنده تخفیف یافته موثر برای تب خونریزی دهنده آرژانتین اخیرا در انسان و حیوانات توصیف شدهاست و ممکن است دارای اثر حفاظتی متقابل برای سایر اشکال SAHF باشد. فیشر - هوچ و همکاران کارآیی حفاظتی یک ویروس واکسینیا - که پروتیینهای ساختاری ویروس تب لاسا را در یک مدل macaque بیان میکند را گزارش کردهاند. در مقایسه با حیوانات غیر ایمن شده، آنهایی که گلیکوپروتئین های بیانکننده G۱ و G۲ را دریافت کردند به طور قابلتوجهی در برابر عفونتهای ویروسی زنده محافظت شدند. دو مطالعه اخیر تاثیر واکسنهای پیشگیرانه را در مدلهای حیوانی عفونت ابولا نشان دادهاند. Xu و al۲۷ خوکچه هندی را با پلاسمید DNA کد کننده نوکلئوپروتئین ویروسی ابولا یا گلیکوپروتئین های ترشحی یا غشایی مرتبط ایمن سازی کردند. حیواناتی که با پلاسمید کد کننده گلیکوپروتئین های DNA واکسینه شده بودند، در مقایسه با حیوانات کنترل ایمن نشده، در برابر مرگ و میر بعد از عفونت حفاظت شدند. سالیوان و دیگران اثر محافظتی DNA و به دنبال آن تقویت ایمنی با ناقل آدنوویروسی که گلیکوپروتئین های ویروسی Ebola و نوکلئوپروتئین را در یک مدل اولیه غیر انسانی بیان میکند را نشان دادند. علاوه بر این، مطالعه اخیر در مورد ایمنی و کارایی واکسن زنده تخفیف یافته ویروس دنگی در انسان گزارش دادهاست. تاکنون گزارشهای محدودی در مورد اثر حفاظتی سرم ایمنی یا ریباویرین در جلوگیری از عفونت با عوامل VHF وجود داشتهاست. گوپتا و همکارانش گزارش دادند که آنتی سرمهای نوع خاص و چند کلونی در موشهای ایمن شده با ویروس زنده ابولا، ۵۶ % از موشها را از عفونت حفاظت کردند. Chemoprophylaxis با استفاده از ریباویرین توانایی محدودی در بهبود سیر تب خونریزی دهنده در ارهسوس ماکاکوس آرژانتین دارد، اگرچه ممکن است در پیشگیری از تب دره ریفت و عفونتهای CCHF نقش داشته باشد. کمپلکس ویروس انسفالیت استوایی ونزوئلا
ویروس آنسفالیت اسبی ونزوئلا (Vae)به ویروسهای منتقله از پشه اشاره دارد که باعث بیماری انسان در آمریکای مرکزی، مکزیک و گاهی در ایالاتمتحده میشود. Equines به عنوان میزبان تقویتکننده و منبع عفونت پشه عمل میکنند.. عفونت با آنسفالیت اسب غربی و یا آنسفالیت اسب شرقی از نظر بالینی غیرقابلتشخیص است. با این حال، به دلیل دوز عفونی کمتر انسان، VEE بیشتر کاندی استفاده به عنوان سلاح بیولوژیک است. آخرین شیوع بیماری در ونزوئلا و کلمبیا در سال ۱۹۹۵ رخ داد که در طی آن نزدیک به ۱۰۰۰۰۰ نفر به این بیماری مبتلا شدند که این امر نشاندهنده حساسیت بالای این جمعیت نسبت به این بیماری میباشد. به دلیل این که بیماری در اسب بیماری زا است، عفونت میتواند تلفات عمدهای را در جمعیت اسب و الاغ ایجاد کند. عفونتهای طبیعی ممکن است منجر به ۳۰ تا ۹۰ درصد مرگ و میر در اسبها شوند. اگر چه تصور نمیشود که انتقال انسان به انسان رخ دهد، VEE به دلیل دوز عفونی کم انسان، تولید آسان و توزیع بالقوه آن با آئروسل سازی عمدی و یا با آزاد کردن پشههای عفونی، به عنوان یک سلاح بیولوژیک موثر مورد مطالعه قرار گرفتهاست. در دهههای ۱۹۵۰ و ۱۹۶۰، چندین کشور، از جمله ایالاتمتحده، مطالعاتی را در مورد VEE انجام دادند. با این حال، انبارهای آمریکا،در سال 169 تخریب شد. پتانسیل VEE برای bioweapon موثر بعد از آئروسل شدن با این آگاهی تقویت میشود که برخی اشکال به شدت عفونی هستند و به راحتی میتوانند دسترسی مستقیم به سیستم عصبی مرکزی از طریق مجرای بویایی را به دست آورند. عفونت VEE طبیعی معمولا یک بیماری خود محدود است که شامل تب، لرز، ضعف و سردرد شدید با کمتر از ۱ % بزرگسالان و ۴ % کودکان در حال پیشرفت به انسفالیت شدید است. Ataxia، تشنج، فلج و کما ممکن است انسفالیت را پیچیده کند و مرگ و میر ممکن است به ۲۰ % برسد. عفونت در دوران بارداری ممکن است باعث نقایص عصبی - آناتومیک جنین و یا سقط خود به خودی شود. تشخیص با تشخیص ویروس در مایع مغزی - نخاعی توسط کشت و یا واکنش زنجیرهای پلیمراز تایید میشود. نمونهها باید در سطح ایمنی زیستی ۳ آزمایشگاه به کار گرفته شوند. اگر چه سرم بیماران مبتلا به انسفالیت ممکن است منفی باشد، آنتیبادیهای اختصاصی نوع VEE در سرم یا نمونههای مایع مغزی نخاعی نیز تشخیص را پیشنهاد میکنند.
هیچ عامل ضد ویروسی قطعی برای VEE وجود ندارد؛ بنابراین درمان عمدتا حمایتی است. با این حال، لوکاسوسکی و بروکس نقش بالقوه پروسه pegylated اینترفرون آلفا در VEE گزارش کردهاند. درمان موشهای عفونی VEE با IFN آلفا pegylated به طور قابلتوجهی بقا را از عفونت با آئروسل یا عفونت زیر جلدی بهبود بخشید. قرنطینه مورد نیاز نیست اما روشهای کنترل پشه در صورت شیوع بیماری باید مورد استفاده قرار گیرند. مطالعات محدود، کارایی حفاظتی را در حیوانات آزمایشگاهی از یک واکسن غیرفعال شده با فرمالین و اخیرا از یک واکسن ویروسی تضعیفشده زنده و واکسن نوترکیب ویروس واکسینیا که ناحیه ژن ساختاری VEE را کد میکند، نشان دادهاست.
ادامه دارد